Clear Sky Science · it
Analisi su larga scala a singola cellula e perturbazione in silico rivelano l’evoluzione dinamica dell’HCC: dall’inizio al targeting terapeutico
Perché la vita interna del fegato canceroso è importante
Il carcinoma epatocellulare, la forma più diffusa di tumore del fegato, è notoriamente difficile da trattare. Molti pazienti non rispondono bene ai farmaci attuali e i tumori spesso recidivano o si diffondono. Un motivo importante è che ogni tumore è un miscuglio caotico di cellule diverse che evolvono nel tempo e comunicano costantemente con l’ambiente circostante. Questo studio utilizza potenti tecnologie di lettura genica a singola cellula e spaziali per osservare quell’evoluzione, cellula per cellula, dalla crescita tumorale iniziale alla malattia avanzata resistente ai trattamenti, e per individuare punti deboli che nuove terapie potrebbero sfruttare.
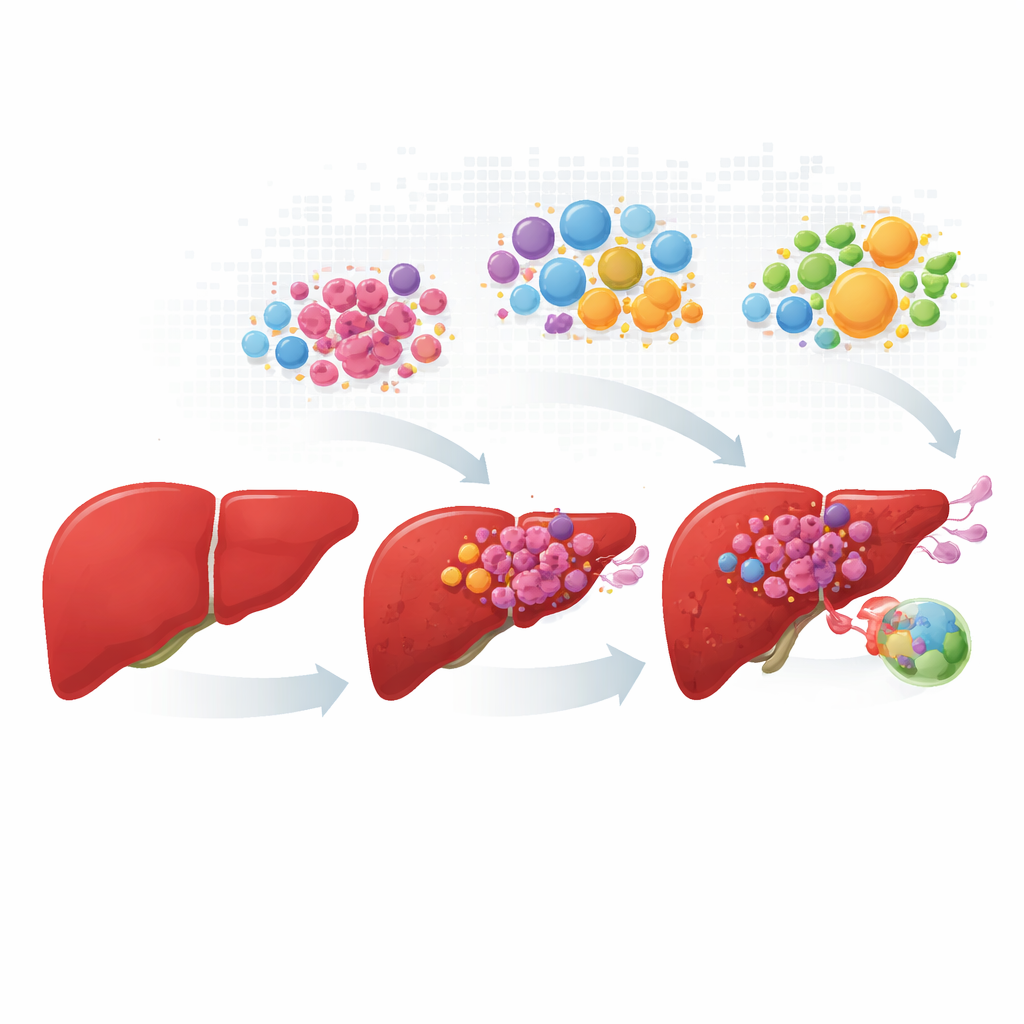
Seguire le cellule tumorali dall’inizio alla diffusione
I ricercatori hanno raccolto e armonizzato dati provenienti da oltre cento pazienti, includendo fegato normale, tumori primari, lesioni nei vasi sanguigni e metastasi linfonodali. Invece di trattare ogni tumore come una massa uniforme, hanno profilato centinaia di migliaia di singole cellule e poi mappato la loro posizione nei campioni tissutali. Le cellule epatiche cancerose si raggruppavano in quattro “personalità” ricorrenti. Un gruppo manteneva molte funzioni epatiche normali e compiti metabolici; gli altri tre mostravano crescita indotta da stress, alta attività della via di crescita MYC o comportamento invasivo legato all’infiammazione. Questi quattro stati comparivano in proporzioni diverse con l’avanzare della malattia, con cellule a crescita rapida e invasive che predominavano nelle lesioni vascolari e linfonodali.
Quattro personalità tumorali con destini diversi
I quattro stati delle cellule tumorali non erano solo categorie teoriche; si associavano all’andamento clinico dei pazienti. I tumori ricchi dello stato simile al fegato, metabolicamente attivo, erano collegati a una sopravvivenza migliore, mentre i tumori dominati dagli altri tre stati aggressivi tendevano ad avere esiti peggiori. Tuttavia anche lo stato “buono” presentava una complicazione: risultava fortemente arricchito nei pazienti che non traevano beneficio dal farmaco per il fegato sorafenib, probabilmente perché queste cellule conservano meccanismi di detossificazione che possono inattivare i medicinali. Riproducendo i percorsi di sviluppo delle cellule, il gruppo ha mostrato che le cellule invasive e infiammatorie possono diramarsi verso stati più differenziati o verso stati altamente proliferativi, suggerendo che le cellule tumorali possono cambiare identità e sfuggire a terapie mirate a uno stato unico.
Il cast di supporto: complici immunitari e stromali
Le cellule tumorali non agiscono da sole. Lo studio ha rivelato cellule immunitarie specializzate e cellule di supporto che o combattono i tumori o li aiutano silenziosamente. Tra i macrofagi, i netturbini e sentinelle tissutali, alcuni tipi producevano segnali infiammatori che possono favorire l’immunità anti‑tumorale, mentre altri erano riadattati metabolicamente, sopprimevano segnali utili e promuovevano la formazione di vasi e l’invasione. Questi macrofagi “nocivi” si espandevano nei campioni avanzati. Allo stesso modo, specifici endoteli delle pareti vascolari e fibroblasti che costruiscono il tessuto connettivo formavano sottogruppi distinti legati a una prognosi sfavorevole. Nella malattia avanzata, un particolare sottotipo endoteliale e due tipi di fibroblasti creavano hub strettamente connessi che rimodellavano la matrice extracellulare, alimentavano la neoangiogenesi e si correlavano con gli stati cellulari tumorali più aggressivi.
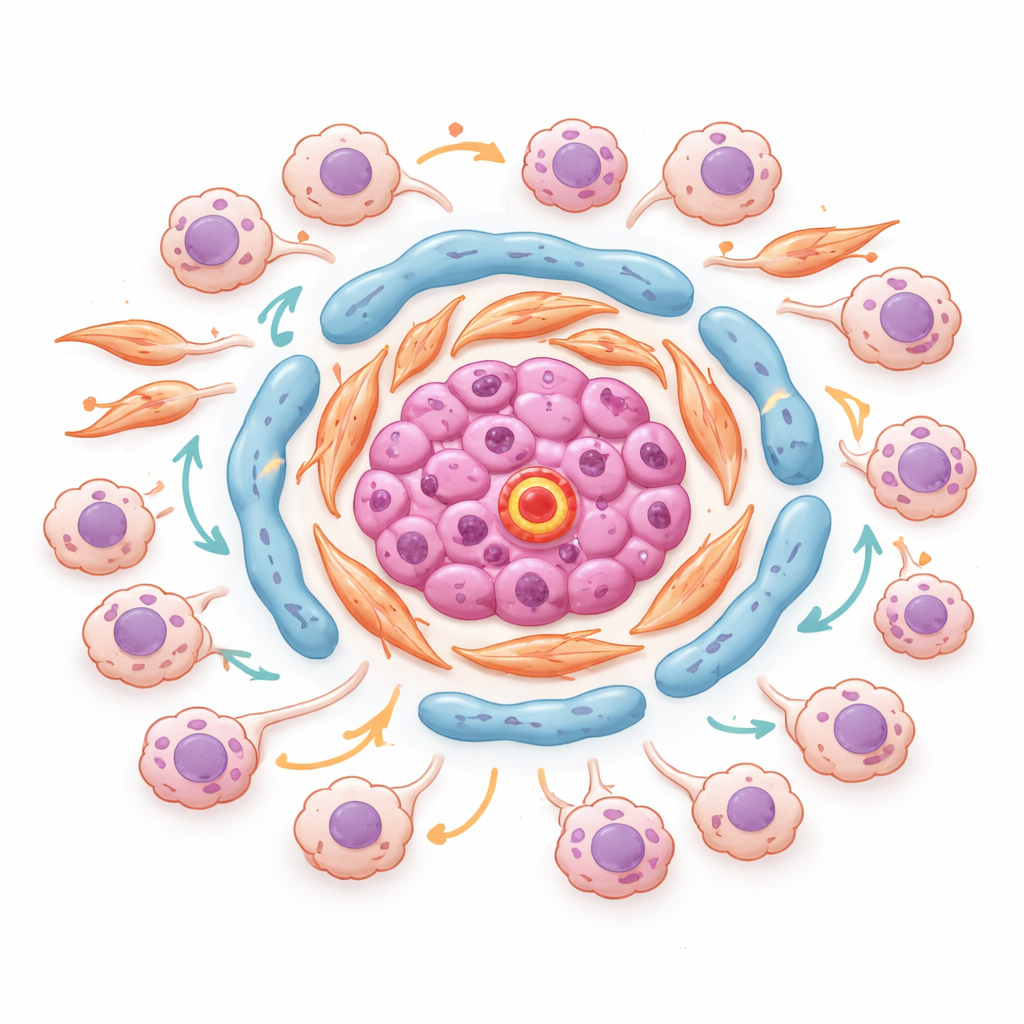
Individuare i quartieri pericolosi all’interno dei tumori
Utilizzando la trascrittomica spaziale, che misura l’attività genica senza perdere la mappa della posizione di ogni zona nel tessuto, gli autori hanno identificato “quartieri” organizzati all’interno dei tumori. In un tumore rappresentativo, cellule endoteliali ricche di una molecola chiamata ESM1 si raggruppavano con fibroblasti assetati di lipidi e produttori di matrice al centro di isole stromali. Attorno a questi nuclei si accumulavano cellule tumorali guidate dallo stress e invasive, in regioni con forti segnali TGF‑beta e bassi livelli di ossigeno. Fattori di trascrizione chiave che controllano la risposta delle cellule a stress e infiammazione erano condivisi tra questi stati tumorali e risultavano più attivi proprio dove le cellule tumorali toccavano questi hub stromali. Ciò suggerisce che micro‑nicchie specifiche ai bordi tumore‑stroma favoriscono attivamente il cambiamento di stato delle cellule tumorali, rendendole più aggressive e resistenti alle terapie.
Trovare un punto debole comune per nuovi trattamenti
Per passare dalla descrizione all’intervento, il gruppo ha usato un modello di apprendimento automatico addestrato su milioni di cellule per simulare “knockout virtuali” di geni e prevedere quali modifiche potessero spingere le cellule dannose verso stati più sani. Confrontando macrofagi, cellule endoteliali e cellule tumorali, hanno individuato un piccolo insieme di geni la cui rimozione aiutava a normalizzare tutti e tre i tipi. Tra questi, HSP90B1 è emerso come punto chiave: le linee cellulari tumorali dipendono fortemente da questo gene, è sovraespresso nei tumori epatici — in particolare in quelli resistenti ai farmaci mirati e all’immunoterapia — e livelli elevati predicono una sopravvivenza peggiore. HSP90B1 codifica una chaperone coinvolta nella gestione dello stress nella fabbrica di ripiegamento delle proteine della cellula che supporta numerosi recettori di superficie e vie di segnalazione. Poiché esistono già farmaci selettivi contro questa chaperone che possono anche rimodellare l’ambiente immunitario, lo studio propone HSP90B1 come un bersaglio promettente per superare la resistenza, soprattutto se combinato con i trattamenti attuali per il cancro del fegato.
Cosa significa per i pazienti e le terapie
Nel complesso, questo lavoro mostra che il cancro del fegato non è una sola malattia, ma un ecosistema dinamico di stati cellulari e nicchie che mutano mentre il tumore cresce e si diffonde. Collegando specifiche personalità delle cellule tumorali, cellule di supporto e quartieri spaziali all’esito del paziente e alla risposta ai farmaci, lo studio offre una mappa per terapie più precise: abbinare i trattamenti agli stati cellulari dominanti, interrompere gli hub stromali che favoriscono comportamenti aggressivi e colpire dipendenze condivise come HSP90B1 di cui molte cellule tumorali e del microambiente dipendono. Pur richiedendo ulteriori test di laboratorio e studi clinici, l’atlas costruito dal team fornisce un progetto dettagliato per trasformare la complessità interna del tumore da ostacolo a opportunità per terapie del cancro del fegato più intelligenti e durature.
Citazione: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
Parole chiave: carcinoma epatocellulare, analisi a singola cellula, microambiente tumorale, trascrittomica spaziale, HSP90B1