Clear Sky Science · it
La perdita di microRNA-29b promuove la riduzione di STING mediata da DNMT3b attenuando l’immunità antitumorale indotta da radioterapia nel carcinoma colorettale con mutazione KRAS
Perché questa ricerca è importante
Per molte persone con tumore del retto e del colon, la radioterapia è una componente chiave del trattamento prima dell’intervento chirurgico. Tuttavia alcuni tumori si riducono appena e il cancro spesso recidiva o si diffonde. Questo studio esplora un comune cambiamento genetico nel carcinoma colorettale — la mutazione di KRAS — per spiegare perché questi tumori resistono spesso alla radioterapia e alle nuove immunoterapie, e propone una strategia per riattivare il sistema immunitario dell’organismo contro di essi.
Una mutazione comune che nasconde i tumori dall’attacco immunitario
Il carcinoma colorettale porta frequentemente mutazioni nel gene KRAS, un importante motore della crescita e della diffusione tumorale. I clinici avevano già osservato che i tumori con KRAS mutato tendono a rispondere male sia ai farmaci mirati sia alla radioterapia. Analizzando grandi banche dati oncologiche e campioni di pazienti, gli autori hanno scoperto che i tumori con KRAS mutato mostrano meno cellule CD8 in grado di uccidere il cancro e una minore attività dei segnali interferonici che potenziano l’immunità. Nei pazienti sottoposti a chemioradioterapia standard prima dell’intervento per il cancro del retto, quelli con KRAS normale hanno mostrato un aumento molto maggiore di cellule CD8 all’interno dei tumori dopo il trattamento rispetto a chi aveva KRAS mutato, contribuendo a spiegare i loro esiti migliori.
Il sistema d’allarme mancante all’interno delle cellule tumorali
La radioterapia non solo danneggia il DNA tumorale; può anche agire come un segnale d’allarme, inducendo le cellule tumorali a rilasciare frammenti di DNA che attivano una via di allerta interna chiamata cGAS–STING. Quando STING è attivo, le cellule producono interferoni di tipo I e altri segnali che richiamano e attivano le cellule immunitarie, comprese le cellule T e le cellule dendritiche. I ricercatori hanno mostrato che nelle cellule di carcinoma colorettale ingegnerizzate per esprimere KRAS mutato questo sistema d’allarme è attenuato: dopo la radiazione queste cellule producevano molto meno interferone e molecole correlate. Nei topi, il silenziamento di KRAS nei tumori ha ristabilito i livelli di STING, aumentato i segnali interferonici e portato a un maggiore reclutamento di cellule T CD4 e CD8, a meno cellule T regolatorie e a un controllo tumorale più efficace — non solo nei tumori irradiati ma anche in tumori distanti non irradiati, l’effetto cosiddetto “abscopal”.
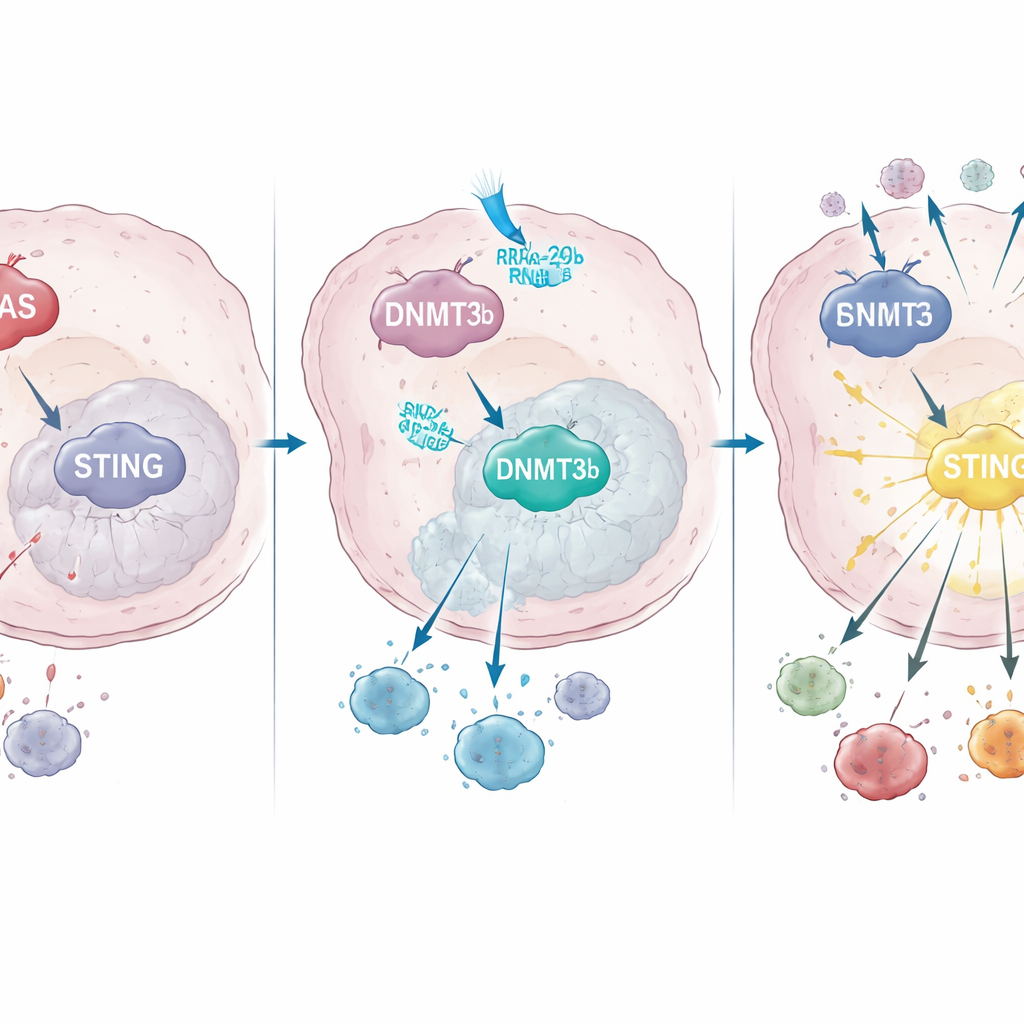
Come KRAS riorganizza il controllo genico per spegnere STING
Approfondendo, il gruppo ha scoperto che KRAS mutato aumenta l’attività di un enzima che modifica il DNA chiamato DNMT3b, che aggiunge gruppi metile a determinate regioni di DNA e spegne i geni vicini. Sia nelle linee cellulari tumorali sia nei campioni di pazienti, alti livelli di DNMT3b correla-vano con bassi livelli di STING. Una porzione chiave del promotore di STING — la regione “interruttore” del DNA — era fortemente metilata nei tumori con KRAS mutato, ma non in quelli con KRAS normale. I pazienti i cui tumori riuscivano ancora ad aumentare STING dopo la chemioradioterapia presentavano maggiore infiltrazione di cellule T CD8 e sopravvivenza migliore, sottolineando quanto sia cruciale questa via per il successo del trattamento.
Un piccolo RNA che può riattivare l’allarme
Gli autori si sono quindi chiesti cosa determinasse l’abbondanza di DNMT3b nel cancro KRAS‑mutato. Con il sequenziamento dei microRNA hanno identificato un piccolo RNA regolatorio, microRNA‑29b‑3p, che normalmente tiene sotto controllo DNMT3b ma è fortemente soppresso da KRAS mutato. Ripristinare questo microRNA in cellule KRAS‑mutate coltivate in laboratorio ha ridotto DNMT3b, riattivato STING e aumentato la produzione di interferone dopo la radiazione; bloccarlo aveva l’effetto opposto. Nei campioni tumorali, i pazienti con KRAS mutato tendevano ad avere bassi livelli di microRNA‑29b‑3p, alti livelli di DNMT3b e bassi livelli di STING, e coloro con livelli più elevati di microRNA‑29b‑3p vivevano più a lungo, collegando questa catena molecolare direttamente agli esiti clinici.
Un approccio mirato di consegna genica che potenzia radioterapia e immunoterapia
Per tradurre queste scoperte in una possibile terapia, il team ha ingegnerizzato un virus innocuo (AAV) che veicola microRNA‑29b‑3p sotto il controllo di un promotore attivo principalmente nelle cellule del carcinoma colorettale. In modelli murini portatori di tumori colorettali KRAS‑mutati, la somministrazione di questo AAV insieme a radioterapia localizzata ha ridotto drasticamente sia i tumori irradiati sia i tumori distanti non trattati con radiazioni. I tumori presentavano meno DNMT3b, più STING, segnali interferonici aumentati e massiccia infiltrazione di cellule T e altre cellule immunitarie. Quando lo stesso trattamento con microRNA‑29b‑3p è stato combinato con un inibitore del checkpoint immunitario diretto contro PD‑1, la sopravvivenza è migliorata ulteriormente, e questo beneficio dipendeva dalle cellule T CD8, confermando che è il sistema immunitario a svolgere il ruolo principale.
Cosa potrebbe significare per i pazienti
In termini semplici, questo studio rivela come i carcinomi colorettali con KRAS mutato “taglino il filo” di un sistema d’allarme interno che la radioterapia normalmente attiva, permettendo loro di eludere l’attacco immunitario. Ripristinando un singolo piccolo RNA, microRNA‑29b‑3p, i ricercatori sono riusciti a ridurre DNMT3b, riattivare STING e trasformare tumori immunologicamente “freddi” in tumori “caldi” che rispondono meglio sia alla radioterapia sia al blocco dei checkpoint. Sebbene questo lavoro sia ancora a livello preclinico, indica direzioni per futuri trattamenti che accoppino la radioterapia a terapie geniche mirate al tumore per superare la resistenza nei carcinomi colorettali KRAS‑mutati, potenzialmente rendendo efficaci le terapie esistenti per molti più pazienti.
Citazione: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
Parole chiave: carcinoma colorettale con mutazione KRAS, resistenza alla radioterapia, via STING, microRNA-29b, immunologia tumorale