Clear Sky Science · it
Analisi comparativa delle strategie di monitoraggio del ctDNA in NSCLC avanzato con salti dell’esone 14 di MET trattati con ensartinib
Perché un esame del sangue conta nel cancro polmonare
Per le persone con cancro polmonare avanzato, una delle questioni principali è capire se un nuovo farmaco sta effettivamente funzionando — e quanto presto i medici possono saperlo. Questo studio esplora un approccio basato sul sangue, utilizzando minuscoli frammenti di DNA tumorale che circolano nel flusso sanguigno, per valutare rapidamente quanto un farmaco mirato chiamato ensartinib stia aiutando pazienti i cui tumori presentano un particolare difetto genetico. I risultati suggeriscono che un semplice esame del sangue precoce potrebbe segnalare quali pazienti probabilmente trarranno beneficio più a lungo dal trattamento e quali potrebbero aver bisogno di cambiare strategia.
Mettere le impronte digitali di un tumore in una provetta
Le cellule tumorali rilasciano frammenti del loro materiale genetico nel sangue, noti come DNA tumorale circolante. In questo trial, i ricercatori si sono concentrati su persone con carcinoma polmonare non a piccole cellule guidato da una alterazione del gene MET, nello specifico un difetto noto come salto dell’esone 14. Tutti i pazienti hanno ricevuto ensartinib dopo il fallimento di terapie precedenti. I campioni di sangue sono stati prelevati subito prima di iniziare il farmaco e di nuovo quattro settimane dopo. Usando un test di sequenziamento avanzato che analizza 229 geni correlati al cancro, il gruppo ha raggruppato le variazioni rilevate in tre categorie: alterazioni nel MET stesso, un set di noti oncogeni, e un gruppo ampio e generico di qualsiasi mutazione rilevabile.
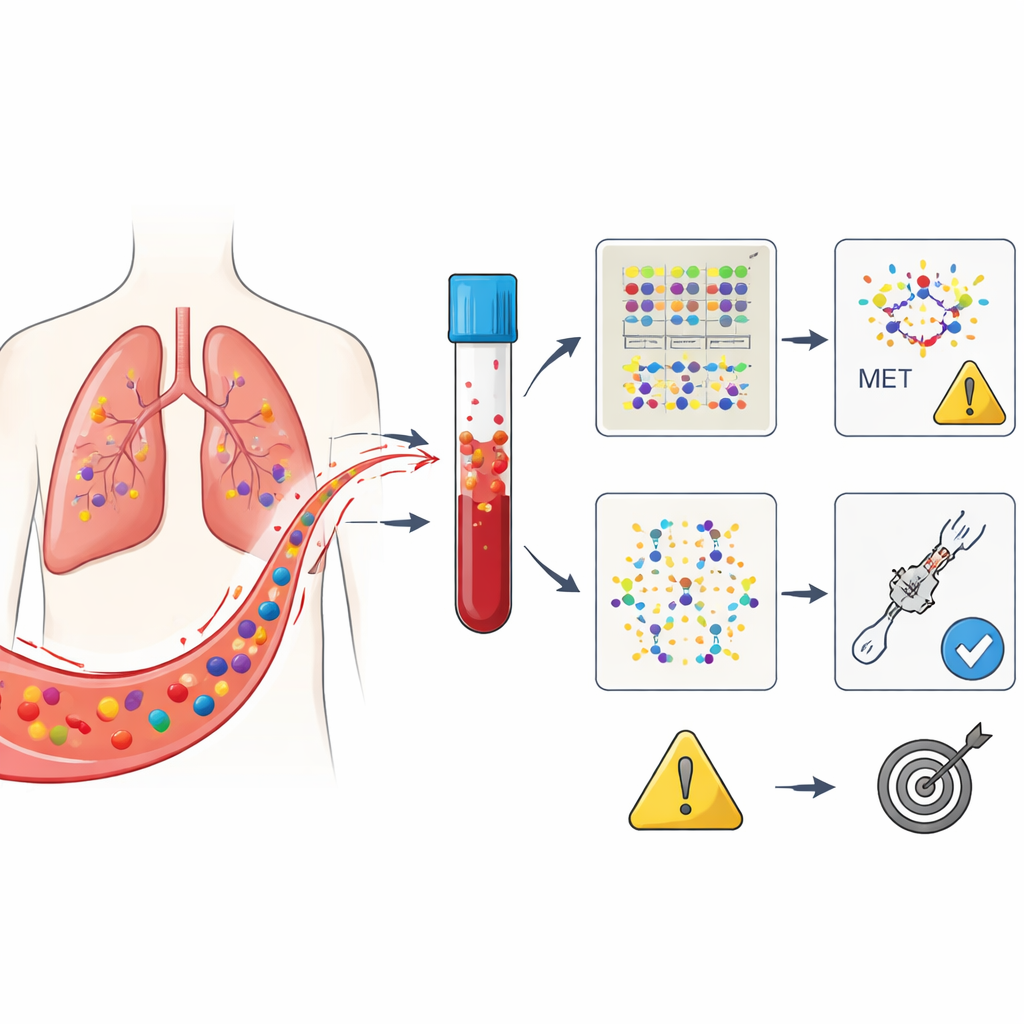
Tre modi di leggere lo stesso segnale nel sangue
La domanda centrale era quale di queste tre «visioni» del sangue predicesse meglio chi avrebbe risposto all’ensartinib e per quanto tempo questa risposta sarebbe durata. All’inizio, non tutti i pazienti avevano DNA tumorale rilevabile nel sangue, nonostante i loro tumori presentassero il difetto su MET; questo riflette quanto in modo non uniforme i tumori rilascino DNA. Nelle prime analisi, essere semplicemente positivi o negativi per DNA tumorale al basale non ha avuto un forte valore predittivo. Tuttavia, al momento della valutazione a quattro settimane è emerso un quadro chiaro: i pazienti il cui sangue non mostrava più alterazioni correlate a MET tendevano a restare senza progressione di malattia molto più a lungo rispetto a coloro in cui questi segnali persistevano. Ciò era vero anche se le scansioni tumorali in quel momento potevano risultare ancora ambigue.
Quando i segnali MET svaniscono, gli esiti migliorano
Analizzando più nel dettaglio come i risultati del sangue cambiavano nel tempo, il team ha identificato tre percorsi. Alcuni pazienti non hanno mai avuto DNA MET rilevabile nel sangue, alcuni sono passati da positivo a negativo, e altri sono rimasti positivi o hanno sviluppato nuove alterazioni di MET. Coloro che hanno eliminato i segnali MET entro la quarta settimana hanno goduto del periodo più lungo prima della progressione della malattia, circa nove mesi in media, e hanno mostrato il tasso più alto di riduzione misurabile del tumore. I pazienti che sono rimasti positivi per il DNA MET hanno avuto esiti molto peggiori, con progressione della malattia in poco più di due mesi in media. Il monitoraggio di insiemi più ampi di mutazioni ha fornito anch’esso informazioni utili, ma si è rivelato meno preciso perché molte alterazioni a basso livello o non correlate potevano offuscare il quadro.
Bilanciare semplicità e approfondimento
Usare solo il DNA correlato a MET come guida ha offerto lo scatto più netto e semplice per capire se l’ensartinib stava aiutando. Questo approccio mirato ha mostrato alta specificità, il che significa che quando i segnali MET scomparivano c’era una forte probabilità che il paziente andasse bene. Ciò lo rende attraente come strumento pratico: i test su singoli geni sono più economici, più rapidi e più facili da interpretare rispetto a pannelli di grandi dimensioni. Allo stesso tempo, l’analisi di un numero maggiore di geni ha mantenuto il suo valore, perché può scoprire nuove mutazioni che potrebbero spiegare perché un tumore ha poi smesso di rispondere e indicare opzioni terapeutiche future. Lo studio suggerisce che combinare una visione ristretta, centrata su MET, per decisioni terapeutiche precoci con una visione più ampia per monitorare le resistenze potrebbe offrire il meglio di entrambi gli approcci.
Cosa significa per i pazienti
Per un lettore non specialistico, il messaggio chiave è che un esame del sangue effettuato già un mese dopo l’inizio dell’ensartinib può dare indicazioni sull’efficacia a lungo termine del farmaco. Se il DNA tumorale correlato a MET scompare dal circolo ematico, le probabilità di un beneficio significativo e duraturo sono alte; se persiste, i medici potrebbero dover sorvegliare più da vicino o considerare altre opzioni. Pur trattandosi di uno studio relativamente piccolo e a braccio singolo che richiede conferma in cohorti più ampie, ciò rafforza l’idea che le «biopsie liquide» possano fungere da valutazione precoce delle terapie mirate. In futuro, questo tipo di monitoraggio potrebbe contribuire a personalizzare le cure, evitando ai pazienti di proseguire trattamenti inefficaci e indirizzandoli più rapidamente verso terapie efficaci.
Citazione: Zhou, M., Zhu, Y., Sun, X. et al. Comparative analysis of ctDNA monitoring strategies in advanced NSCLC with MET exon 14 skipping mutations treated with ensartinib. npj Precis. Onc. 10, 110 (2026). https://doi.org/10.1038/s41698-026-01284-6
Parole chiave: DNA tumorale circolante, salto dell’esone 14 di MET, ensartinib, carcinoma polmonare non a piccole cellule, monitoraggio con biopsia liquida