Clear Sky Science · it
L’apprendimento profondo multi-omico migliora la prognosi a lungo termine del tumore al seno basata su FDG PET-CT
Perché è importante per pazienti e famiglie
Quando a una persona viene diagnosticato un tumore al seno, una delle prime domande è: «Cosa significa questo per il mio futuro?» Gli attuali sistemi di stadiazione e gli esami di laboratorio forniscono solo stime approssimative. Questo studio esplora se combinare le immagini mediche, i referti dei medici e le informazioni cliniche di base con l’intelligenza artificiale avanzata possa offrire una prospettiva più chiara e personalizzata sulla sopravvivenza a lungo termine e sul rischio di recidiva.
Guardare l’uso di carburante del corpo
Uno strumento chiave in questa ricerca è una scansione chiamata FDG PET-CT. Mostra non solo la morfologia dei tessuti, come una CT convenzionale, ma anche quanto zucchero consumano, rivelando quanto è attivo un tumore. I medici sanno già che alcuni indicatori ricavati da queste scansioni — per esempio quanto «luminoso» appare il tumore o quanto è grande — sono collegati agli esiti. Tuttavia, queste misure tradizionali catturano solo una piccola porzione delle ricche informazioni contenute nelle immagini e spesso dipendono dall’impegno manuale di specialisti che contornano i tumori a mano.
Insegnare ai computer a leggere immagini e referti
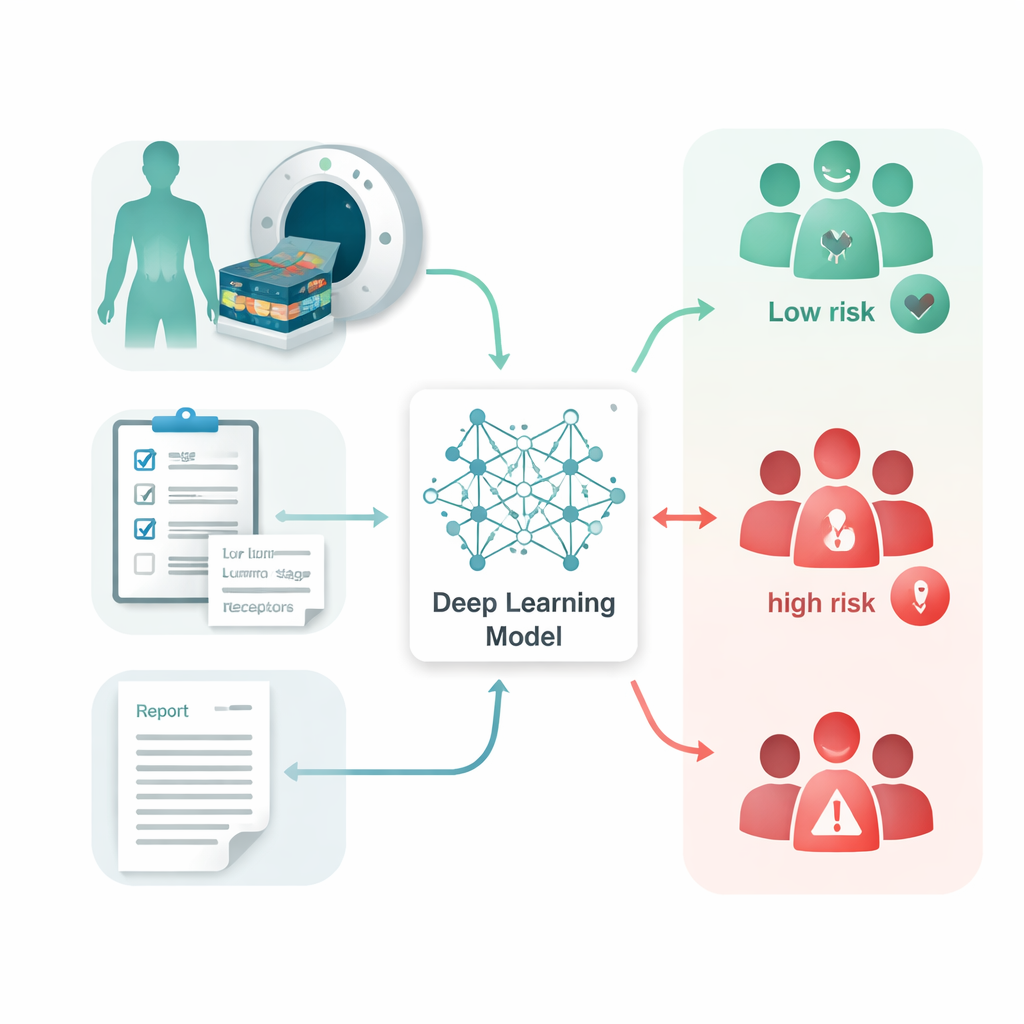
I ricercatori hanno raccolto scansioni FDG PET-CT, i corrispondenti referti di radiologia e i dati clinici di routine di 1.210 donne con tumore al seno trattate in un centro oncologico olandese nell’arco di 15 anni. Nessuna presentava metastasi a distanza visibili al momento della diagnosi. Hanno costruito un sistema chiamato Multi-Omics Prognostic Stratification (MOPS), che usa l’apprendimento profondo — un tipo di intelligenza artificiale che apprende pattern da grandi insiemi di dati — per combinare tre tipi di informazioni: le immagini, i referti testuali che descrivono ciò che i radiologi hanno osservato e i fattori clinici come età, dimensione del tumore, stato dei linfonodi e sottotipi ormonali. Un programma automatizzato ha prima delineato i tumori della mammella e i linfonodi coinvolti in modo che il modello potesse concentrarsi sulle regioni più rilevanti senza tracciature manuali.
Ottenere di più combinando molti indizi
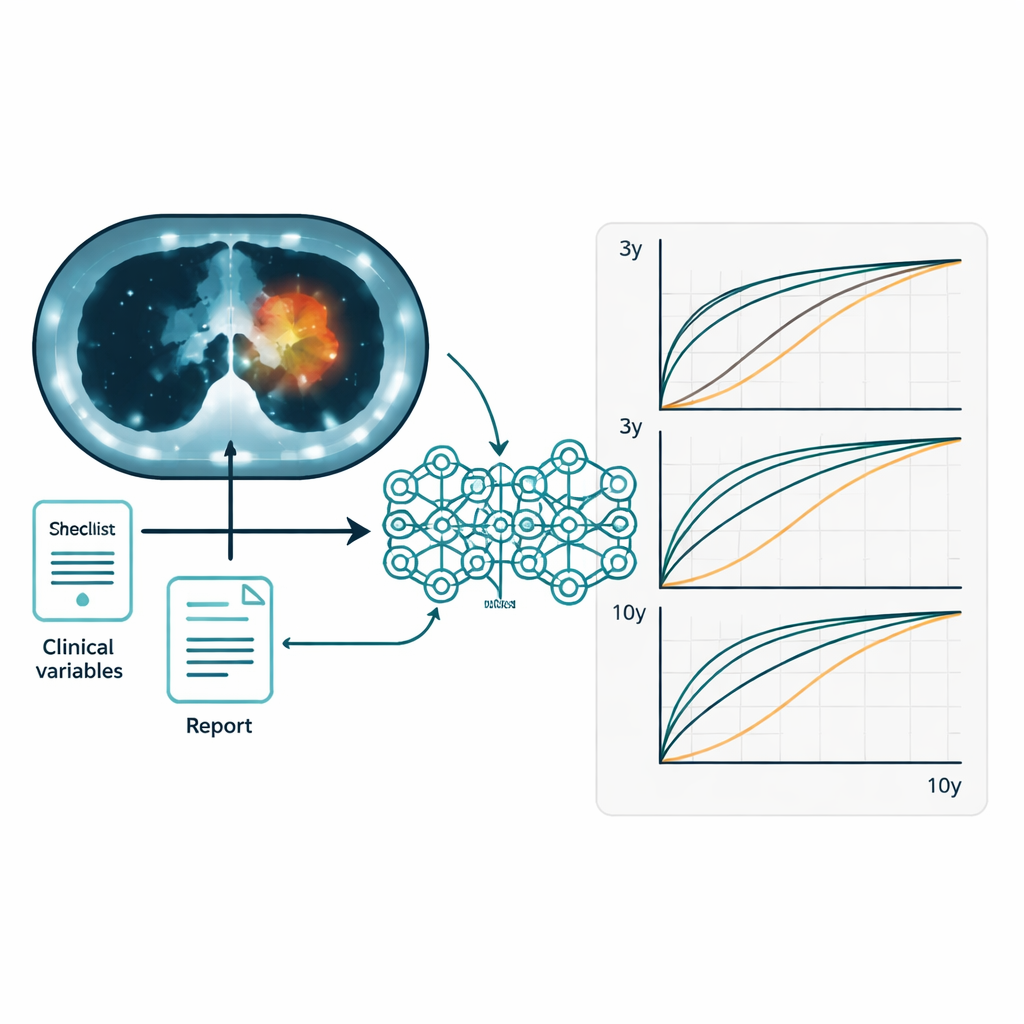
Il gruppo ha prima verificato quanto bene i numeri abituali basati sulle scansioni predicessero chi avrebbe vissuto più a lungo e chi avrebbe avuto una recidiva. Le misure che riflettono il carico tumorale complessivo, come il volume tumorale metabolico e la glicolisi totale della lesione, hanno reso meglio rispetto a un semplice indice di picco di intensità, ma la loro accuratezza è rimasta modesta. Un modello di apprendimento profondo che ha analizzato l’intero torace su PET-CT ha migliorato questi parametri tradizionali. Successivamente i ricercatori hanno testato separatamente tre «flussi» di dati: le immagini, i referti testuali e le informazioni cliniche. Tra questi, i dati clinici da soli hanno fornito la singola fonte prognostica più solida. Tuttavia, quando tutti e tre sono stati fusi insieme nel sistema MOPS, le prestazioni sono ulteriormente migliorate, offrendo previsioni più affidabili sia per la sopravvivenza globale sia per la sopravvivenza libera da malattia a 3, 5 e 10 anni.
Aprire la scatola nera
Poiché i medici devono poter fidarsi e spiegare qualsiasi strumento che influenzi le decisioni terapeutiche, il gruppo ha progettato MOPS con l’interpretabilità in primo piano. Mappe di calore sovrapposte alle sezioni CT hanno mostrato che il modello si concentrava sui tumori primari della mammella e sui linfonodi coinvolti, piuttosto che su parti irrilevanti dell’immagine. Per i dati clinici, il modello ha evidenziato fattori ad alto impatto già familiari, come la dimensione del tumore (stadio T), lo stato dei linfonodi e la storia familiare. Nei referti testuali tendeva a enfatizzare parole che descrivevano i linfonodi, la localizzazione del tumore e l’attività metabolica, rispecchiando il ragionamento dei radiologi. Attraverso diversi stadi tumorali e sottotipi biologici, il modello è stato in grado di suddividere i pazienti in gruppi a rischio più elevato e più basso, sebbene la distinzione fosse naturalmente meno marcata per tumori molto piccoli e in stadio precoce che già presentano eccellenti tassi di sopravvivenza.
Cosa potrebbe significare per la cura
In termini pratici, questo lavoro suggerisce che combinare in modo ponderato immagini, referti medici e informazioni cliniche standard può affinare le stime sulla prognosi a lungo termine di una paziente con tumore al seno oltre quanto può offrire una singola fonte. Se validato in altri ospedali e con diversi tipi di scanner, uno strumento come MOPS potrebbe aiutare i medici a identificare le pazienti che richiedono davvero un follow-up più stretto o terapie più intensive, risparmiando nel contempo alle pazienti a basso rischio trattamenti e ansia non necessari. Piuttosto che sostituire i clinici, il sistema agisce come un secondo paio di occhi, distillando dati complessi in un punteggio di rischio individualizzato che supporta conversazioni più chiare sulla prognosi e i passi successivi.
Citazione: Liang, X., Zhang, T., Braga, M. et al. Multi-omics deep learning improves FDG PET-CT-based long-term prognostication of breast cancer. npj Precis. Onc. 10, 74 (2026). https://doi.org/10.1038/s41698-026-01283-7
Parole chiave: prognosi del cancro al seno, imaging PET-CT, apprendimento profondo, multi-omica, predizione della sopravvivenza