Clear Sky Science · it
Sovraespressione della subunità NDUFS4 del complesso I mitocondriale guida la progressione del glioma regolando la funzione mitocondriale e COX5B
Perché i tumori cerebrali ad alto consumo energetico sono importanti
I gliomi sono tra i tumori cerebrali più aggressivi, spesso recidivanti nonostante interventi chirurgici, radioterapia e chemioterapia. Questo studio guarda dentro le cellule dei gliomi per porsi una domanda semplice ma di grande impatto: questi tumori dipendono da una specifica parte delle loro "centrali elettriche" interne per crescere e diffondersi? Tracciando una piccola proteina mitocondriale chiamata NDUFS4, i ricercatori scoprono un punto debole metabolico che sembra alimentare la progressione tumorale lasciando le cellule cerebrali sane molto meno colpite.
Un interruttore nascosto nelle centrali dei tumori cerebrali
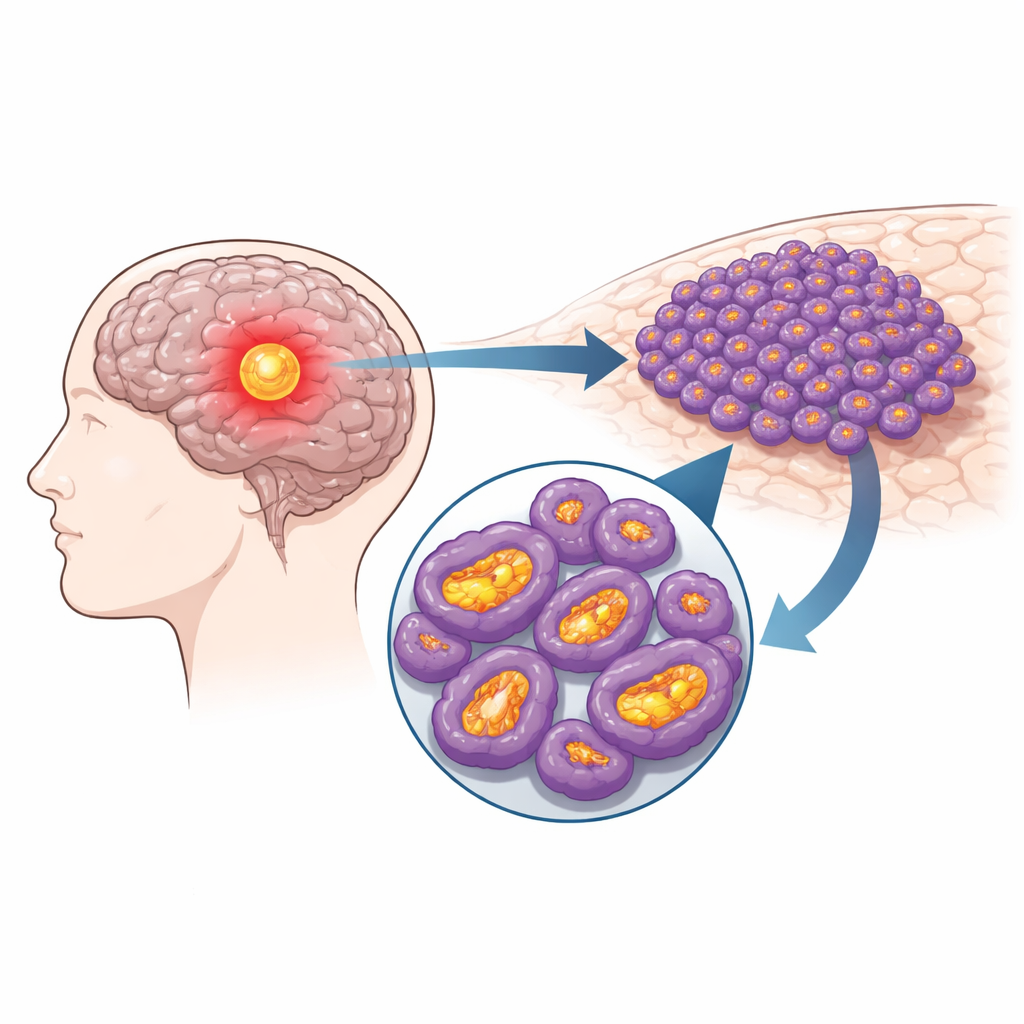
All’interno di ogni cellula, i mitocondri agiscono come piccoli generatori, trasformando i nutrienti in energia utilizzabile. Nelle cellule dei gliomi questi generatori sono portati a un livello superiore. Il gruppo ha analizzato grandi database oncologici pubblici e dati di sequenziamento a cellula singola e ha constatato che la proteina NDUFS4, componente di uno dei principali complessi produttori di energia nei mitocondri, è costantemente aumentata nei tessuti di glioma rispetto al cervello normale. Livelli più elevati di NDUFS4 si associano a un grado tumorale più avanzato e a pazienti con sopravvivenza più breve. L’analisi a risoluzione di singola cellula ha mostrato che questo eccesso di NDUFS4 è concentrato specificamente nelle cellule tumorali piuttosto che nelle cellule non cancerose circostanti del cervello.
Abbassare il livello energetico per rallentare il cancro
Per verificare se NDUFS4 fosse solo un marcatore o un vero e proprio motore della malattia, i ricercatori lo hanno ridotto o eliminato deliberatamente in cellule di glioma derivate da pazienti e coltivate in laboratorio. Quando NDUFS4 è stato silenziato o annullato, i mitocondri delle cellule hanno ceduto: l’uso di ossigeno è diminuito, un passaggio chiave della produzione di energia si è rallentato e la quantità di carburante cellulare (ATP) è calata. Contemporaneamente, sono aumentati sottoprodotti dannosi noti come specie reattive dell’ossigeno e le membrane interne cellulari hanno mostrato segni di stress e ossidazione. A livello funzionale, queste cellule tumorali affamate di energia si sono divise di meno, hanno formato meno colonie, si sono mosse e invase con minore efficacia e hanno mostrato più segnali di morte cellulare programmata. In modo sorprendente, lo stesso intervento genetico in astrociti non cancerosi — cellule di supporto del tessuto cerebrale normale — ha causato pochi o nessun danno, suggerendo che le cellule tumorali dipendono in modo particolare da questo interruttore mitocondriale.
Aumentare la potenza rende i tumori più aggressivi
La faccia opposta dell’esperimento ha fornito un quadro altrettanto chiaro. Quando gli scienziati hanno forzato le cellule di glioma a produrre NDUFS4 in eccesso, i loro mitocondri sono diventati più attivi: la produzione di energia è aumentata e il complesso respiratorio chiave ha lavorato di più. Queste cellule potenziate crescevano più velocemente, migravano più facilmente e invadevano barriere in modo più aggressivo, sia nelle cellule primarie dei pazienti sia nelle linee cellulari di laboratorio standard. Nei topi, le cellule di glioma ingegnerizzate per mantenere livelli elevati di NDUFS4 hanno formato tumori intracranici più grandi, mentre le cellule con NDUFS4 ridotto crescevano molto più lentamente nel cervello, mostravano performance mitocondriali più deboli, maggior danno ossidativo, meno cellule in divisione e più cellule morenti. Nel complesso, questi esperimenti stabiliscono NDUFS4 non come un semplice passeggero ma come un promotore della progressione del glioma.
Una proteina partner collega il controllo energetico al comportamento tumorale
Approfondendo, il team ha cercato di capire come NDUFS4 eserciti effetti così ampi. Mettendo a confronto dati di espressione genica da tumori bulk, cellule singole e mappe proteiche di cellule tumorali, hanno individuato un’altra proteina mitocondriale, COX5B, come partner chiave. COX5B contribuisce a gestire l’ultimo passaggio della principale catena energetica cellulare. Era strettamente correlata ai livelli di NDUFS4 nei gliomi ed è già nota per essere elevata in altri tumori. Quando i ricercatori hanno ridotto COX5B nelle cellule di glioma, hanno osservato lo stesso schema visto con la perdita di NDUFS4: performance mitocondriali indebolite, maggiore stress ossidativo, crescita e movimento rallentati e maggiore morte cellulare. Crucialmente, quando hanno ripristinato COX5B nelle cellule depauperate di NDUFS4, gran parte del danno mitocondriale e dell’effetto anti-tumorale si è invertito. Hanno inoltre scoperto che NDUFS4 influenza quanto fortemente un fattore di trascrizione (Sp1) si lega alla regione di controllo del gene COX5B, modulando la quantità di COX5B che la cellula produce.
Cosa significa questo per i futuri trattamenti del cancro cerebrale
Per un non specialista, il messaggio centrale è che molti gliomi sembrano dipendere da un sistema energetico potenziato incentrato su NDUFS4 e sul suo partner a valle COX5B. Spegnere questo sistema priva le cellule tumorali del carburante e dell’equilibrio necessari per crescere e invadere, pur risparmiando in misura comparativa le normali cellule di supporto cerebrale. Poiché questa vulnerabilità è consistente nei campioni dei pazienti, nelle cellule isolate e nei tumori cerebrali nei topi, NDUFS4 — e il suo controllo su COX5B — emerge come un bersaglio promettente per nuovi farmaci. Terapie che interrompano selettivamente questo “circuito di potenza” mitocondriale potrebbero integrare i trattamenti esistenti, rallentando la crescita tumorale e prolungando la sopravvivenza senza danneggiare gravemente il tessuto cerebrale sano.
Citazione: Wu, J., Li, J., Xu, L. et al. Mitochondrial complex I subunit NDUFS4 overexpression drives glioma progression by regulating mitochondrial function and COX5B. npj Precis. Onc. 10, 99 (2026). https://doi.org/10.1038/s41698-026-01281-9
Parole chiave: glioma, mitocondri, NDUFS4, COX5B, metabolismo del cancro cerebrale