Clear Sky Science · it
Un modello di deep learning interpretabile per predire i sottotipi molecolari del cancro endometriale da vetrini colorati in H&E
Perché è importante per la salute delle donne
Il cancro dell’endometrio, che origina nel rivestimento dell’utero, è uno dei tumori più comuni nelle donne, e il tasso di mortalità sta aumentando a livello globale. Oggi sappiamo che questo tumore esiste in diverse “varianti” molecolari che rispondono in modo differente a chirurgia, radioterapia, chemioterapia e alle più recenti terapie immunitarie. Attualmente, identificare questi sottotipi molecolari richiede spesso test genetici costosi e dispendiosi in termini di tempo che molti ospedali non sono in grado di offrire facilmente. Questo studio valuta se un sistema di intelligenza artificiale (IA) progettato con cura possa leggere i normali vetrini di patologia — le immagini tinto‑rosa e viola dei tessuti già preparate per ogni paziente — e inferire con precisione questi sottotipi molecolari, rendendo potenzialmente più accessibile la medicina di precisione.
Uno sguardo più ravvicinato alla diversità tumorale
Non tutti i carcinomi endometriali si comportano allo stesso modo. Alcuni crescono lentamente e restano confinati nell’utero; altri si diffondono precocemente e sono più difficili da trattare. Le linee guida moderne suddividono questi tumori in quattro sottotipi molecolari basati su alterazioni del DNA e sul modo in cui le cellule riparano il danno genetico. Queste categorie aiutano a prevedere l’esito e a guidare decisioni come l’estensione dell’intervento chirurgico e se una paziente possa beneficiare dell’immunoterapia. Tuttavia, i test genetici e le colorazioni speciali richieste sono costosi, dipendono dall’interpretazione esperta e spesso non sono disponibili in ospedali più piccoli o con risorse limitate. I patologi hanno da tempo il sospetto che molte di queste differenze molecolari lascino tracce visive nell’aspetto delle cellule e del tessuto di supporto al microscopio — ma questi indizi possono essere troppo sottili e complessi perché l’occhio umano li giudichi in modo costante.
Insegnare ai computer a leggere i vetrini di patologia
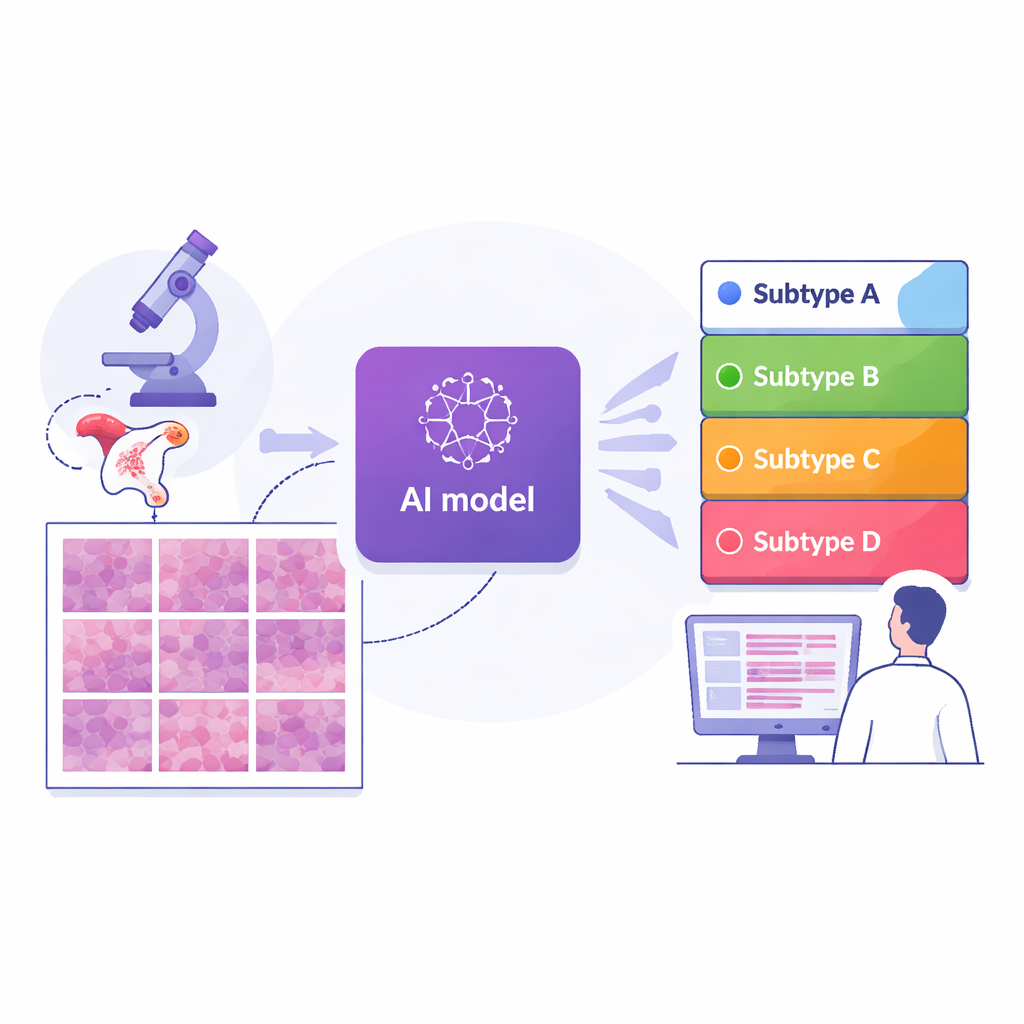
I ricercatori hanno raccolto immagini digitali di 364 vetrini da 324 donne trattate in un importante centro oncologico di Shanghai, insieme a due gruppi di confronto indipendenti: 296 vetrini da un dataset pubblico internazionale e 36 da un altro ospedale a Suzhou. Ogni caso era già stato assegnato a uno dei quattro sottotipi molecolari mediante test genetici avanzati. Il team ha quindi suddiviso ogni immagine dell’intero vetrino in migliaia di piccole tessere e ha addestrato un modello di deep learning — un tipo di IA usata nel riconoscimento delle immagini — per analizzare ogni tessera e stimare la probabilità che appartenesse a ciascun sottotipo. Mediando le predizioni delle tessere su tutto il vetrino, il sistema produceva una singola previsione di sottotipo per ciascuna paziente, rispecchiando in modo vicino il modo in cui i medici considerano il tumore nel suo complesso.
Quanto bene ha funzionato il sistema
Nel gruppo principale di Shanghai, l’IA ha raggiunto un elevato livello di accuratezza: il suo punteggio complessivo per distinguere tra i quattro sottotipi (misurato con una statistica standard che va da 0,5 per il caso alla possibilità di 1,0 per una separazione perfetta) era circa 0,87. La performance è rimasta solida — intorno a 0,84 — quando testata sui due gruppi esterni provenienti da ospedali e scanner dei vetrini differenti, suggerendo che l’approccio è ragionevolmente robusto. Rispetto a diverse strategie IA di punta che usano schemi di attenzione o pooling più complessi, questo modello end‑to‑end, costruito su un moderno backbone per l’analisi delle immagini, ha generalmente ottenuto risultati migliori. È importante sottolineare che gli autori hanno progettato il sistema per essere interpretabile: hanno utilizzato strumenti di visualizzazione per evidenziare esattamente quali regioni di ogni tessera l’IA ha usato per le sue decisioni.
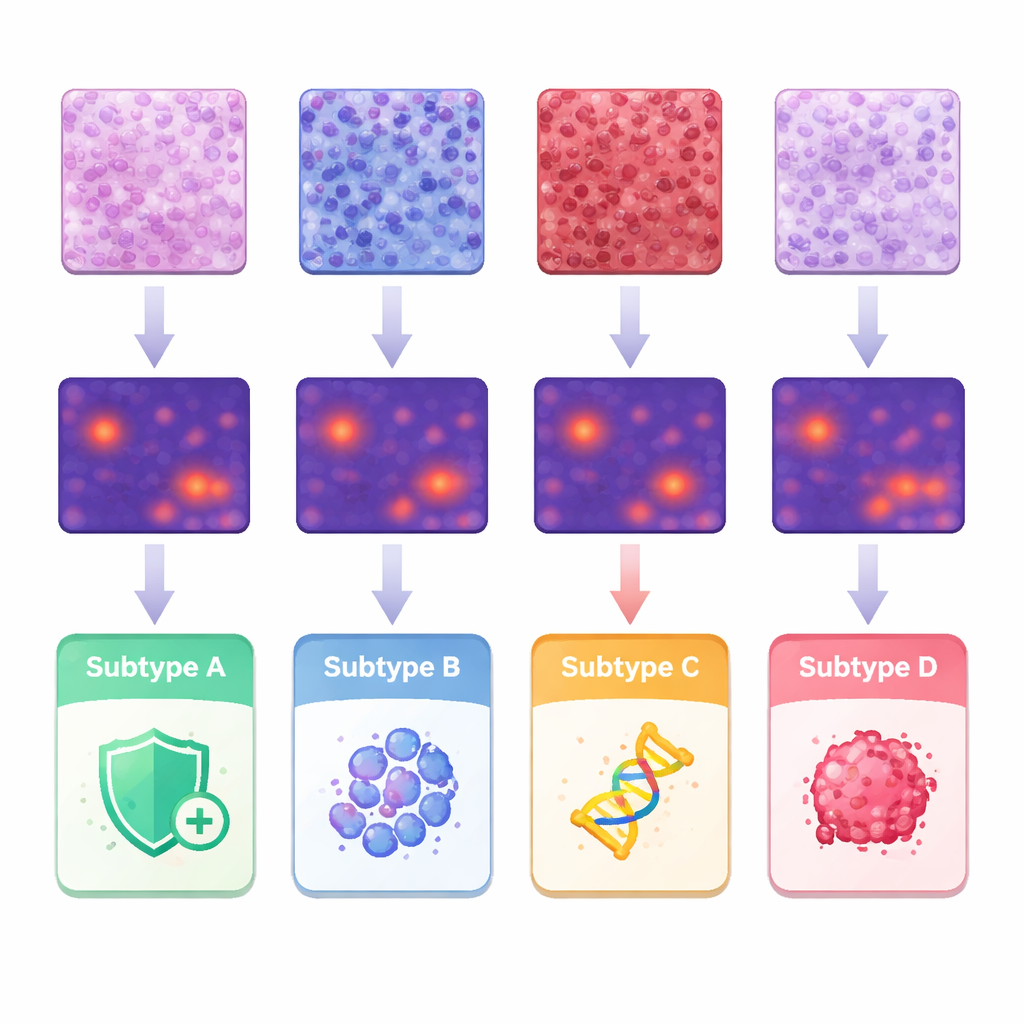
Cosa l’IA “ha visto” nel microambiente tumorale
Per comprendere quali caratteristiche guidassero le predizioni, il team ha collegato le heatmap dell’IA alle osservazioni classiche di patologia e a misurazioni dettagliate delle forme e degli arrangiamenti delle singole cellule. I tumori di un sottotipo mostravano una densa infiltrazione di cellule immunitarie nel tessuto di supporto, mentre un altro sottotipo tendeva ad avere cellule strutturali molto compatte. Un terzo gruppo presentava più lembi solidi di cellule tumorali altamente anomale, e il sottotipo associato a comportamento aggressivo mostrava strutture papillari a dita e nuclei molto irregolari. Segmentando e analizzando circa 245 milioni di cellule, i ricercatori hanno quantificato le differenze nelle dimensioni cellulari, nella variabilità e negli spazi tra le cellule, e hanno mostrato come certe combinazioni si allineassero con sottotipi specifici. Questi risultati supportano l’idea che le differenze molecolari lascino un’impronta riconoscibile sull’architettura tessutale che le macchine possono rilevare in modo sistematico.
Dal proof of concept all’aiuto clinico
Questo lavoro non si propone di sostituire i test genetici; piuttosto, propone uno strumento di triage “H&E‑first” che sfrutta la colorazione standard già preparata per ogni biopsia. In pratica, una mappa di probabilità di sottotipo generata dall’IA potrebbe aiutare i patologi a decidere quali test confermativi richiedere per primi, prioritizzare il tessuto limitato per gli esami più informativi e accelerare le decisioni terapeutiche, specialmente in ospedali dove il profilo molecolare completo è difficile da ottenere. Lo studio evidenzia anche i limiti attuali, come la performance più debole per il sottotipo più raro e la necessità di dataset più ampi e diversificati prima dell’implementazione clinica. Tuttavia, offre una dimostrazione convincente che le immagini microscopiche di routine contengono informazioni nascoste sufficienti affinché l’IA approssimi etichette molecolari complesse, aprendo la strada a un’assistenza più equa e basata sui dati per le donne con cancro endometriale.
Citazione: Guo, Q., Cui, H., Zhang, Y. et al. An interpretable deep learning model for predicting endometrial cancer molecular subtypes from H&E-stained slides. npj Precis. Onc. 10, 71 (2026). https://doi.org/10.1038/s41698-026-01280-w
Parole chiave: cancro dell’endometrio, patologia digitale, deep learning, sottotipi molecolari, oncologia di precisione