Clear Sky Science · it
Un atlante integrato del cancro polmonare a singola cellula rivela fenotipi fibroblastici distinti tra adenocarcinoma e carcinomi squamosi
Perché il vicinato attorno a un tumore conta
Il cancro polmonare non è formato solo da cellule tumorali. È più simile a una città affollata in cui le cellule tumorali convivono con vasi sanguigni, cellule immunitarie e cellule di supporto. Questo studio pone una domanda sorprendentemente semplice ma dalle grandi implicazioni: le due forme principali di carcinoma polmonare non a piccole cellule—adenocarcinoma e carcinoma squamoso—costruiscono “vicinati” diversi all'interno del polmone, e queste differenze potrebbero aiutare a spiegare perché i pazienti hanno esiti migliori o peggiori? Usando potenti strumenti per leggere il DNA a singola cellula, i ricercatori mappano centinaia di migliaia di singole cellule per rivelare come un gruppo chiave di cellule di supporto, chiamate fibroblasti, si comporti in modo molto diverso in questi due tipi di tumore.
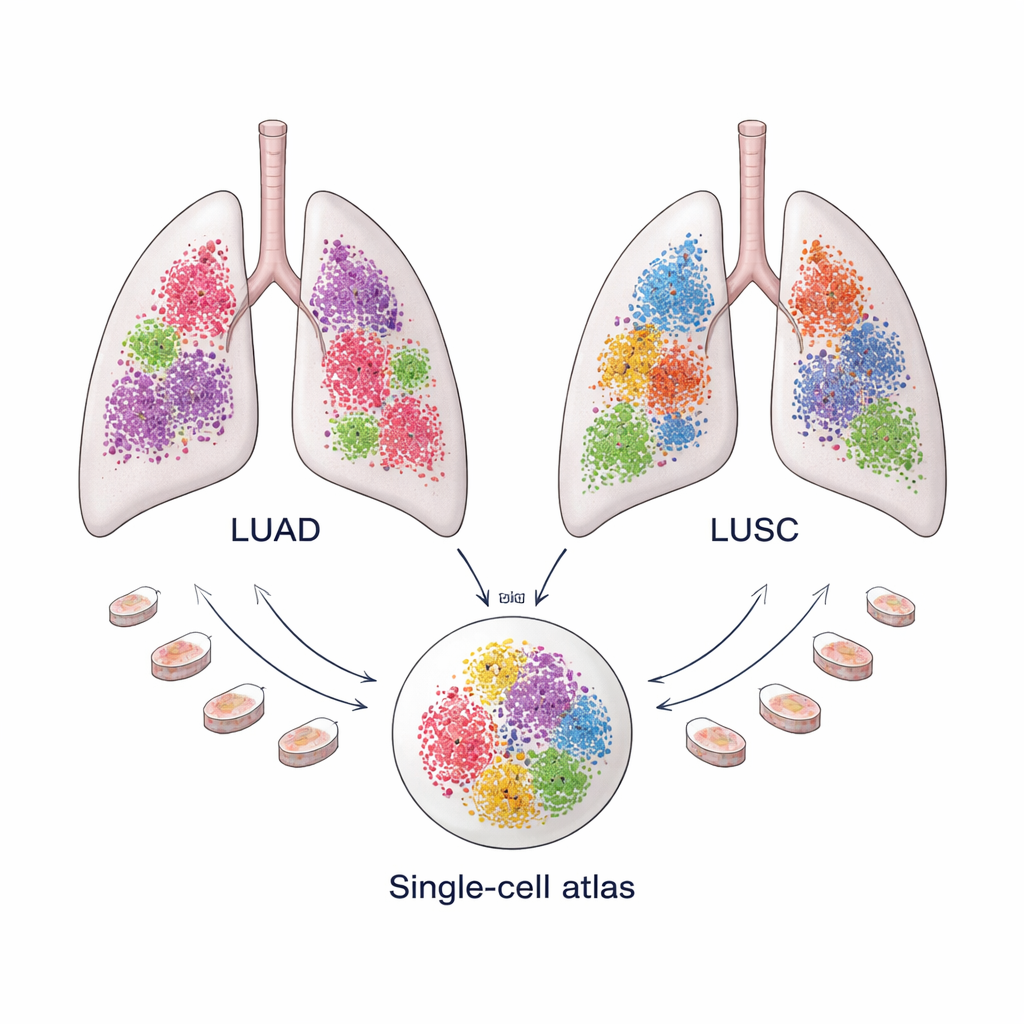
Due tumori polmonari comuni, due ecosistemi distinti
Il carcinoma polmonare non a piccole cellule rappresenta circa l'85% dei tumori polmonari ed è dominato da due tipi: l'adenocarcinoma polmonare (LUAD), che spesso nasce nelle zone periferiche del polmone, e il carcinoma squamoso polmonare (LUSC), che tende a comparire in posizione più centrale. Sebbene oggi vengano trattati sotto la stessa etichetta generale, rispondono in modo diverso alle terapie e hanno esiti a lungo termine distinti. Evidenze crescenti suggeriscono che queste differenze non siano dovute solo alle cellule tumorali, ma anche al “microambiente tumorale”—la combinazione di cellule immunitarie, vasi sanguigni e cellule strutturali che circondano e interagiscono con il tumore.
Costruire un atlante del cancro polmonare a singola cellula
Per comprendere questi microambienti in dettaglio, il gruppo ha assemblato un grande “atlante” di dati di sequenziamento dell'RNA a singola cellula: 366.652 cellule provenienti da 175 campioni di LUAD e 125.238 cellule da 74 campioni di LUSC, ricavate da dieci dataset pubblici. Il modello di espressione genica di ciascuna cellula ha funzionato come un'impronta digitale che ha permesso ai ricercatori di raggruppare le cellule in categorie principali come cellule immunitarie, cellule vascolari, cellule tumorali e cellule strutturali o stromali. Metodi computazionali sofisticati hanno poi rimosso il rumore tecnico e allineato i campioni in modo che le cellule di pazienti diversi potessero essere confrontate direttamente. Questa scala è cruciale, perché alcuni tipi cellulari—soprattutto i fibroblasti—sono rari e difficili da isolare in numero sufficiente in un singolo studio.
Fibroblasti: gli architetti del paesaggio tumorale
I fibroblasti sono cellule di supporto che costruiscono e rimodellano il tessuto connettivo. Nei tumori diventano fibroblasti associati al cancro (CAF), che possono o limitare o favorire la crescita tumorale a seconda del loro stato. Concentrandosi su oltre 8.700 fibroblasti, gli autori hanno identificato cinque principali sottotipi di CAF: CAF miofibroblastici (mCAF), CAF infiammatori (iCAF), CAF associati ai vasi (vCAF), CAF in ciclo (cCAF) e CAF presentanti antigeni (apCAF). L'equilibrio tra questi sottotipi differiva in modo marcato tra LUAD e LUSC. I tumori LUAD tendevano a contenere più iCAF, che secernono alti livelli di molecole infiammatorie, mentre i tumori LUSC erano più ricchi di mCAF, che producono tessuto fibroso e rigido e aiutano a modellare l'impalcatura fisica del tumore.
Le cellule tumorali istruiscono i fibroblasti sul loro ruolo
Per verificare se siano le cellule tumorali stesse a istruire i fibroblasti ad assumere queste identità, i ricercatori hanno coltivato fibroblasti polmonari normali in piastre accanto a linee cellulari LUAD o LUSC. Esposti a cellule LUAD, i fibroblasti hanno attivato geni tipici degli iCAF, compresi noti segnali infiammatori come IL-6 e alcune chemochine. In presenza di cellule LUSC, gli stessi fibroblasti hanno invece attivato geni mCAF coinvolti nella contrazione simile a quella muscolare e nella produzione di collagene. Analisi delle comunicazioni cellula-cellula hanno suggerito che le cellule LUAD utilizzano citochine come IL-1, LIF e OSM per guidare lo stato infiammatorio degli iCAF, mentre le cellule LUSC si affidano maggiormente a segnali meccanici e alla segnalazione WNT non canonica per spingere i fibroblasti verso lo stato mCAF, orientato alla costruzione della matrice.
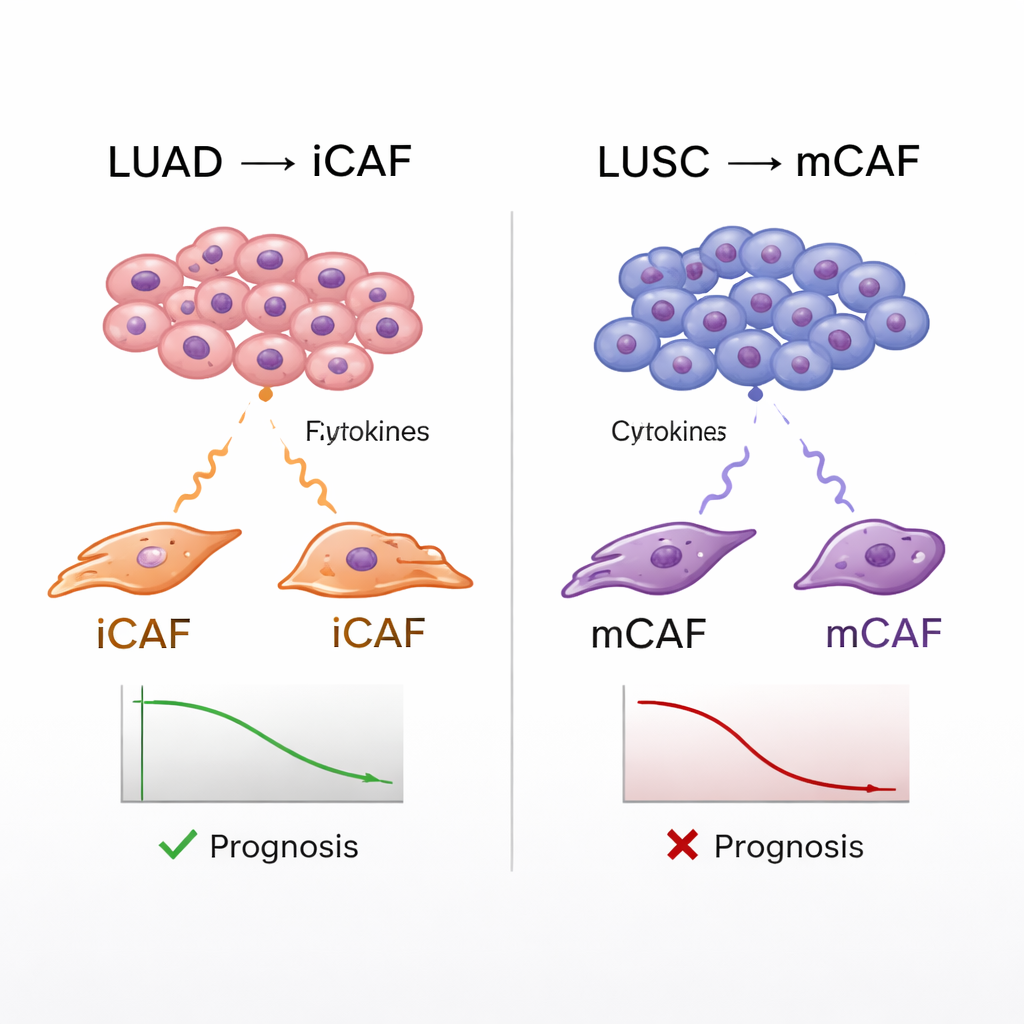
Collegare i tipi di fibroblasti con gli esiti dei pazienti
L'atlante ha permesso anche al gruppo di collegare i sottotipi di CAF ai dati clinici reali dei pazienti. Utilizzando grandi banche dati sul cancro, hanno stimato quanto fortemente il tumore di ciascun paziente esprimesse firme geniche corrispondenti ai diversi tipi di fibroblasti, quindi hanno confrontato questi punteggi con la sopravvivenza. In entrambi LUAD e LUSC, i tumori arricchiti in mCAF erano associati a esiti peggiori, coerentemente con l'idea che una capsula densa e fibrosa attorno ai tumori possa favorire la progressione tumorale e ostacolare l'attacco immunitario. Gli iCAF, invece, hanno mostrato una doppia natura: in LUSC, firme iCAF elevate prevedevano anche una sopravvivenza peggiore, mentre in LUAD erano associate a esiti migliori. Analisi ulteriori hanno suggerito che in LUSC gli iCAF contribuiscono ad attrarre neutrofili—cellule immunitarie che, in questo contesto, sembrano sopprimere i linfociti T benefici—creando un ambiente particolarmente ostile alle risposte immunitarie efficaci.
Cosa significa per la cura futura del cancro polmonare
Per un non specialista, il messaggio chiave è che non tutte le cellule di supporto nei tumori polmonari sono uguali, e lo stesso sottotipo di fibroblasto può avere significati opposti a seconda del contesto tumorale. LUAD e LUSC non differiscono solo nel DNA delle loro cellule tumorali; costruiscono ecosistemi microscopici diversi che modellano come i tumori crescono e come vanno i pazienti. Mappando questi ecosistemi cellula per cellula, questo studio identifica popolazioni specifiche di fibroblasti che potrebbero servire come marker prognostici o come bersagli per terapie future—consentendo idealmente trattamenti personalizzati non solo in base al tipo di tumore, ma anche al mosaico di cellule che lo circondano e lo sostengono.
Citazione: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
Parole chiave: cancro polmonare, microambiente tumorale, fibroblasti, sequenziamento dell'RNA a singola cellula, prognosi del cancro