Clear Sky Science · it
TheraMind: un ensemble multi-LLM per accelerare il riposizionamento di farmaci nel cancro al polmone tramite l’estrazione da case report
Perché è importante per pazienti e medici
Per le persone con cancro al polmone avanzato, il tempo è prezioso e le opzioni terapeutiche spesso si esauriscono rapidamente. Sviluppare farmaci completamente nuovi può richiedere più di un decennio, ma indizi sparsi su terapie utili potrebbero già essere nascosti nelle storie cliniche pubblicate come case report. Questo articolo presenta TheraMind, un sistema di intelligenza artificiale che analizza migliaia di questi report per individuare farmaci esistenti che potrebbero essere riutilizzati in modo sicuro per aiutare pazienti con tumori polmonari difficili da trattare.
La sfida di trovare nuovi usi per farmaci già esistenti
Il carcinoma polmonare non a piccole cellule è il cancro più letale al mondo, con tassi di sopravvivenza che restano molto bassi una volta che la malattia si è diffusa. Scoprire e testare nuovi farmaci da zero è un processo lento, costoso e rischioso. Al contrario, i farmaci “riposizionati” sono già approvati per altre condizioni, quindi la loro sicurezza è in gran parte nota. Gli oncologi sono interessati a questi farmaci, soprattutto per pazienti che hanno esaurito i trattamenti standard, ma hanno bisogno di evidenze dal mondo reale che un farmaco abbia effettivamente aiutato qualcuno con cancro al polmone — non solo dati promettenti in laboratorio. Questi indizi clinici spesso compaiono in singoli case report sepolti nella letteratura medica, difficili e dispendiosi da trovare manualmente.
Un lettore digitale per migliaia di storie di pazienti
I ricercatori hanno costruito TheraMind per funzionare come un lettore instancabile e accurato dei case report. Partendo da 18 candidati farmacologici suggeriti da studi genomici e di laboratorio precedenti, il sistema ha automaticamente estratto 10.023 case report da PubMed, il più grande database di articoli medici. Ha poi inviato il testo di ogni report a tre modelli linguistici distinti — diversi “lettori” di AI addestrati a comprendere la scrittura medica. Per ciascun report, questi modelli hanno risposto alle stesse quattro semplici domande: il paziente è descritto come affetto da carcinoma polmonare non a piccole cellule? Il farmaco in studio è stato somministrato specificamente per trattarlo? Il trattamento è stato interrotto precocemente? E il paziente ha avuto un buon esito clinico?
Come il team di AI arriva a una decisione comune
Una volta che TheraMind trasforma ogni report in un insieme di risposte sì/no, entrano in gioco diversi livelli di decisione. Un metodo utilizza un albero decisionale costruito a mano che richiede che tutte e quattro le condizioni siano soddisfatte prima di considerare un caso rilevante per il riposizionamento farmacologico. Un altro consente a un singolo modello di valutare le prove in modo più flessibile, considerando sia le risposte sì/no sia le brevi spiegazioni che ha prodotto. Il metodo più potente combina tre classificatori separati, ciascuno basato su un modello diverso, e accetta un report solo quando almeno due dei tre concordano che sia rilevante. Questo approccio a “voto di maggioranza” aiuta a cancellare errori individuali, un po’ come chiedere a diversi medici indipendenti di rivedere lo stesso fascicolo.
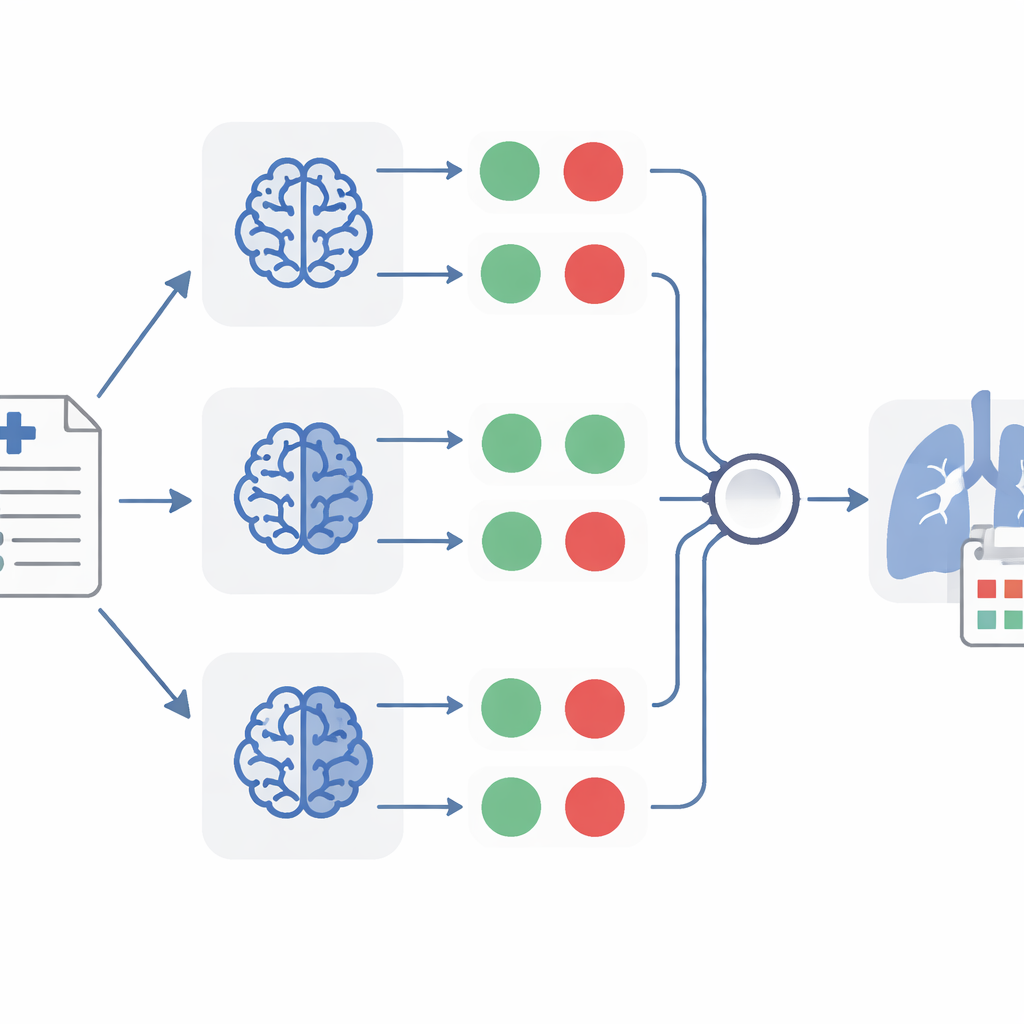
Cosa ha scoperto TheraMind nei report sul cancro al polmone
Applicato alla vasta raccolta di case report, TheraMind ha segnalato 26 documenti come fortemente indicativi dell’uso di dieci diversi farmaci nel carcinoma polmonare non a piccole cellule. Il metodo ensemble ha raggiunto un richiamo (recall) di circa il 92 percento, il che significa che ha catturato quasi tutti i report realmente rilevanti, mantenendo al contempo una specificità molto alta del 99,7 percento, così che pochissimi report irrilevanti sono passati. Per ciascun report selezionato, il sistema ha anche estratto dettagli chiave del paziente — come età, sesso, storia medica, condizione e il farmaco sospettato — in un formato di dati coerente, e ha generato un breve sommario semplice del caso. Revisori umani con background in biologia e informatica hanno controllato questi output e hanno confermato che uno dei modelli in particolare produceva estrazioni molto accurate e complete.
Oltre il cancro al polmone e verso la clinica
Per testare la flessibilità del sistema, il team ha anche applicato TheraMind al cancro al seno e a diversi farmaci candidati identificati in precedenza dalla loro ricerca. In quel contesto, il sistema non ha riportato case report corrispondenti, riflettendo accuratamente il record scientifico attuale invece di inventare prove. Gli autori sostengono che questo tipo di pipeline strutturata e trasparente — che combina logica basata su regole con più lettori AI — può contribuire a colmare il divario tra scoperte di laboratorio e trattamenti pronti per studi clinici. Mettono in evidenza sia la promessa di applicare metodi simili ad altri tumori sia la necessità di gestire attentamente la privacy dei pazienti se versioni future si collegassero direttamente alle cartelle cliniche elettroniche.
Cosa significa per i trattamenti futuri
In termini semplici, TheraMind trasforma storie di pazienti sparse e non strutturate in evidenze organizzate su cui medici e ricercatori possono agire. Facendo emergere rapidamente i report in cui farmaci esistenti sembrano aiutare persone con cancro al polmone, può guidare quali medicinali riposizionati meritano uno studio più approfondito in trial clinici. Pur non sostituendo il giudizio medico, questo lettore AI multimodello offre un modo per setacciare montagne di testi medici e fornire una lista breve e affidabile di opzioni promettenti per pazienti che hanno urgente bisogno di nuove alternative.
Citazione: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
Parole chiave: riposizionamento di farmaci, cancro del polmone, case report, modelli linguistici di grandi dimensioni, estrazione di evidenze cliniche