Clear Sky Science · it
Neoadiuvante con sintilimab, paclitaxel legato all'albumina e carboplatino per carcinoma squamoso esofageo localmente avanzato e resecabile: studio clinico ed esplorazione meccanicistica
Invertire la rotta contro un letale tumore della gola
Il cancro esofageo è tra i tumori più letali a livello mondiale, spesso diagnosticato solo dopo che si è esteso in profondità nella cavità toracica. Molti pazienti possono ancora essere sottoposti a chirurgia, ma anche con la migliore chemioterapia e radioterapia odierna il rischio di recidiva rimane elevato. Questo studio mette alla prova un nuovo modo di potenziare le difese dell’organismo prima dell’intervento e analizza al microscopio come cambiano i tumori e le cellule circostanti in risposta. I risultati suggeriscono trattamenti più efficaci e un percorso verso cure veramente personalizzate.
Un nuovo schema a tre farmaci prima dell’intervento
I ricercatori hanno arruolato 24 persone in Cina affette da una forma comune e aggressiva di cancro esofageo chiamata carcinoma squamoso. Tutti avevano tumori avanzati ma ancora asportabili chirurgicamente. Prima dell’intervento, ogni paziente ha ricevuto tre cicli di una terapia combinata: sintilimab, un anticorpo che attiva il sistema immunitario aiutando le cellule T a riconoscere il cancro; più due farmaci chemioterapici standard, paclitaxel legato all’albumina e carboplatino. Dopo questa fase neoadiuvante, i pazienti sono stati sottoposti a chirurgia per rimuovere il tumore esofageo e la maggior parte ha poi proseguito con sintilimab in seguito.
Maggiore riduzione tumorale e sopravvivenza incoraggiante
Quando chirurghi e patologi hanno esaminato i tumori asportati, hanno constatato che questo regime preoperatorio aveva prodotto una marcata riduzione in molti pazienti. Circa il 42% ha mostrato quella che i medici definiscono una risposta patologica maggiore, ossia è rimessa solo una piccola frazione di cellule tumorali vive. Un paziente su tre non aveva cellule tumorali rilevabili nell’area principale del tumore. Su immagini e follow-up clinico i risultati sono stati altrettanto promettenti: tre anni dopo il trattamento, circa tre pazienti su quattro erano vivi senza segni di recidiva e quasi quattro su cinque erano ancora in vita. È importante notare che gli effetti collaterali di questo schema intensificato sono stati gestibili, senza decessi correlati alla terapia e con la chirurgia rimasta sicura e praticabile.
Come il quartiere del tumore modella la risposta
Non tutti i pazienti hanno beneficiato allo stesso modo, così il team ha cercato di capire il perché. Si sono concentrati sul microambiente tumorale — il complesso contesto di cellule tumorali, cellule immunitarie e molecole di segnalazione. Utilizzando misure proteiche mirate su campioni tumorali accuratamente dissezionati, hanno confrontato chi ha risposto bene con chi non ha risposto. Prima del trattamento hanno trovato 14 proteine che differivano tra i due gruppi. Una proteina di superficie, CD44, è emersa in modo particolare: i tumori con livelli più alti di CD44 tendevano a rispondere meglio alla terapia a base di sintilimab. Dopo il trattamento, molte proteine coinvolte nell’attività immunitaria e nella riparazione del DNA erano ridotte nei responder, suggerendo che la terapia combinata avesse interrotto con successo i sistemi di supporto del tumore e rimodellato il paesaggio immunitario locale.
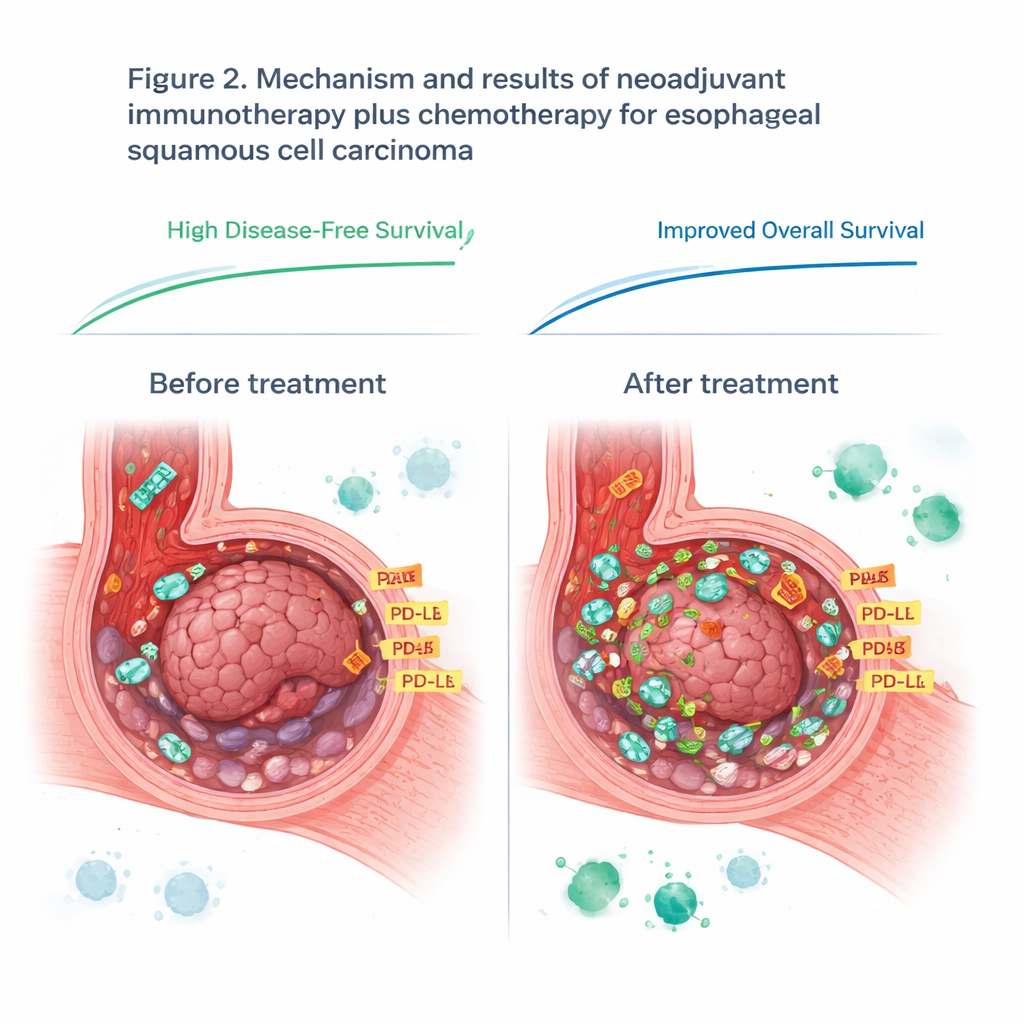
Riconsiderare un marcatore immunitario popolare
Lo studio ha inoltre esaminato PD-L1, una proteina spesso usata come guida per decidere chi potrebbe beneficiare dei farmaci che bloccano i checkpoint immunitari. Prima del trattamento, i livelli di PD-L1 sui campioni tumorali non prevedevano chi avrebbe avuto un buon esito, mettendo in discussione la pratica corrente per questo tipo di tumore. Tuttavia, i livelli di PD-L1 sono aumentati in ogni paziente durante la terapia, probabilmente perché il sistema immunitario attivato ha inondato il tumore di segnali infiammatori. Dopo la terapia, livelli più alti di PD-L1 nel tessuto tumorale residuo sono stati più strettamente collegati all’efficacia dell’immunoterapia. Ciò suggerisce che il fattore tempo è importante: una singola misurazione di PD-L1 prima del trattamento può perdere cambiamenti cruciali che emergono una volta che il sistema immunitario è attivato.
Cosa significa per i pazienti e per il futuro
Per le persone che si trovano ad affrontare un intervento per un cancro esofageo avanzato, questo studio offre due messaggi di speranza. Primo, combinare sintilimab con la chemioterapia prima dell’intervento sembra ridurre i tumori in modo più profondo e può migliorare le probabilità di sopravvivenza a lungo termine, senza aggiungere effetti collaterali pericolosi. Secondo, il lavoro mostra che il tumore e il suo microambiente non sono fissi; vengono rimodellati dal trattamento in modi che possono essere tracciati attraverso proteine come PD-L1 e CD44. In futuro, queste impronte molecolari potrebbero aiutare i medici a selezionare e adattare le terapie in tempo reale, trasformando più tumori “freddi” che ignorano il sistema immunitario in tumori “caldi” che invitano a un attacco immunitario potente e duraturo.
Citazione: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
Parole chiave: cancro esofageo, immunoterapia, terapia neoadiuvante, inibitori PD-1, microambiente tumorale