Clear Sky Science · it
La trascrittomica spaziale rivela eterogeneità molecolare e bersagli terapeutici specifici per sottotipo nel carcinoma polmonare microcitico
Perché questo studio sul cancro al polmone è importante
Il carcinoma polmonare microcitico è una delle forme di cancro più letali, colpisce soprattutto persone con una storia di fumo e tende a ricomparire rapidamente dopo la chemioterapia. I medici sanno che non tutti i carcinomi microcitici si comportano allo stesso modo, ma sono mancati strumenti per osservare come i diversi tipi di cellule tumorali e le cellule immunitarie siano organizzati all’interno di ciascun tumore. Questo studio ha usato una nuova tecnologia che legge l’attività genica in migliaia di piccoli punti su un vetrino tumorale, creando una “mappa molecolare” di ogni campione. Abbinando questo approccio ad analisi informatiche su misura, i ricercatori hanno scoperto schemi nascosti che potrebbero indicare trattamenti più precisi e specifici per sottotipo.
Mappare i tumori in sede
Il gruppo ha analizzato campioni tumorali di 21 pazienti con carcinoma polmonare microcitico in stadio limitato che avevano subito intervento chirurgico prima di ricevere farmaci. Invece di omogeneizzare il tessuto e perdere tutte le informazioni spaziali, hanno applicato la trascrittomica spaziale: una tecnica che misura quali geni sono attivi in molti punti definiti di una sezione tissutale. Ogni punto mantiene la propria posizione originale, permettendo agli scienziati di collegare l’attività genica a dove si trovano fisicamente cellule tumorali, cellule normali e cellule immunitarie. Hanno aggiunto due strumenti chiave: un nuovo punteggio “Edgeindex” per quantificare quanto profondamente le cellule tumorali infiltrano il tessuto adiacente, e una rete neurale artificiale — una forma di apprendimento automatico — per marcare automaticamente quali punti sono tumorali e quali no.
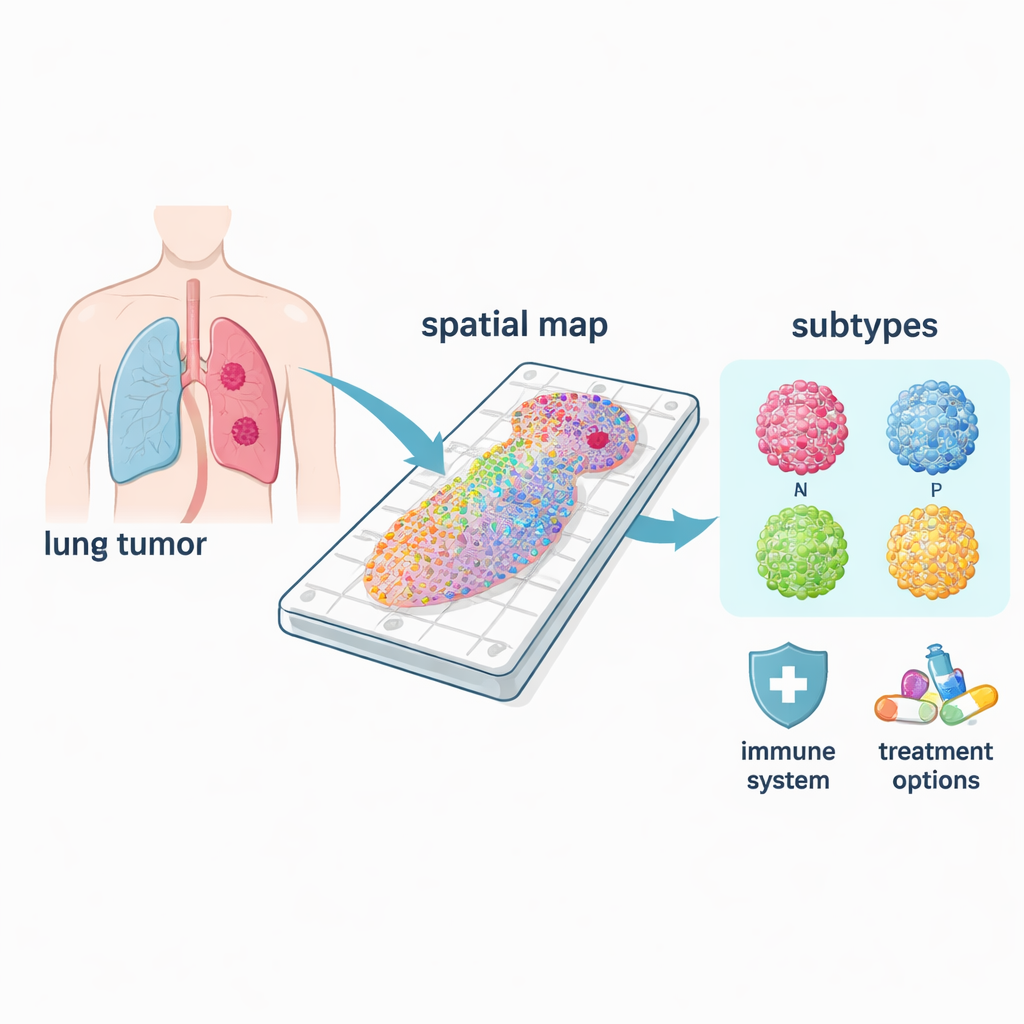
Diversi tipi di cancro in una sola malattia
Il carcinoma polmonare microcitico non è una singola malattia ma include almeno quattro sottotipi molecolari principali, spesso indicati come ASCL1, NEUROD1, POU2F3 e YAP1, dal nome di geni regolatori chiave che li definiscono. Usando le loro mappe spaziali, i ricercatori hanno potuto vedere dove ciascun sottotipo dominava all’interno dei tumori e come la loro biologia differisse. Le forme comuni ASCL1 e NEUROD1 erano fortemente associate a programmi di divisione cellulare, coerenti con la loro reputazione di elevata proliferazione. Al contrario, le regioni POU2F3 erano legate a percorsi correlati al sistema immunitario, mentre le aree YAP1 mostravano segnali relativi al metabolismo e al rimodellamento tissutale, caratteristiche che potrebbero collegarsi alla diffusione e alla resistenza ai trattamenti. Poiché questi schemi sono risolti nello spazio, il metodo può identificare il vero sottotipo “driver” all’interno di un tumore misto, cosa che i test in bulk spesso non colgono.
Il bordo invasivo e il cambiamento immunitario
Una delle innovazioni centrali dello studio, l’Edgeindex, cattura quanto le cellule tumorali si mescolano con il tessuto non tumorale circostante. Punteggi bassi riflettono tumori compatti e ben delimitati, mentre punteggi alti indicano isole disperse e bordi frastagliati e invasivi. I tumori con Edgeindex elevato erano arricchiti per programmi genici legati alla matrice extracellulare, alla metastasi e alla morte cellulare. Mostravano anche un paesaggio immunitario marcatamente alterato: meno linfociti T helper e altri attori dell’immunità adattativa, ma più cellule innate come alcune cellule natural killer e monociti. Gli autori interpretano questo come un “rimodellamento della nicchia immunologica”, in cui il tumore allontana risposte immunitarie precise e mirate e lascia un difetto difensivo meno efficace, in gran parte di tipo innato, che non riesce a controllare pienamente il cancro.
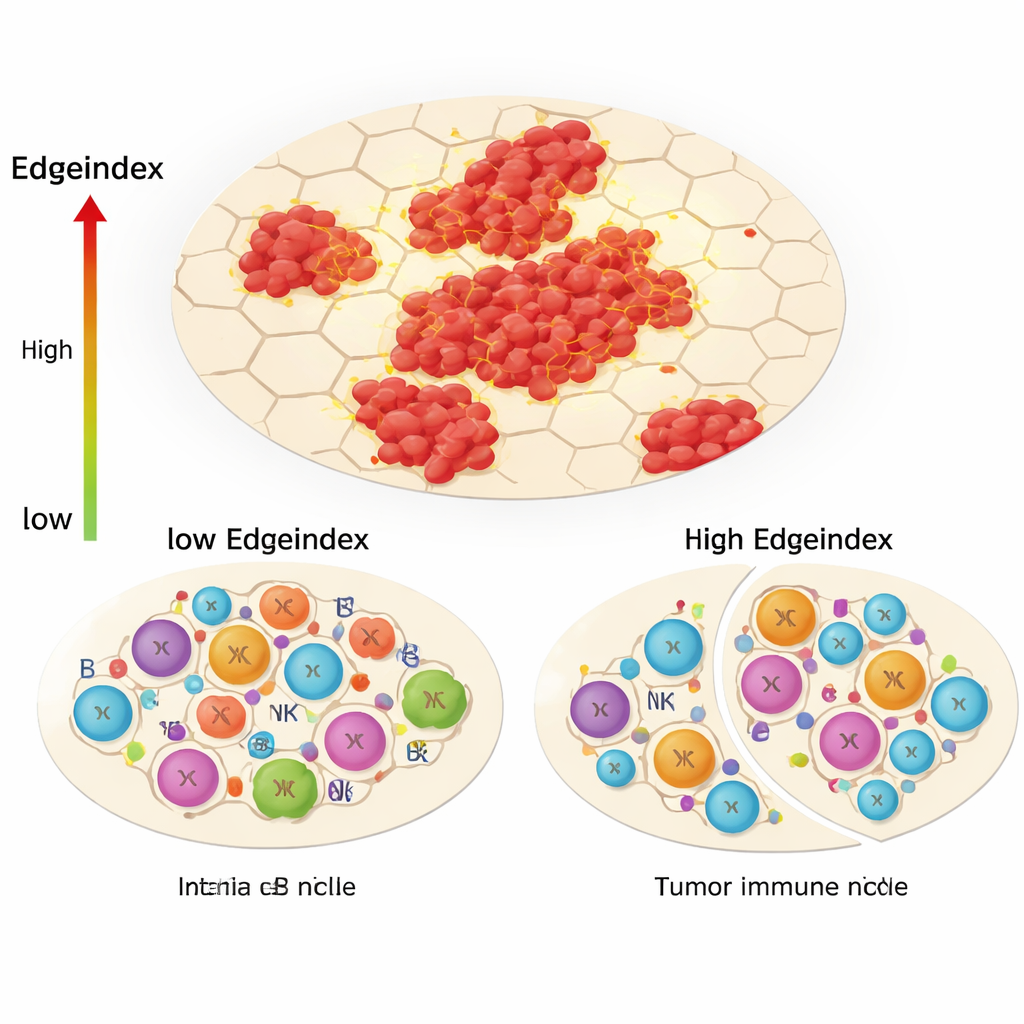
Diversità nascosta dentro e intorno ai tumori
Oltre ai sottotipi e ai modelli di invasione, i dati spaziali hanno rivelato che sia le popolazioni di cellule tumorali sia i microambienti circostanti erano internamente eterogenei. Raggruppando i punti all’interno di ciascun tumore, il gruppo ha contato quante “nazioni” distinte di espressione genica esistevano nelle regioni tumorali e nel tessuto non tumorale vicino. Una maggiore diversità all’interno del tumore era legata a percorsi correlati all’immunità, mentre certi schemi nel tessuto circostante erano associati all’attività del ciclo cellulare e alla regolazione genetica. I ricercatori hanno anche esaminato quanto intensamente diverse regioni “comunicavano” usando molecole di segnalazione note. I tumori con comunicazione più intensa tra regioni tendevano a mostrare segnali immunitari più forti, rafforzando l’idea che l’attività immunitaria e la crescita tumorale siano strettamente intrecciate nello spazio.
Seguire lo sviluppo tumorale nel tempo
Per approssimare come le cellule tumorali cambiano man mano che la malattia progredisce, il gruppo ha eseguito un’analisi di “pseudotempo” che ordina le cellule lungo un percorso di sviluppo basato sull’attività genica. Tra i campioni, hanno identificato ripetutamente un gene, UCHL1, come centrale in queste traiettorie. Livelli elevati di UCHL1 coincidevano con forte attività del ciclo cellulare nei punti tumorali, mentre livelli più bassi si allineavano con percorsi legati all’immunità e alla morte cellulare. Poiché UCHL1 è una proteina di tipo neuronale precedentemente collegata a forme aggressive di tumore polmonare, questi risultati rafforzano l’ipotesi che possa essere un utile bersaglio farmacologico, in particolare per le cellule di tipo neuroendocrino che guidano il carcinoma polmonare microcitico.
Cosa significa per i pazienti
In termini semplici, questo studio trasforma vetrini piatti di carcinoma polmonare microcitico in mappe ricche e stratificate che mostrano dove si trovano i diversi sottotipi tumorali, quanto aggressivamente invadono, come comunicano con l’ambiente circostante e come il sistema immunitario risponde o fallisce. Il nuovo punteggio Edgeindex e l’approccio di mappatura evidenziano quali tumori sono particolarmente infiltrativi e quali cellule immunitarie sono presenti o assenti al margine. Collegando questi schemi spaziali a vulnerabilità specifiche di sottotipo — come farmaci che prendono di mira DLL3, BCL‑2, AURKA, IGF‑1R/PARP o i punti di controllo immunitari — il lavoro avvicina il campo all’abbinare ogni paziente a una strategia terapeutica su misura. Sebbene questi strumenti debbano ancora essere testati in studi più ampi, offrono un modello per terapie più precise e potenzialmente più efficaci in un tipo di cancro che ha urgente bisogno di opzioni migliori.
Citazione: Xie, T., Tang, L., Fan, G. et al. Spatial transcriptomics reveals molecular heterogeneity and subtype-specific therapeutic targets in small cell lung cancer. npj Precis. Onc. 10, 81 (2026). https://doi.org/10.1038/s41698-025-01243-7
Parole chiave: carcinoma polmonare microcitico, trascrittomica spaziale, eterogeneità tumorale, microambiente immunitario tumorale, oncologia di precisione