Clear Sky Science · it
Decifrare le metastasi cerebrali nel carcinoma ovarico epiteliale: analisi multimodale e potenziali biomarcatori
Perché questa ricerca è importante
Il carcinoma ovarico è già una malattia pericolosa, ma in una piccola percentuale di donne si manifesta successivamente in una sede molto più fragile: il cervello. Queste metastasi cerebrali sono rare ma spesso letali, e i medici hanno ancora pochi strumenti per prevedere chi è a rischio o come trattarle al meglio. Questo studio segue quel percorso dal bacino al cervello a livello molecolare, utilizzando strumenti moderni per analizzare DNA e RNA per capire come i tumori ovarici si adattano al cervello e individuare segnali di allarme precoci che un giorno potrebbero guidare cure più personalizzate.
Da un tumore comune a una minaccia cerebrale rara
Il carcinoma ovarico epiteliale è il tumore ginecologico più letale nei paesi sviluppati. La maggior parte delle pazienti risponde inizialmente a chirurgia e chemioterapia, ma circa l’80% vede infine la recidiva della malattia e lo sviluppo di resistenza ai farmaci. Le recidive restano solitamente nell’addome; solo una piccola frazione di donne sviluppa diffusione a distanza, come al cervello. Tuttavia, con il miglioramento delle terapie e l’aumento della sopravvivenza, c’è più tempo perché cellule tumorali vaganti impiantino il cervello, e i medici stanno osservando queste metastasi più frequentemente. Quando le metastasi cerebrali compaiono, la sopravvivenza tipica scende sotto l’anno, sottolineando la necessità di capire come e perché ciò avviene.
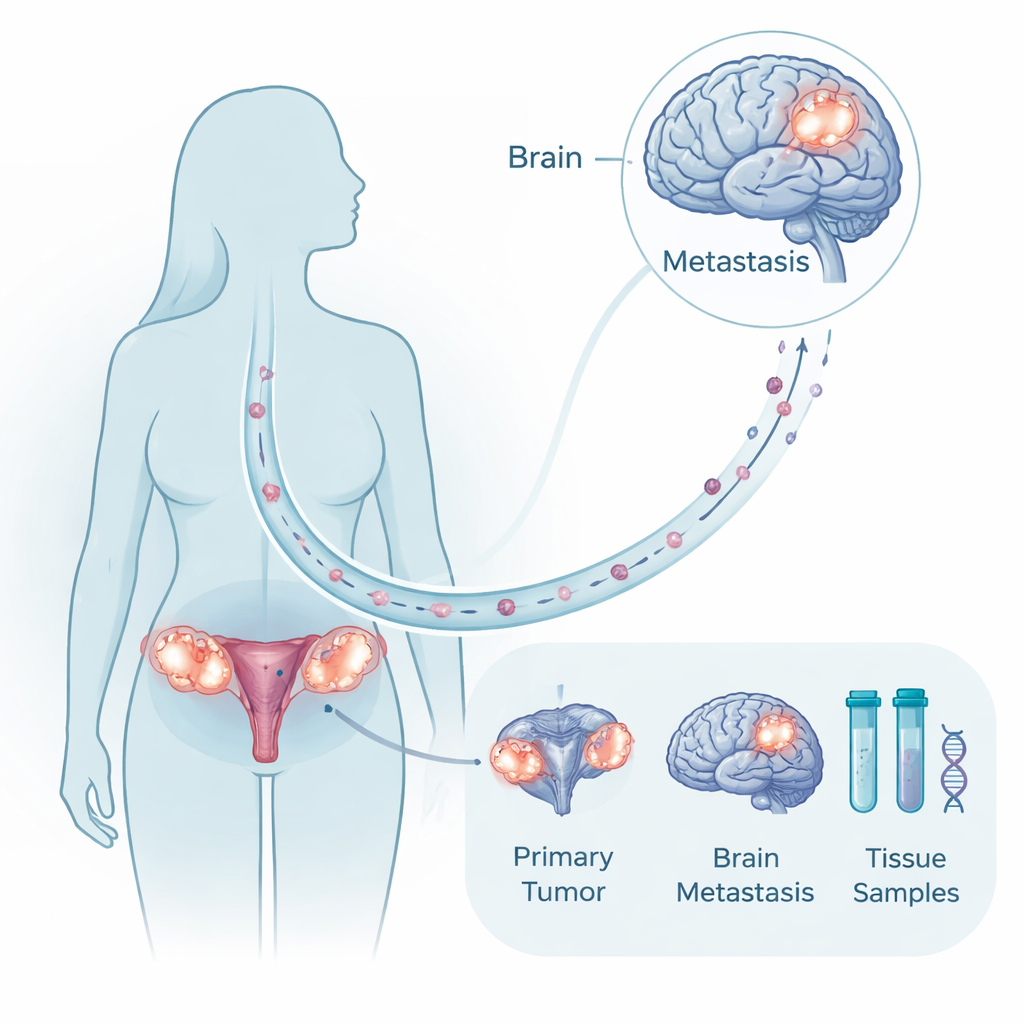
Una raccolta tissutale rara ma preziosa
Poiché la neurochirurgia non è possibile o appropriata per molte pazienti, è insolito disporre di campioni tumorali sia della massa ovarica primaria sia del corrispondente deposito cerebrale nella stessa donna. I ricercatori hanno raccolto esattamente questo tipo di materiale accoppiato proveniente da dieci pazienti trattate nell’arco di due decenni, insieme a campioni di confronto da cervello e ovaio sani e da altre metastasi non cerebrali. Hanno analizzato il DNA tumorale per cercare mutazioni e ampie variazioni cromosomiche, e hanno profilato l’RNA per vedere quali geni erano attivi o spenti. Questo approccio multimodale ha permesso di interrogarsi se i tumori cerebrali siano del tutto nuovi rami evolutivi o cugini strettamente correlati al primario, e quali programmi molecolari cambino quando le cellule si radicano nel cervello.
Stabilità genetica, ma nuovo comportamento
L’analisi del DNA ha mostrato che i tumori ovarici originari e le corrispondenti metastasi cerebrali erano sorprendentemente simili. Entrambi presentavano molte delle stesse mutazioni oncogene, in particolare in un gene chiamato TP53, e condividevano un’origine complessiva «monoclonale», il che significa che le lesioni cerebrali sembrano derivare dalla stessa cellula cancerosa ancestrale. Guadagni e perdite di porzioni di DNA erano un po’ più frequenti nelle lesioni cerebrali, ma non in modo schiacciante. Ciò suggerisce che non è l’acquisizione di un set completamente nuovo di mutazioni a consentire la diffusione al cervello. Invece, il cambiamento critico appare a livello dell’attività genica: quali istruzioni vengono lette dal DNA e usate dalle cellule tumorali mentre si adattano all’ambiente unico del cervello.
Come i tumori ovarici imparano a vivere nel cervello
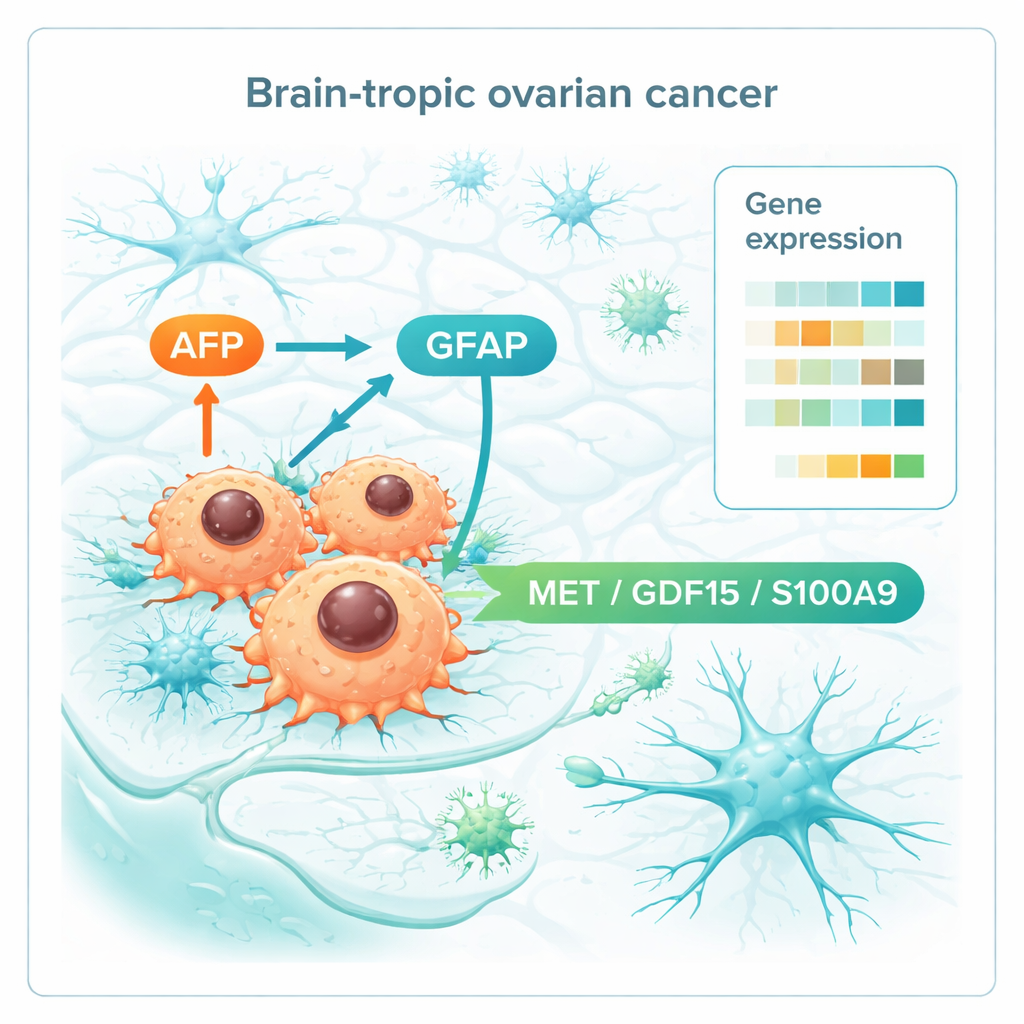
Quando il gruppo ha confrontato l’attività genica tra tutti i tessuti, è emersa una firma distinta delle metastasi cerebrali. Le lesioni cerebrali mostravano segni di crescita aggressiva, con attivazione di programmi del ciclo cellulare guidati da noti regolatori del cancro come MYC ed E2F. Hanno inoltre modificato le proteine che formano e rimodellano l’impalcatura tissutale, facilitando l’invasione e l’ancoraggio nelle sostanze cerebrali. In modo notevole, alcuni geni associati a neuroni e cellule gliali risultavano accesi, suggerendo che le cellule del carcinoma ovarico in parte mimano le cellule cerebrali per integrarsi. Tra i più evidenti c’erano AFP, solitamente attivo nel feto e in certi tumori, e GFAP, una proteina caratteristica delle cellule di supporto nel cervello. Gli autori hanno anche identificato un piccolo gruppo di geni già elevati nei tumori ovarici primari delle donne che in seguito svilupparono metastasi cerebrali ma non nei sopravvissuti a lungo termine senza coinvolgimento cerebrale. Questo schema «premetastatico» coinvolgeva modulazione immunitaria, comunicazione tramite segnali di tipo nervoso e cambiamenti nel metabolismo.
Segnali di allarme precoci e dialogo molecolare
Approfondendo, i ricercatori si sono concentrati su molecole che si trovano sulla superficie cellulare o che vengono secrete, perché sono candidati ideali per test nel sangue o per bersagli farmacologici. Hanno individuato tre attori — MET, GDF15 e S100A9 — che risultavano costantemente più alti sia nei tumori primari destinati al cervello sia nelle metastasi cerebrali stesse. Queste molecole sono coinvolte nel movimento cellulare, nella percezione dello stress e dei nutrienti e nella modellazione dell’ambiente immunitario, suggerendo che aiutino le cellule del carcinoma ovarico a comunicare e rimodellare il tessuto cerebrale a loro vantaggio. Insieme ad AFP e GFAP, costituiscono una breve lista di potenziali biomarcatori che un giorno potrebbero segnalare pazienti ad alto rischio o indicare farmaci in grado di interrompere la comunicazione tumore–cervello.
Cosa significa per le pazienti
Per ora, questo lavoro non cambierà immediatamente il trattamento, e gli autori riconoscono che il loro gruppo di pazienti è piccolo. Tuttavia, mostrando che i carcinomi ovarici metastatizzanti al cervello mantengono gran parte del loro patrimonio genetico originale pur rimodulando l’uso dei loro geni, lo studio mette in luce nuovi modi per individuare tempestivamente segnali di pericolo. Se ricerche future confermeranno che marker come AFP, GFAP, MET, GDF15 e S100A9 segnalano in modo affidabile una tendenza a diffondersi al cervello, i medici potrebbero sorvegliare più da vicino certe pazienti, modificare le scelte terapeutiche o testare farmaci che bloccano queste vie. In sostanza, lo studio comincia a trasformare una complicanza tardiva e temibile in un processo che può essere misurato, compreso e, alla fine, intercettato.
Citazione: Trozzi, R., Salvi, M., Karimi, M. et al. Deciphering brain metastasis in epithelial ovarian cancer: multimodal analysis and potential biomarkers. npj Precis. Onc. 10, 83 (2026). https://doi.org/10.1038/s41698-025-01206-y
Parole chiave: carcinoma ovarico, metastasi cerebrali, biomarcatori, espressione genica, oncologia di precisione