Clear Sky Science · it
Metodi per la valutazione randomizzata, in cieco e controllata di ipotetici interventi terapeutici in reti multilaboratorio di valutazione preclinica
Perché questo è importante per la salute di tutti i giorni
Molti trattamenti medici promettenti appaiono efficaci negli studi sugli animali ma poi falliscono in grandi e costosi trial clinici. Questo articolo mostra, in dettaglio concreto, come gli scienziati possano riprogettare quei test preclinici iniziali affinché i loro risultati siano più affidabili e più predittivi di ciò che accadrà nei pazienti reali—utilizzando l’ictus come caso di prova. 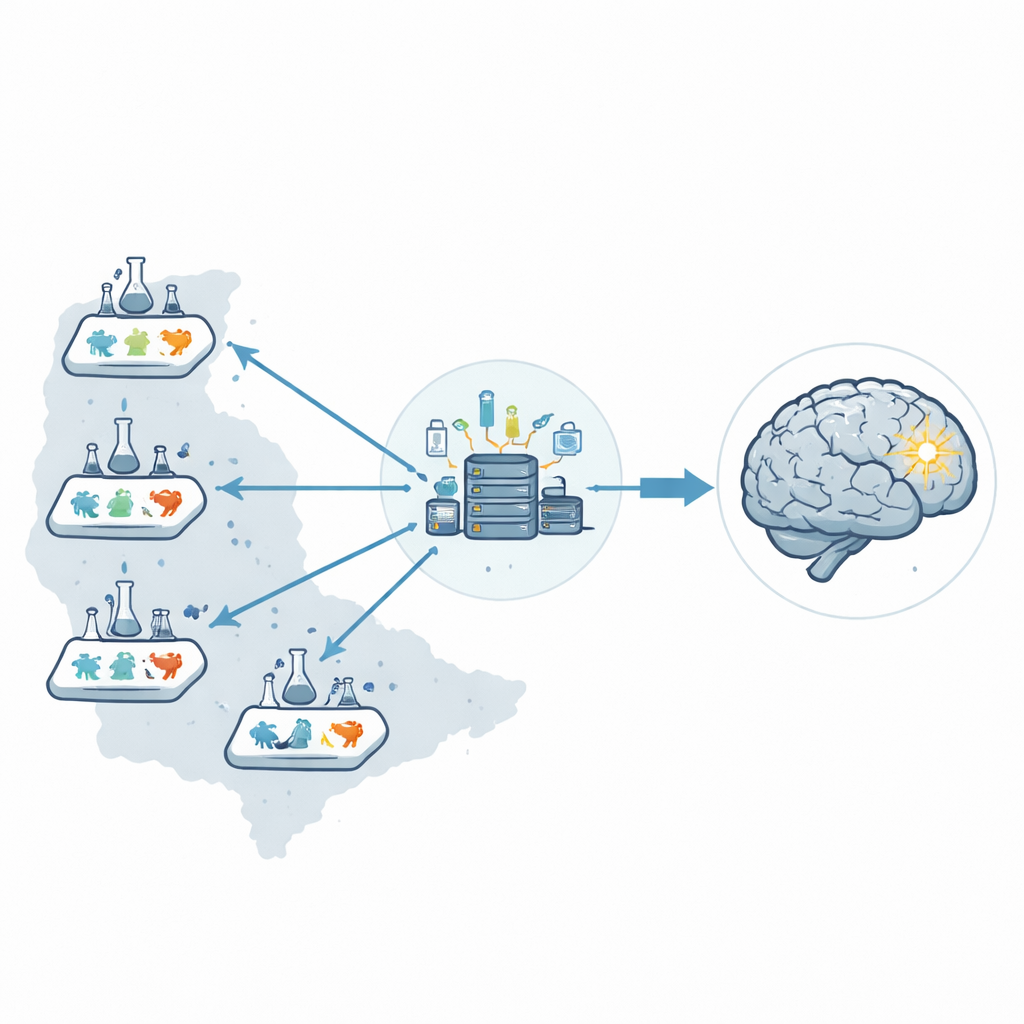
Costruire una rete invece di un singolo laboratorio
Invece di fare affidamento su un unico laboratorio, i ricercatori hanno creato una rete preclinica di sei laboratori negli Stati Uniti, chiamata Stroke Preclinical Assessment Network. Un centro di coordinamento centrale ha gestito l’intera operazione: spedendo fiale di farmaco codificate, assegnando i trattamenti in modo casuale, ricevendo tutti i dati ed eseguendo le analisi statistiche. Separando questi ruoli dalle persone che eseguivano gli interventi chirurgici o valutavano gli esiti, hanno ridotto la probabilità che le aspettative umane influenzassero in modo sottile i risultati.
Mettere in pratica equità e occultamento
Per imitare le regole di un buon trial clinico, ogni animale è stato arruolato, etichettato e tracciato dal momento in cui è arrivato in laboratorio. I trattamenti erano nascosti in fiale identiche così che i chirurghi non potessero distinguere i farmaci reali dai placebo durante l’induzione dell’ictus e la somministrazione della terapia. Un piano di randomizzazione strutturato ha garantito che maschi e femmine, diversi modelli di ictus e tutti e sei i siti contribuissero in modo equilibrato a ciascun gruppo di trattamento. Anche se un animale moriva o una procedura falliva, rimaneva registrato in modo che le perdite non potessero essere ignorate silenziosamente, contribuendo a evitare bias nascosti.
Testare i trattamenti in modelli di ictus realistici
La rete ha utilizzato cinque diversi modelli di roditori che insieme catturavano aspetti importanti dell’ictus umano, inclusi età, ipertensione e obesità indotta dalla dieta. L’ictus è stato indotto nello stesso modo in tutti i siti bloccando brevemente una grande arteria cerebrale e poi ripristinando il flusso sanguigno—simile alle moderne procedure di rimozione del coagulo negli esseri umani. Gli animali hanno ricevuto uno dei sei trattamenti protettivi candidati o un controllo corrispondente. Il team li ha poi seguiti con semplici test di movimento, come la capacità di svoltare in un angolo o camminare su una griglia, e con scansioni cerebrali per misurare l’estensione della lesione nell’arco di 30 giorni.
Valutazioni in cieco, dati condivisi e statistiche intelligenti
Per mantenere imparziali le valutazioni, i test comportamentali sono stati registrati in video e caricati in un archivio centrale. Questi video, privati di qualsiasi informazione identificativa, sono stati inviati a valutatori formati in altri laboratori, che li hanno valutati senza sapere quale trattamento avesse ricevuto l’animale o in quale sito fosse stato testato. Le immagini di risonanza magnetica sono state elaborate tramite una pipeline di analisi automatizzata che segmentava il cervello e l’area di lesione con un intervento umano minimo. Tutti i risultati sono confluiti in un disegno statistico multi-braccio e multi-fase che permetteva di testare diversi trattamenti in parallelo: i candidati deboli o chiaramente inefficaci potevano essere scartati precocemente, mentre quelli promettenti proseguivano alle fasi successive. 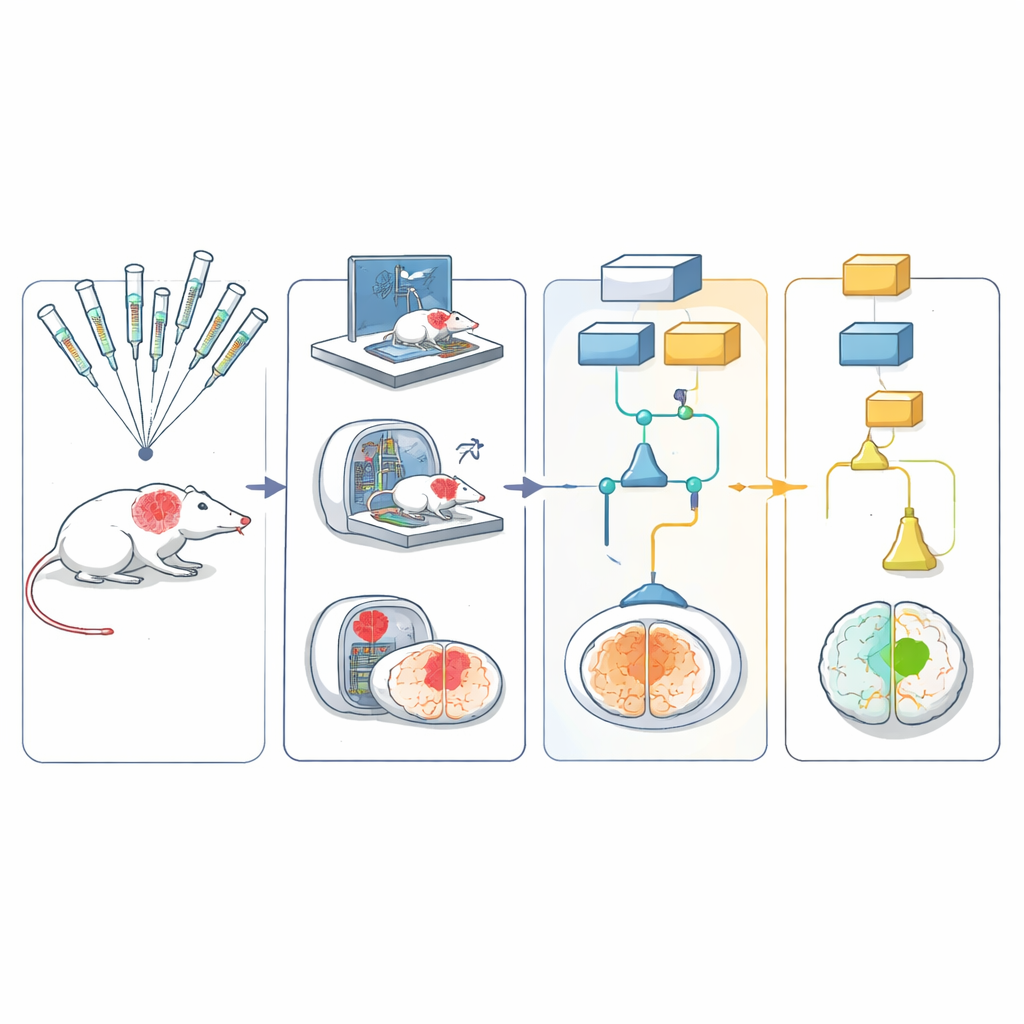
Cosa hanno mostrato i risultati sulle terapie per l’ictus
Attraverso quattro fasi e 2.615 animali, il sistema si è dimostrato praticabile anche durante le interruzioni causate dalla pandemia di COVID-19. I metodi hanno mantenuto costantemente bilanciati i gruppi di trattamento, minimizzato gli errori di dosaggio e mostrato un miglioramento della qualità dei dati man mano che i siti acquisivano esperienza. Alla fine, cinque dei sei trattamenti sono stati esclusi, mentre uno—l’acido urico, un catturatore di radicali liberi—ha raggiunto la soglia prefissata per un beneficio. Allo stesso tempo, il lavoro ha messo in luce i limiti di alcuni modelli popolari, come i tassi di mortalità molto elevati nei topi anziani, suggerendo che potrebbero non essere pratici o realistici per studi futuri.
Visione d’insieme: un modello per una scienza preclinica più affidabile
Per il lettore non specialista, il messaggio chiave è che il modo in cui testiamo i trattamenti negli animali conta tanto quanto ciò che testiamo. Importando le salvaguardie dei moderni trial clinici—randomizzazione, cieco, rendiconto completo di ogni soggetto e statistiche accurate—nella ricerca su animali, questa rete dimostra che gli studi iniziali possono essere allo stesso tempo più rigorosi ed efficienti. Il manuale dettagliato che forniscono può essere adattato ad altre malattie, offrendo un percorso verso risultati di laboratorio che resistono alla replicazione e che danno a medici, pazienti e finanziatori maggiore fiducia che una terapia abbia realmente possibilità di funzionare in clinica.
Citazione: Lamb, J., Nagarkatti, K., Diniz, M.A. et al. Methods for randomized, blinded, controlled evaluation of putative disease interventions in multilaboratory, preclinical assessment networks. Lab Anim 55, 74–82 (2026). https://doi.org/10.1038/s41684-026-01683-z
Parole chiave: ictus, trial preclinici, modelli animali, rigore della ricerca, studi multicentrici