Clear Sky Science · it
Trasgenesi mediata da PiggyBac e knockout CRISPR–Cas9 nella mosca maggiore della cera, Galleria mellonella
Un piccolo bruco con grande potenziale medico
Immaginate di testare nuovi antibiotici o studiare infezioni pericolose senza ricorrere a topi o altri mammiferi. Le larve della mosca maggiore della cera, Galleria mellonella, stanno emergendo come un sostituto economico e dal profilo etico più favorevole per tali esperimenti. Questo studio mostra come i ricercatori abbiano compiuto un passo importante dotando questi bruchi degli stessi strumenti genetici che hanno reso così potenti per la ricerca biomedica la Drosophila e i pesci zebra.
Perché questo insetto conta per la salute umana
Le larve di Galleria mellonella sono sorprendentemente efficaci nel riprodurre alcune risposte del corpo umano agli agenti patogeni. Possono essere mantenute a 37 °C—la nostra temperatura corporea—e possono essere infettate da un’ampia gamma di batteri e funghi di rilevanza medica. Quando si ammalano, il loro corpo si scurisce attraverso un processo chiamato melanizzazione, offrendo ai ricercatori un indicatore visibile dello stato di salute. Essendo invertebrati, evitano molti degli ostacoli legali ed etici legati all’uso di vertebrati e sono poco costose da allevare in grandi quantità. Le larve sono state persino trovate in grado di degradare plastiche comuni, suggerendo possibili impieghi anche nella ricerca ambientale.
Il kit genetico mancante
Nonostante questi vantaggi, le larve della mosca della cera sono state a lungo prive degli stratagemmi genetici sofisticati disponibili negli animali da laboratorio classici. Nell’ultimo decennio diversi gruppi hanno decodificato il genoma della falena e catalogato i suoi geni e proteine attivi, ma i ricercatori non potevano ancora attivare o spegnere facilmente i geni né aggiungere marcatori utili. Questa lacuna ha limitato le potenzialità del modello—forse creando animali che si illuminano quando infettati, o eliminando geni specifici per testare il loro ruolo nell’immunità. Il lavoro attuale affronta il problema adattando due potenti sistemi di ingegneria genica, noti come PiggyBac e CRISPR–Cas9, per l’uso in Galleria mellonella.
Costruire larve reporter che brillano al buio
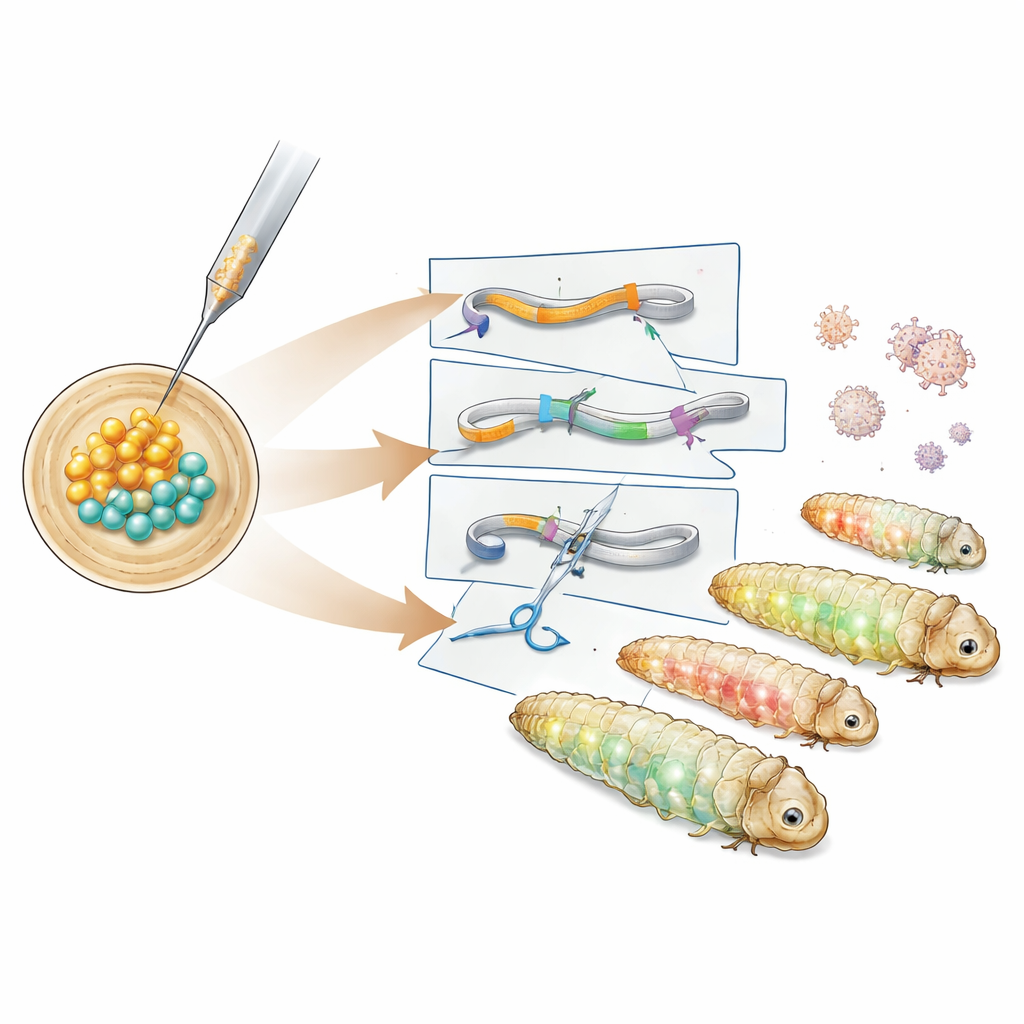
Il gruppo ha prima studiato i tempi dello sviluppo embrionale precoce della falena e ha individuato una finestra di circa sei ore dopo la deposizione delle uova durante la quale tutti i nuclei in divisione condividono ancora un citoplasma comune. Iniettare DNA in questo periodo permette al materiale genetico introdotto di raggiungere tutti i tessuti successivi, inclusi i futuri spermatozoi e ovuli. Sfruttando questa finestra, i ricercatori hanno introdotto costrutti di DNA basati sul trasposone PiggyBac, un elemento “taglia‑e‑incolla” che inserisce grandi frammenti di DNA nel genoma. Dopo aver testato diversi plasmidi helper, hanno identificato una versione contenente una variante iperattiva dell’enzima PiggyBac che ha prodotto con successo linee transgeniche. Queste larve esprimevano proteine fluorescenti verdi e rosse in tessuti corporei distinti, e l’analisi del DNA ha mostrato che il cassetto genetico si è inserito in una regione tra geni nativi priva di effetti dannosi.
Osservare le cellule e abbattere i geni
Successivamente gli autori hanno creato linee reporter più specializzate. Un costrutto ha marcato una proteina strutturale chiamata tubulina con fluorescenza verde per evidenziare lo scheletro interno della cellula, mentre un altro ha fuso un marcatore rosso a una proteina istonica che avvolge il DNA nel nucleo. Queste linee brillavano con pattern caratteristici nel tratto gastrointestinale, nel corpo adiposo, nelle ghiandole della seta e in altri tessuti, permettendo ai ricercatori di visualizzare le strutture cellulari in larve vive o fissate. Per andare oltre l’aggiunta di geni e disabilitarli realmente, il team ha usato CRISPR–Cas9. Hanno iniettato complessi proteina‑RNA preassemblati mirati al marcatore fluorescente verde in embrioni che già portavano il cassetto reporter. Molti discendenti hanno mostrato una perdita parziale o completa del segnale verde mantenendo la fluorescenza rossa negli occhi, e il sequenziamento del DNA ha confermato piccole inserzioni e delezioni nel sito di taglio previsto da CRISPR.
Dall’avanzamento tecnico all’impatto pratico
Anche se l’efficienza sia di PiggyBac sia di CRISPR in queste falene è ancora modesta rispetto ad alcuni altri insetti, gli autori delineano percorsi chiari per il miglioramento modulando promotori, varianti enzimatiche e strategie di iniezione. Anche nella forma attuale, il kit di strumenti è abbastanza potente da generare linee stabili che visualizzano componenti cellulari chiave o portano knockout genici mirati. Per i non specialisti, il quadro generale è che Galleria mellonella può ora essere ingegnerizzata quasi con la stessa flessibilità degli animali da laboratorio più noti. Ciò significa che i ricercatori possono costruire bruchi che segnalano l’infezione, modellano aspetti di malattie umane o testano nuovi farmaci in modi più rapidi, economici e più umani, riducendo potenzialmente la dipendenza dai modelli mammiferi nella biologia delle infezioni e in campi affini.
Citazione: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
Parole chiave: Galleria mellonella, modello di infezione negli invertebrati, ingegneria genetica, trasgenesi PiggyBac, knockout CRISPR