Clear Sky Science · it
Mirare l’EGFR espresso nei tumori con un anticorpo monoclonale umanizzato
Individuare le bandiere nascoste del cancro
I trattamenti oncologici spesso faticano a trovare un equilibrio fra colpire le cellule tumorali e risparmiare i tessuti sani. Questo articolo descrive un nuovo anticorpo ingegnerizzato in laboratorio, denominato A10, in grado di distinguere le cellule cancerose che portano una forma particolare di un recettore per segnali di crescita dalle cellule normali. Focalizzandosi su una conformazione che compare prevalentemente quando questo recettore è alterato o sovraespresso sulle cellule tumorali, A10 apre la strada a terapie potenti ma più selettive rispetto a molte opzioni attuali.
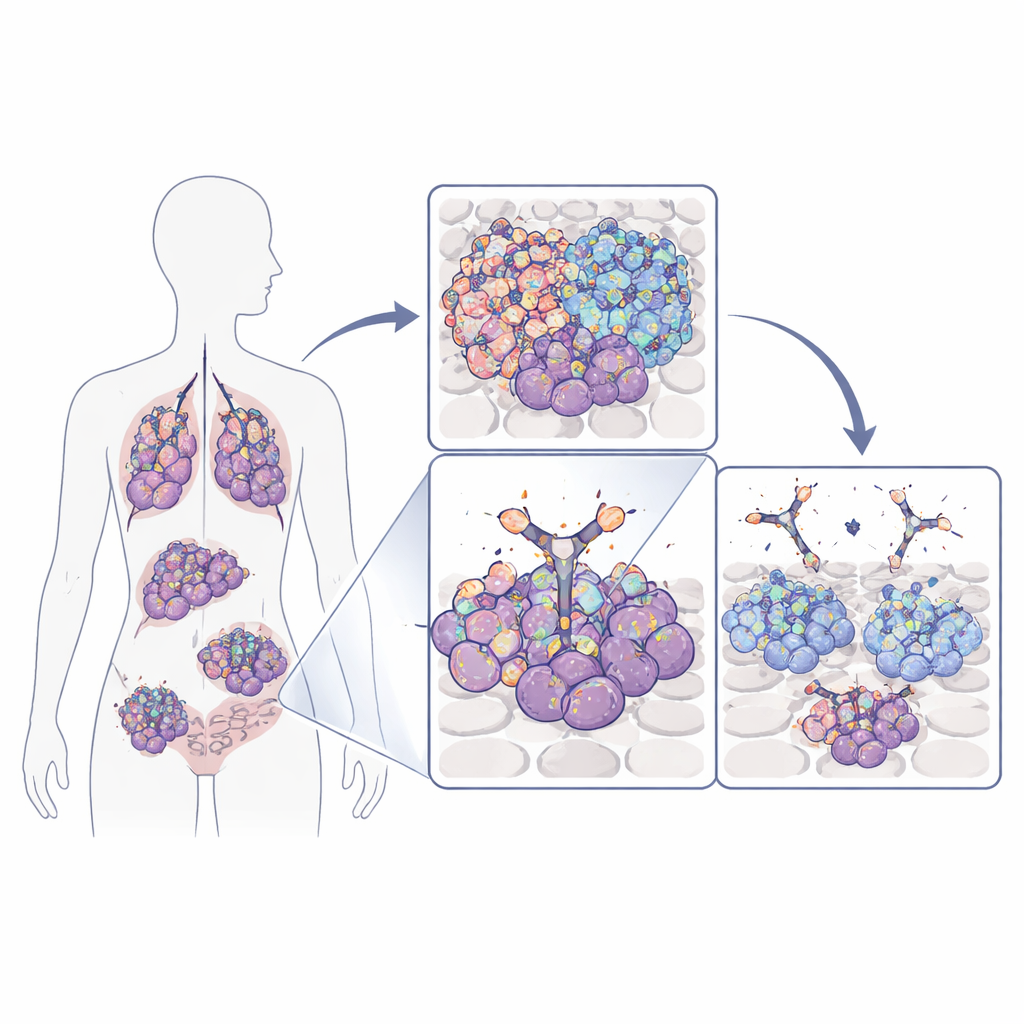
Perché questo interruttore di crescita è importante
Molti tumori, compresi quelli aggressivi del cervello, del polmone, della mammella e del colon-retto, dipendono da una proteina di superficie chiamata recettore del fattore di crescita epidermico (EGFR) per crescere e sopravvivere. Le cellule tumorali possono potenziare questo recettore amplificandone il gene, mutandolo o producendo una versione accorciata e permanentemente attiva nota come EGFRvIII. I farmaci standard che bloccano l’EGFR spesso colpiscono sia le cellule cancerose sia i tessuti normali, perché riconoscono porzioni del recettore presenti ovunque. Il gruppo che ha condotto questo studio si è invece concentrato su un piccolo anello dell’EGFR che risulta chiaramente esposto soprattutto nelle cellule cancerose—o perché l’EGFR è presente in numero anormalmente elevato o perché il recettore è troncato in EGFRvIII. Quel loop agisce come una “bandiera” specifica del cancro che, in linea di principio, può essere bersagliata in modo molto più sicuro.
Trasformare un anticorpo murino in un farmaco umano
I ricercatori avevano in precedenza scoperto un anticorpo di topo, 40H3, che riconosceva questo loop esposto sull’EGFR espresso nei tumori. Gli anticorpi murini, tuttavia, possono scatenare reazioni immunitarie se somministrati ripetutamente ai pazienti. Per superare questo limite, il team ha impiegato metodi di ingegneria proteica per innestare i segmenti chiave di legame di 40H3 su impalcature di anticorpi umani, generando quattordici candidati “umanizzati” più una molecola di riferimento chimerica. Testando queste varianti su cellule tumorali che sovraproducono EGFR, tre versioni si sono legate particolarmente bene, e una—A10—si è distinta come il legante più forte pur ignorando le cellule normali con livelli modesti di EGFR. Su un ampio pannello di linee cellulari tumorali con diverse mutazioni e numeri di copie di EGFR, A10 ha mostrato costantemente un legame superiore rispetto all’anticorpo murino originale e ha mantenuto una forte preferenza per le cellule maligne.
Vedere come l’anticorpo afferra il suo bersaglio
Per capire perché A10 sia così selettivo, il team ha risolto una struttura 3D ad alta risoluzione della parte attiva dell’anticorpo legata al loop dell’EGFR. Il loop si piega in una stretta forcella stabilizzata da un ponte disolfuro, e A10 avvolge questa conformazione in una scanalatura formata tra i suoi due “bracci”, con numerosi contatti carichi che la bloccano in posizione. Confrontando questa struttura con le conformazioni note della molecola completa di EGFR è emerso un punto chiave: sia nella forma inattiva “tethered” sia nella forma attiva dimera dell’EGFR normale, il loop è in gran parte sepolto o parzialmente schermato da domini adiacenti. Ciò significa che A10 non può facilmente raggiungere il suo sito di legame sui recettori tipici espressi a livelli modesti. Al contrario, nella variante tumorale EGFRvIII la parte anteriore del recettore è assente, lasciando il loop altamente esposto e accessibile. I dati suggeriscono che A10 riconosce principalmente l’EGFR in determinate forme transitorie e nelle forme sovraffollate o troncate che si manifestano preferenzialmente sulle cellule tumorali.
Armare l’anticorpo per uccidere le cellule tumorali
Riconoscere una bandiera specifica del tumore è utile di per sé, ma i ricercatori sono andati oltre trasformando A10 in un coniugato anticorpo‑farmaco (ADC). Hanno legato chimicamente un potente composto citotossico, la monometil auristatina E (MMAE), ad A10 usando un linker che può essere tagliato all’interno delle cellule. Questo ADC A10‑MMAE si è legato alle cellule tumorali altrettanto bene quanto l’anticorpo non coniugato. Nei test in vitro su molte linee cellulari, l’ADC è stato più efficace contro i tumori con livelli molto elevati di EGFR o con EGFRvIII, dove A10 aveva abbondanti siti di legame. In queste cellule, piccole quantità del coniugato erano sufficienti a innescare la morte cellulare. Le linee tumorali con meno bersagli per A10 o con resistenza intrinseca alla MMAE sono state meno influenzate, e le fibroblaste normali con EGFR wild‑type sono rimaste indenni nonostante fossero sensibili alla MMAE libera. I risultati mostrano che la combinazione di legame selettivo e rilascio intracellulare del farmaco può concentrare nettamente la tossicità sulle cellule cancerose.
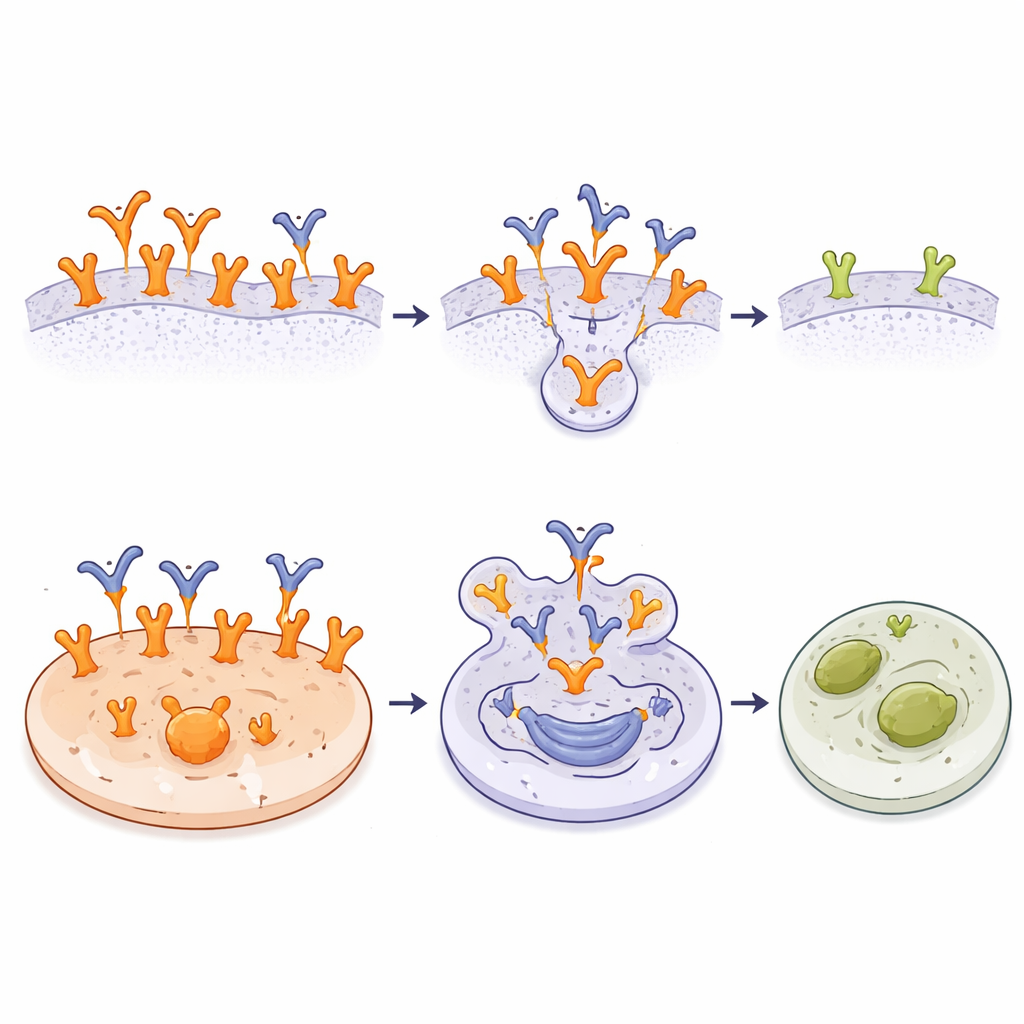
Cosa potrebbe significare per la cura del cancro in futuro
In termini semplici, questo lavoro dimostra che è possibile costruire un anticorpo che “vede” l’EGFR solo quando assume l’aspetto e il comportamento di un recettore che guida il cancro, ignorando in gran parte la sua forma quotidiana nei tessuti sani. Mappando esattamente come A10 afferra un loop nascosto dell’EGFR e dimostrando che un coniugato a base di A10 può uccidere efficacemente le cellule tumorali ricche di recettori risparmiando le cellule normali, lo studio fornisce una solida base per sviluppare terapie mirate più sicure. Se questi risultati si tradurranno nei pazienti, trattamenti futuri basati su A10 potrebbero veicolare farmaci potenti direttamente ai tumori dipendenti da EGFR lasciando il resto del corpo in gran parte intatto.
Citazione: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
Parole chiave: EGFR, coniugato farmaco‑anticorpo, terapia oncologica mirata, glioblastoma, EGFRvIII