Clear Sky Science · it
Approfondimenti strutturali e meccanicistici sul targeting degli integrine α2β1 e α5β1 mediante vescicole extracellulari bioingegnerizzate originate da cellule di cancro polmonare
I messaggeri nascosti del cancro
Il cancro polmonare viene spesso scoperto in fase avanzata, quando le opzioni terapeutiche sono limitate. Un approccio promettente consiste nel veicolare i farmaci solo alle cellule tumorali, risparmiando il tessuto sano. Questo studio esplora un minuscolo sistema di consegna naturale—le vescicole extracellulari, o EV—che le cellule tumorali usano già per inviare segnali. Riprogettando queste vescicole con un breve tag mirato, i ricercatori mostrano come esse possano agganciarsi a siti di ancoraggio specifici sulle cellule tumorali, gettando le basi per terapie oncologiche più precise e meno tossiche.
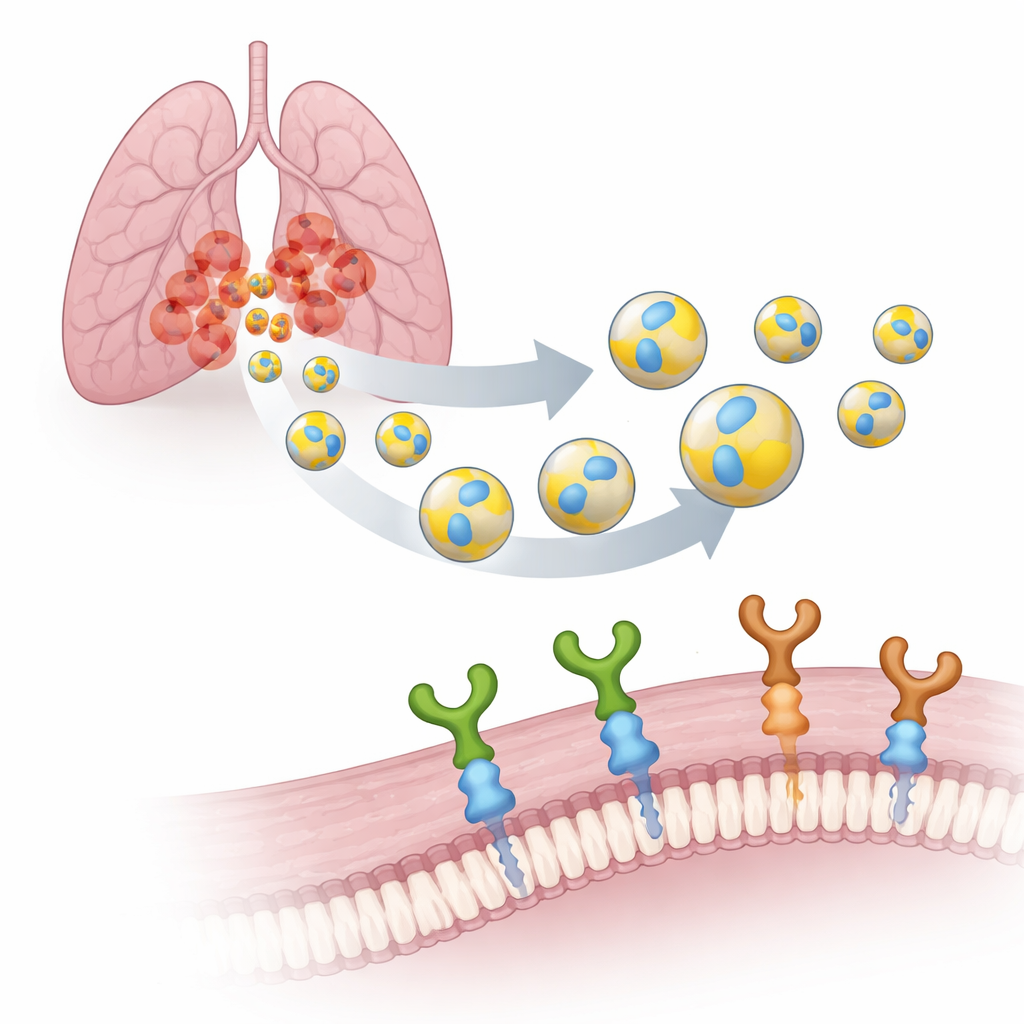
Trasformare pacchetti naturali in corrieri intelligenti
Ogni cellula del nostro corpo rilascia EV: bolle nanoscalari circondate da una membrana, un po’ come microscopiche bolle di sapone. Poiché sono prodotte dalle nostre stesse cellule, le EV sono biodegradabili, attraversano con facilità le barriere biologiche e sono meno propense a provocare effetti collaterali rispetto ai vettori sintetici. Il gruppo si è concentrato su EV prodotte da cellule umane di cancro polmonare (A549) e ha decorato la loro superficie con un piccolo tag di sette unità chiamato PTHTRWA. Esperimenti precedenti avevano dimostrato che questo tag indirizza le EV verso le cellule di cancro polmonare nei topi, legandosi molto più saldamente alle cellule tumorali rispetto a quelle polmonari normali e mostrando bassa tossicità.
Trovare i giusti porti d’attracco sulle cellule tumorali
Per trasformare queste vescicole etichettate in strumenti realmente mirati, i ricercatori dovevano identificare quali “porti” sulle cellule tumorali riconoscono. Hanno esaminato due recettori di superficie correlati, le integrine α2β1 e α5β1. Questi sono uncini molecolari che aiutano le cellule ad aderire all’ambiente circostante e a trasmettere segnali verso l’interno. Nei tumori polmonari, α5β1 è fortemente associata a comportamento aggressivo, diffusione e scarsa sopravvivenza, mentre α2β1 è stata collegata alla resistenza alla chemioterapia. Utilizzando una tecnica sensibile chiamata risonanza plasmonica di superficie, il gruppo ha confrontato quanto fortemente le EV decorate con PTHTRWA si legano a entrambe le integrine. Hanno scoperto che le vescicole prive del tag interagivano a malapena, mentre le EV etichettate formavano complessi stretti e stabili con entrambi i recettori in condizioni prossime a quelle fisiologiche.
Ingresso ravvicinato nell’abbraccio molecolare
Per capire cosa accade atomo per atomo quando il tag incontra le integrine, i ricercatori si sono rivolti a simulazioni al computer. Hanno costruito modelli tridimensionali del peptide legato a regioni chiave delle integrine e hanno lasciato evolvere questi sistemi in acqua virtuale per centinaia di nanosecondi. I calcoli hanno mostrato che PTHTRWA si adatta perfettamente in una gola poco profonda sul recettore α2β1, formando una rete di legami idrogeno e contatti idrofobici che stabilizzano il complesso. In modo cruciale, il legame favoriva una conformazione più “aperta” del recettore—la sua forma ad alta affinità e pronta a trasmettere segnali—piuttosto che lo stato chiuso di riposo. Testando versioni leggermente modificate del tag, hanno osservato che piccole modifiche chimiche a un’estremità possono rimodellare sottilmente l’orientamento del peptide nella gola e la sua preferenza di legame per un’integrina rispetto all’altra.
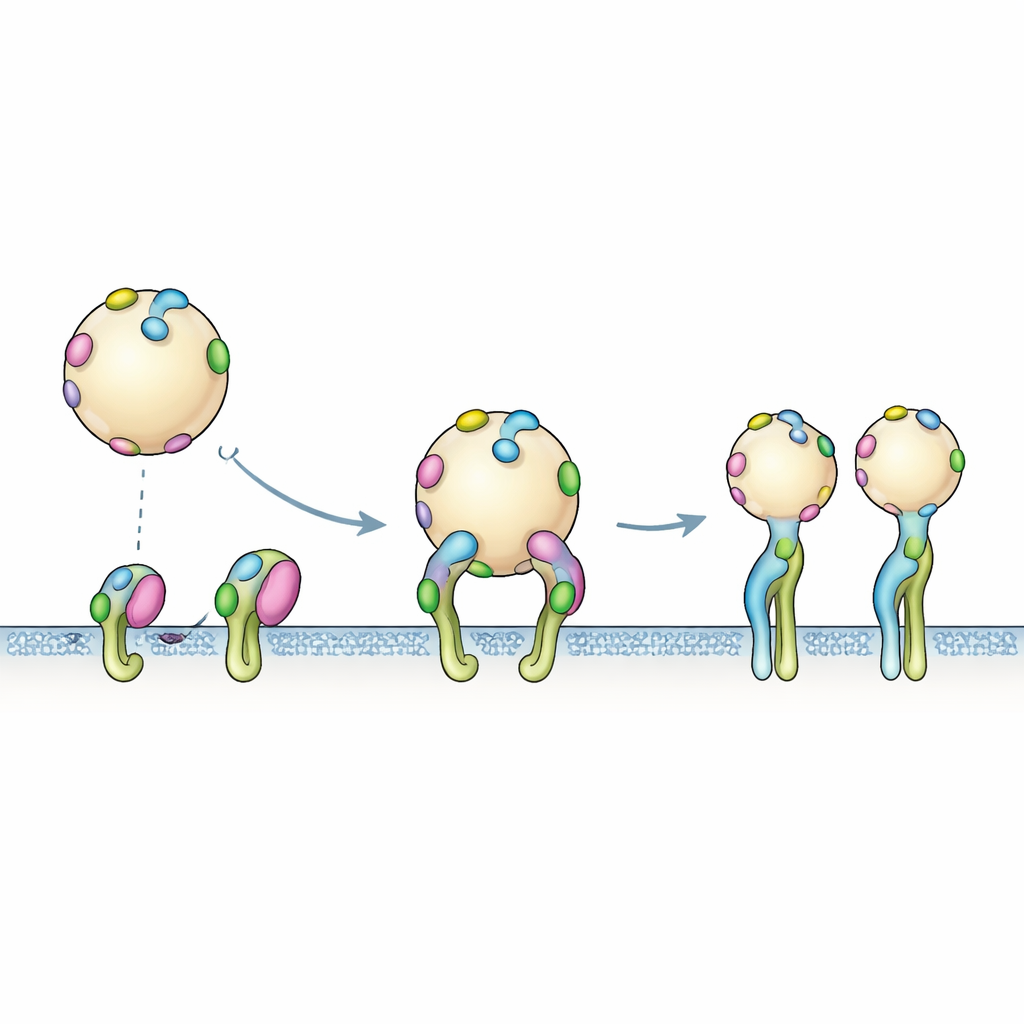
Da tag singoli a prese multivalenti
I modelli computazionali catturano un tag che tocca un recettore alla volta, ma la superficie reale delle EV è punteggiata da molte copie di PTHTRWA. Gli esperimenti di legame riflettevano questa realtà multivalente: quando una vescicola etichettata si avvicina a una patch di integrine, più tag possono impegnarsi contemporaneamente. I dati del sensore si adattavano meglio a un processo in due fasi. Prima, la vescicola si ancora brevemente tramite incontri rapidi e reversibili. Poi avviene un riorganizzazione più lenta in cui le integrine passano alla forma aperta e la presa complessiva si rafforza. Questo meccanismo cooperativo a molte mani spiega perché la forza di legame apparente delle vescicole intere è maggiore di quella prevista da un singolo tag isolato.
Cosa potrebbe significare per i trattamenti futuri
In termini semplici, lo studio dimostra che le EV armate con il tag PTHTRWA possono riconoscere selettivamente integrine iperattive nel cancro polmonare e che lo fanno spingendo questi recettori verso una forma aperta e fortemente legata. Mappando queste interazioni in dettaglio, i ricercatori forniscono regole di progetto per vettori di nuova generazione basati su vescicole che potrebbero consegnare farmaci, agenti di imaging o altri carichi direttamente alle cellule maligne, ignorando in gran parte il tessuto sano. Sebbene siano necessari ulteriori studi in animali e nell’uomo, questa strategia di targeting delle integrine avvicina la visione di una medicina oncologica personalizzata basata sulle EV a un orizzonte più concreto.
Citazione: Nowicka, A.M., Żołek, T., Kowalczyk, A. et al. Structural and mechanistic insights into α2β1 and α5β1 integrin targeting by bioengineered extracellular vesicles originating from lung cancer cells. Sci Rep 16, 10833 (2026). https://doi.org/10.1038/s41598-026-46071-2
Parole chiave: cancro polmonare, vescicole extracellulari, integrine, consegna mirata di farmaci, simulazioni molecolari