Clear Sky Science · it
Prova di concetto per l’estrazione di DNA libera da cellule dal plasma basata su un sistema acquoso a due fasi per applicazioni di biopsia liquida
Perché un esame del sangue è importante per il cancro e altre malattie
Molti test medici moderni cercano minuscoli frammenti di DNA che fluttuano liberamente nel nostro sangue. Questi pezzi, noti come DNA libero da cellule, possono rivelare se un tumore sta rilasciando materiale genetico, se un organo trapiantato viene rigettato o come procede una gravidanza. Ma poiché questi frammenti di DNA sono scarsi, corti e mescolati in una zuppa di proteine e altre molecole, isolarli in modo pulito e rapido è sorprendentemente difficile. Questo studio presenta un nuovo metodo più semplice per estrarre questi frammenti dal plasma sanguigno utilizzando una separazione delicata a base d’acqua, che potrebbe rendere i test avanzati di “biopsia liquida” più accessibili e meno costosi.
La sfida di pescare pezzi di DNA minuscoli
I medici e i ricercatori usano le biopsie liquide per leggere indizi genetici da un semplice prelievo di sangue invece di asportare tessuto. Il problema è che il DNA libero da cellule nel plasma è di solito presente a solo poche decine di nanogrammi per millilitro ed è frammentato in pezzi corti. Una piccola frazione di questo materiale può provenire da un tumore o da un organo trapiantato, quindi ogni frammento conta. I kit di estrazione standard catturano il DNA facendolo aderire a superfici di silice in presenza di sali forti, seguiti da diversi passaggi di lavaggio e centrifugazione. Questi kit funzionano bene ma richiedono tempo, attrezzature speciali e possono essere costosi. Possono inoltre avere difficoltà a recuperare i frammenti più corti e possono portare con sé lunghe porzioni di DNA genomico normale, che possono mascherare segnali rari legati a malattie.
Un trucco a due strati d’acqua per catturare il DNA
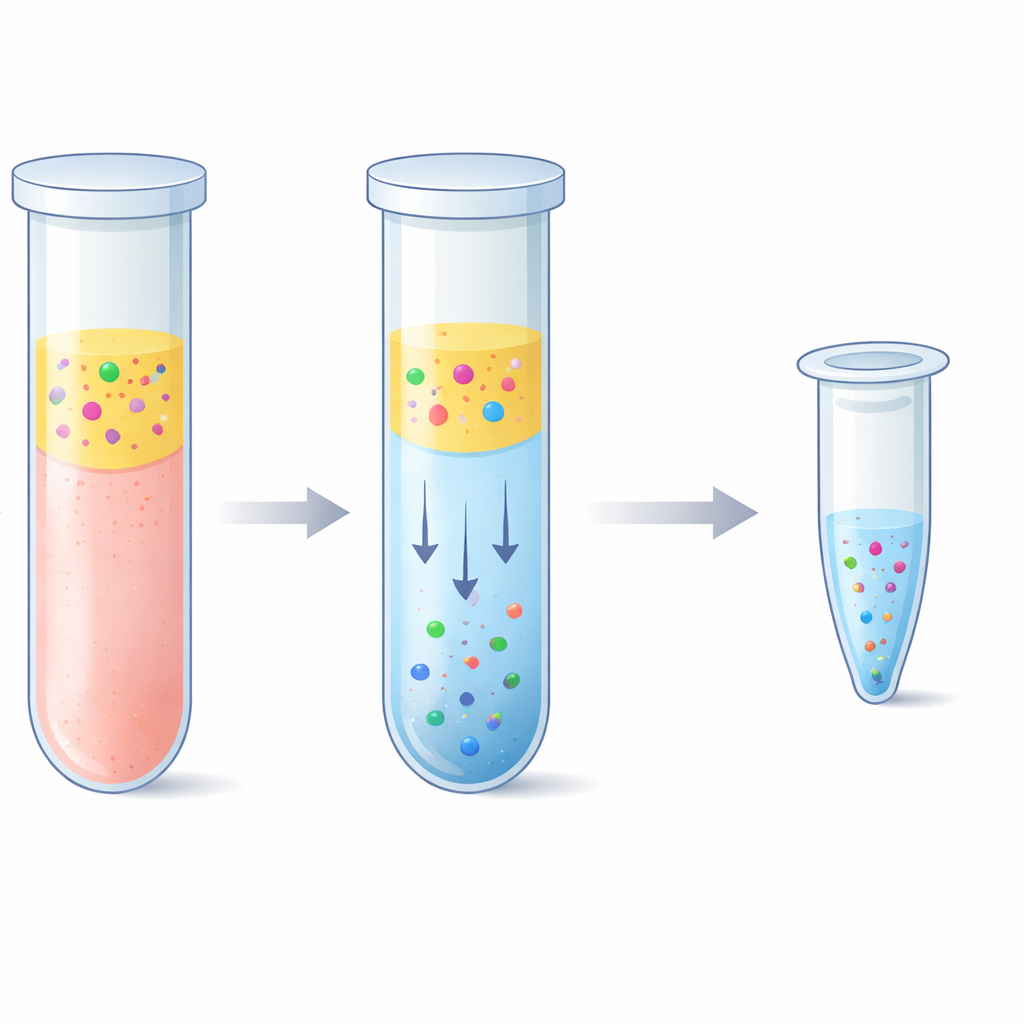
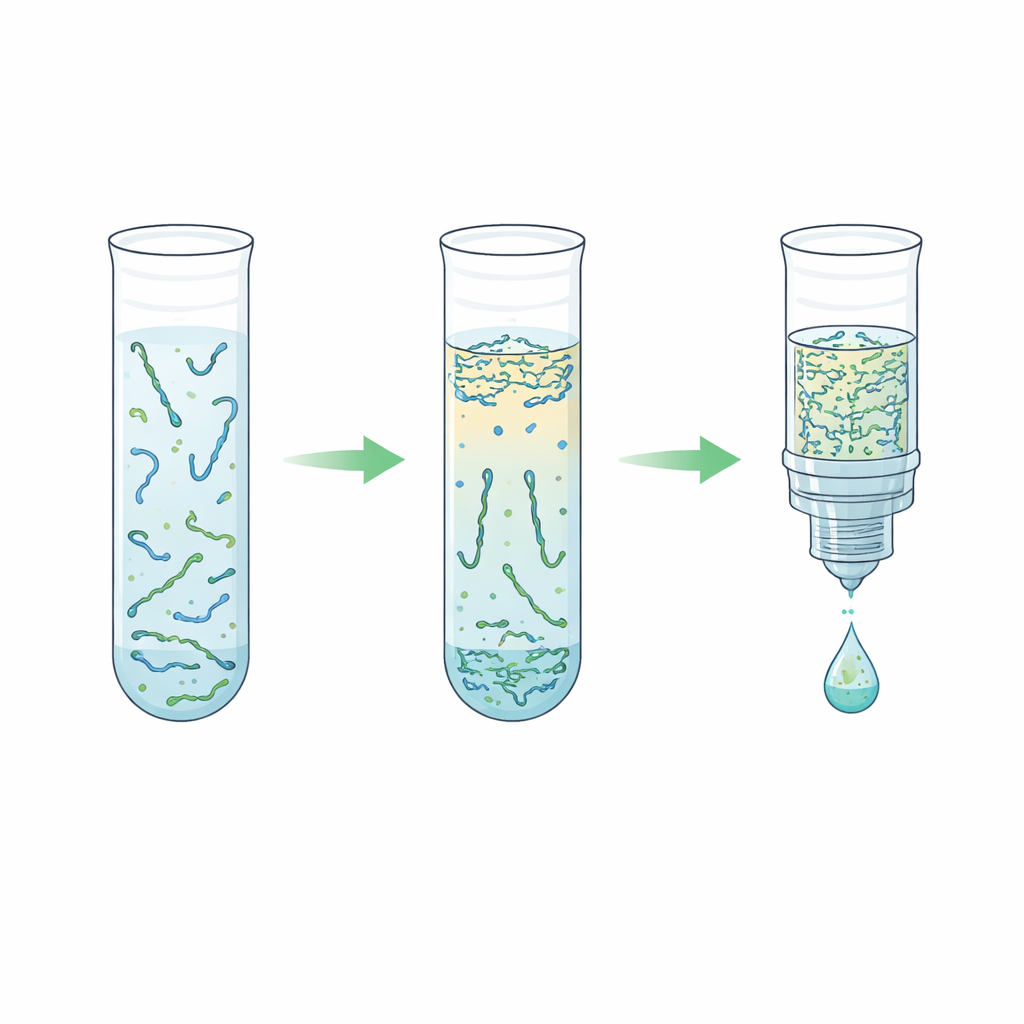
Il gruppo ha esplorato un’alternativa basata su un “sistema acquoso a due fasi” — in termini semplici, due liquidi ricchi d’acqua che non si mescolano completamente, come olio e aceto ma entrambi per lo più costituiti da acqua. Combinando il plasma con un polimero chiamato polietilenglicole e semplici sali fosfato, la miscela si separava naturalmente in uno strato superiore e uno inferiore. Sorprendentemente, i frammenti di DNA corti preferivano nettamente lo strato inferiore ricco di sali, mentre la maggior parte delle proteine del sangue e i lunghi filamenti di DNA rimanevano nello strato superiore o all’interfaccia. I ricercatori hanno messo a punto con cura la ricetta in modo che questo strato inferiore rimanesse sufficientemente piccolo da concentrare il DNA ma abbastanza delicato da non danneggiarlo. Hanno quindi abbinato questo passaggio a una purificazione di “eluizione inversa”, che spinge lo strato inferiore salino attraverso una matrice porosa per rimuovere il sale e ridurre il volume finale, ottenendo una soluzione di DNA più pulita e concentrata.
Rifinire il processo per l’uso nel mondo reale
Attraverso molteplici cicli di test, gli autori hanno regolato l’equilibrio tra polimero e sale, le velocità di centrifugazione, i volumi e i passaggi opzionali di lisi che spezzano i complessi proteina–DNA. Hanno scoperto che l’aumento del contenuto di polimero lungo certe linee di composizione raddoppiava la concentrazione di DNA senza compromettere il recupero, e che un condizionamento più aggressivo nella fase di eluizione inversa quadruplicava approssimativamente la concentrazione rispetto al loro lavoro precedente. Sorprendentemente, hanno scoperto che saltare la lisi aggressiva prima della separazione a due fasi spesso funzionava meglio; la lisi tendeva a disturbare le fasi e a ridurre la resa. Un flusso di lavoro semplificato e in gran parte privo di lisi ha rimosso circa il 99,7% delle proteine plasmatiche recuperando fino a circa due terzi del DNA corto in ingresso in un volume quattro volte più piccolo, il tutto in circa dieci minuti di tempo di lavorazione totale e solo un paio di minuti di lavoro operativo diretto.
Come si confronta il nuovo metodo
I ricercatori hanno confrontato il loro approccio con un kit commerciale a base di silice ampiamente usato. Il kit standard produceva rese totali di DNA leggermente più elevate e una concentrazione maggiore perché eluiva in volumi molto piccoli. Tuttavia, il metodo a due fasi ha mostrato recuperi costanti sopra il 60% per una gamma di input di DNA, anche partendo da quantità molto piccole, e richiedeva molti meno passaggi manuali e meno attrezzature. È importante che il nuovo processo funzionasse anche come un filtro integrato per la lunghezza dei frammenti: arricchiva DNA corto simile al DNA libero da cellule escludendo in gran parte i lunghi filamenti che possono provenire da cellule sanguigne rotte. Test con PCR quantitativa hanno mostrato che gli estratti puliti non inibivano l’amplificazione successiva. Quando il team ha utilizzato un campione di riferimento commerciale contenente mutazioni note correlate al cancro, il DNA recuperato con il loro metodo è stato convertito in librerie di sequenziamento, sequenziato su un sequenziatore ad alto rendimento e ha permesso di rilevare tutte le varianti attese alle frequenze corrette.
Che cosa potrebbe significare per i futuri esami del sangue
In termini semplici, questo lavoro dimostra che una separazione relativamente semplice a base d’acqua può sostituire una chimica più complessa su superfici solide per la preparazione del DNA libero da cellule dal plasma. Sebbene il nuovo metodo attualmente renda leggermente meno DNA rispetto ai kit commerciali di punta, offre una lavorazione rapida, una forte rimozione di proteine indesiderate e di DNA lungo, e compatibilità immediata con PCR e sequenziamento di nuova generazione. Se ulteriormente validato su campioni clinici reali e perfezionato per l’automazione, questo approccio potrebbe abbassare i costi e semplificare i flussi di lavoro di laboratorio, aiutando a portare test del sangue basati sulla genetica per cancro, trapianto e altre condizioni a un uso più ampio nella pratica quotidiana.
Citazione: Meutelet, R., Buerfent, B.C., Hess, T. et al. Proof of concept for aqueous two-phase system-based extraction of cell-free DNA from plasma for liquid biopsy applications. Sci Rep 16, 11232 (2026). https://doi.org/10.1038/s41598-026-45585-z
Parole chiave: biopsia liquida, DNA libero da cellule, test del sangue per il cancro, estrazione del DNA, sequenziamento di nuova generazione