Clear Sky Science · it
Interferone-β e FTY720 attenuano l’infiammazione progressiva del SNC tramite il segnale astrocitario associato a SOCS1
Perché questa ricerca è importante per le persone con sclerosi multipla
Per molte persone con sclerosi multipla (SM), la paura maggiore non sono tanto le ricadute iniziali quanto la perdita lenta e costante di funzioni che può seguire. In questa fase avanzata e progressiva, il danno all’interno del cervello e del midollo spinale continua anche quando i farmaci standard che agiscono sul sistema immunitario nel sangue stanno facendo il loro lavoro. Questo studio esplora un modo per raggiungere quell’infiammazione “nascosta” combinando una pillola anti‑SM già esistente con una forma di un farmaco di lunga data somministrata direttamente verso il cervello.
Una malattia cerebrale a lungo termine con poche opzioni
La SM è una malattia autoimmune in cui le cellule immunitarie dell’organismo attaccano l’isolamento delle fibre nervose, causando problemi visivi, debolezza e altri sintomi neurologici. Nelle fasi iniziali i sintomi tendono a comparire e poi attenuarsi. Nel tempo molti pazienti entrano in una fase progressiva caratterizzata da una disabilità graduale e spesso irreversibile. In questa fase la barriera emato‑encefalica diventa più difficile da attraversare per i farmaci e l’attività dannosa delle cellule residenti del cervello chiamate glia — in particolare astrociti e microglia — assume un ruolo sempre più rilevante. I trattamenti attuali, che agiscono per lo più bloccando le cellule immunitarie nel sangue, offrono solo un aiuto limitato una volta che questa fase è stabilita.
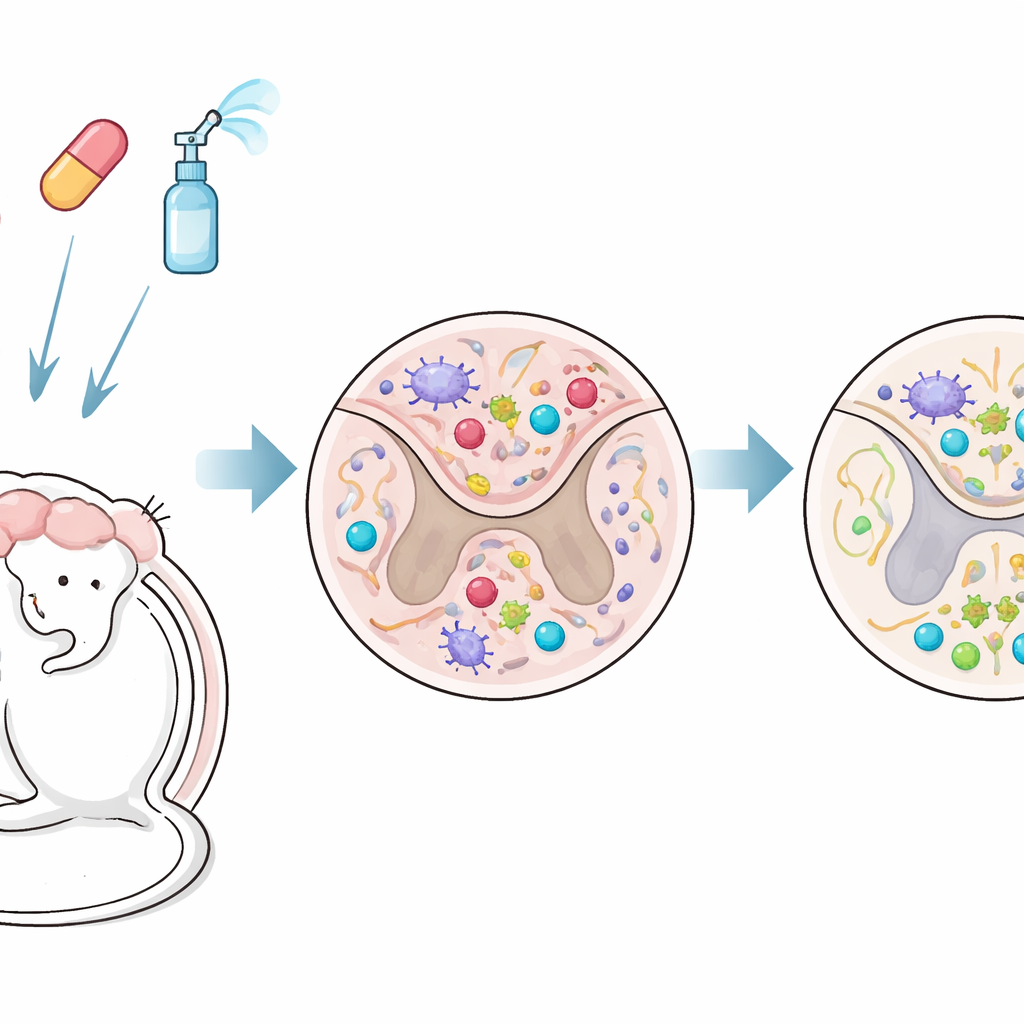
Abbinare due farmaci per raggiungere sangue e cervello
I ricercatori hanno testato un trattamento combinato in un modello murino che imita da vicino la SM progressiva. Un farmaco, il fingolimod (FTY720), è una compressa che intrappola le cellule immunitarie nei linfonodi e può anche entrare nel cervello. L’altro, l’interferone‑beta, è una terapia per la SM usata da tempo che normalmente agisce al di fuori del cervello perché non attraversa facilmente la barriera emato‑encefalica. In questo studio l’interferone‑beta è stato somministrato per via intranasale — attraverso il naso — in modo da eludere questa barriera e raggiungere il sistema nervoso centrale più direttamente. Il trattamento è iniziato dopo che i topi avevano già sviluppato problemi neurologici cronici, riflettendo una fase in cui il danno è tipicamente più difficile da invertire.
Meno danni e attività immunitaria più calma
I topi che hanno ricevuto il trattamento combinato fingolimod più interferone‑beta intranasale hanno ottenuto risultati migliori rispetto a quelli trattati solo con fingolimod. I loro punteggi di malattia sono migliorati di più e alcuni deficit neurologici preesistenti si sono attenuati. Quando gli scienziati hanno esaminato i midolli spinali, hanno riscontrato più mielina preservata, meno segni di danno assonale e meno cellule immunitarie infiltranti. Le cellule T e i monociti pro‑infiammatori sono diminuiti e le cellule T rimanenti producevano meno molecole messaggere dannose come interferone‑gamma e IL‑17. È importante che la terapia combinata abbia anche attenuato i segnali nocivi provenienti da astrociti e microglia, le cellule gliali che contribuiscono a modellare l’ambiente locale all’interno di cervello e midollo spinale.
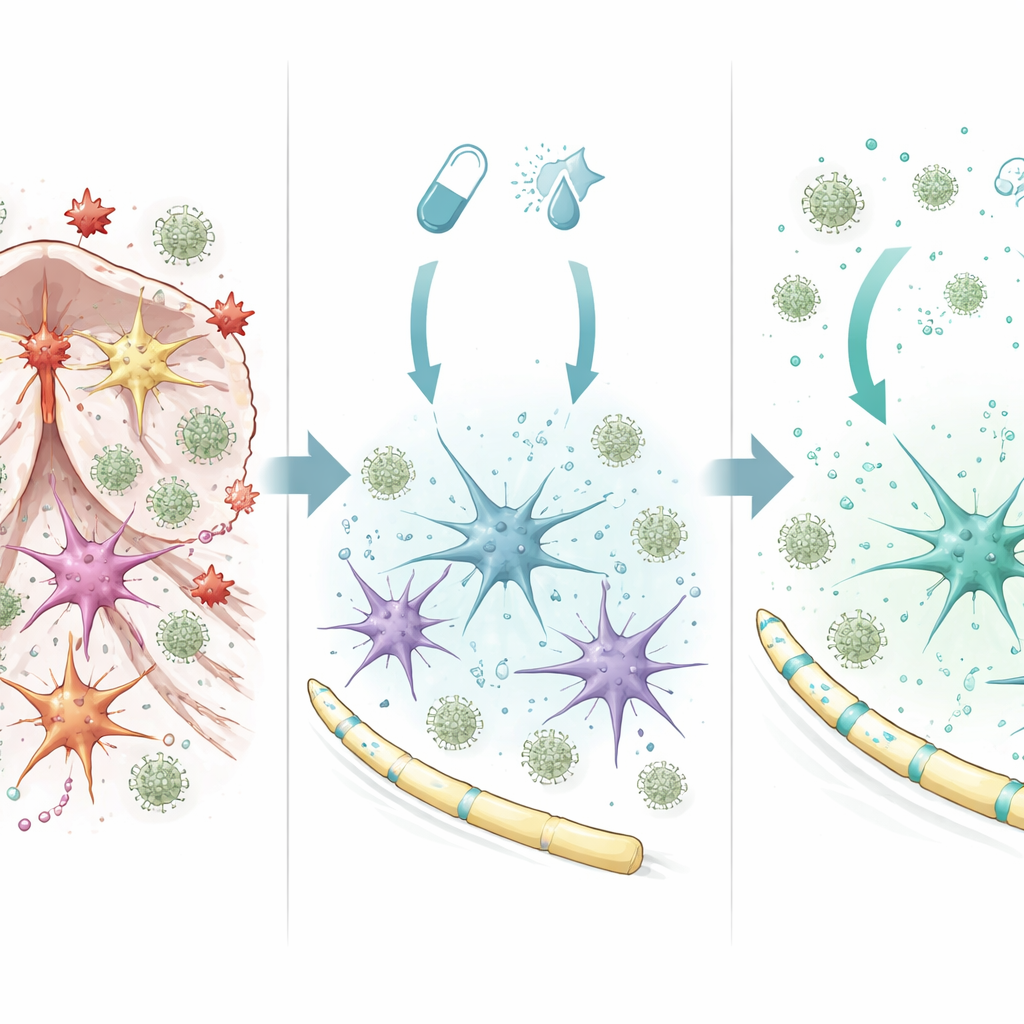
Gli astrociti passano da comportamenti dannosi a protettivi
Per comprendere come agisse la terapia combinata all’interno del cervello, il gruppo ha studiato astrociti purificati in coltura. Quando esposti a fingolimod più interferone‑beta, gli astrociti hanno attivato un ampio insieme di geni legati alla sopravvivenza cellulare, alla riduzione dell’infiammazione e a una migliore protezione della guaina mielinica. Un elemento chiave è stato un regolatore chiamato SOCS1, che agisce come freno sui segnali infiammatori. Bloccare SOCS1 negli astrociti ha annullato gran parte del profilo genico protettivo e ha portato queste cellule a rilasciare più fattori infiammatori che attraggono cellule immunitarie. Al contrario, quando SOCS1 era attivo, gli astrociti producevano più segnali di crescita e riparazione e rilasciavano una miscela di molecole che riduceva la migrazione dei monociti infiammatori. Cambiamenti protettivi simili sono stati osservati in linee cellulari umane di astrociti e microglia trattate con la combinazione farmacologica, suggerendo che il meccanismo è rilevante anche oltre il modello murino.
Cosa potrebbe significare per le future terapie della SM
Questo studio mostra che abbinare il fingolimod con l’interferone‑beta somministrato per via nasale può fare più che bloccare le cellule immunitarie nel sangue. Può anche riprogrammare gli astrociti all’interno del sistema nervoso centrale verso uno stato più calmo e protettivo, con SOCS1 che agisce come nodo di controllo centrale. Pur essendo lavori condotti su topi e colture cellulari, e pur avendo l’interferone‑beta non testato sempre in parallelo in tutti gli esperimenti, i risultati indicano una strategia promettente: mirare contemporaneamente al sistema immunitario periferico e alle cellule di supporto del cervello. Se effetti simili potranno essere ottenuti e dimostrati sicuri nell’uomo, approcci combinati e focalizzati sul cervello potrebbero contribuire a rallentare o in parte invertire i danni silenziosi che guidano la SM progressiva.
Citazione: Tsaktanis, T., Beyer, T., Nirschl, L. et al. Interferon-β and FTY720 ameliorate progressive CNS inflammation via SOCS1-associated astrocyte signaling. Sci Rep 16, 9851 (2026). https://doi.org/10.1038/s41598-026-45303-9
Parole chiave: sclerosi multipla progressiva, fingolimod, interferone beta, astrociti, neuroinfiammazione