Clear Sky Science · it
Indagare le interazioni tra la proteina di immunità Colicin E9 di Escherichia coli e la DNA girasi di Pseudomonas aeruginosa: approccio computazionale avanzato per sviluppare nuove strategie antimicrobiche
Trasformare le armi batteriche in nuovi farmaci
Con la diffusione della resistenza agli antibiotici, i medici stanno esaurendo gli strumenti per fermare le infezioni pericolose. Alcuni dei colpevoli più ostinati, come Pseudomonas aeruginosa, sono in grado di resistere a molti farmaci. Questo studio cerca ispirazione direttamente dai batteri, esplorando come la proteina protettiva integrata di un microrganismo potrebbe essere riconvertita per disattivare un enzima vitale in un altro microrganismo. Utilizzando simulazioni computazionali avanzate, i ricercatori mostrano come una piccola proteina di “immunità” possa legarsi saldamente a un enzima batterico chiave, suggerendo una nuova strada per futuri antimicrobici.
Un piccolo scudo contro una tossina letale
Alcuni ceppi di Escherichia coli producono potenti tossine proteiche chiamate colicine, in grado di uccidere batteri vicini. Per evitare di avvelenarsi, questi batteri producono anche proteine di immunità corrispondenti. Uno di questi protettori, noto come proteina di immunità del Colicin E9 (spesso chiamata Im9), si lega al dominio tagliente della tossina e impedisce che danneggi il DNA dell’ospite. Poiché questa coppia è così specifica e stabile, gli scienziati hanno da tempo sospettato che comprenderne i dettagli possa rivelare nuovi modi per controllare batteri dannosi. In questo lavoro, gli autori si chiedono se Im9 possa anche agganciarsi alla DNA girasi, un enzima essenziale di Pseudomonas aeruginosa che gestisce il modo in cui il suo DNA è avvolto e replicato.
Colpire un enzima vulnerabile in un germe difficile da trattare
Pseudomonas aeruginosa è un importante patogeno ospedaliero, capace di sopravvivere in ambienti ostili e resistente a molti farmaci. La DNA girasi è uno dei suoi enzimi più importanti, responsabile di mantenere correttamente attorcigliati i lunghi filamenti di DNA del batterio affinché possano essere replicati. Poiché bloccare questo enzima può arrestare la crescita batterica, è già un bersaglio valido per alcuni antibiotici. Gli autori hanno usato uno strumento di deep learning per esaminare la struttura tridimensionale della DNA girasi di Pseudomonas e individuare i probabili “hotspot”—cluster di amminoacidi sulla sua superficie più importanti per il legame con partner. Queste regioni formano la tasca attiva dell’enzima, dove avviene il normale processamento del DNA e dove idealmente si legherebbe un potenziale inibitore.
Simulare una stretta di mano molecolare
Per verificare se Im9 potesse afferrare questi hotspot, i ricercatori hanno impiegato programmi di docking molecolare che “incastrano” virtualmente le proteine come puzzle 3D. Hanno prima ripulito e completato le strutture disponibili di Im9 e della DNA girasi, riparando un loop mancante nell’enzima ed eseguendo brevi simulazioni per rilassare eventuali regioni in tensione. Hanno quindi usato due strumenti di docking complementari, ClusPro e LightDock, per generare molteplici complessi candidati. Da questi hanno selezionato gli arrangiamenti più promettenti e li hanno sottoposti a lunghe simulazioni di dinamica molecolare che si estendono per centinaia di nanosecondi. Questi filmati temporali hanno permesso di osservare come le due proteine si adattassero, si flettevano e si stabilizzassero in conformazioni più stabili quando legate tra loro.
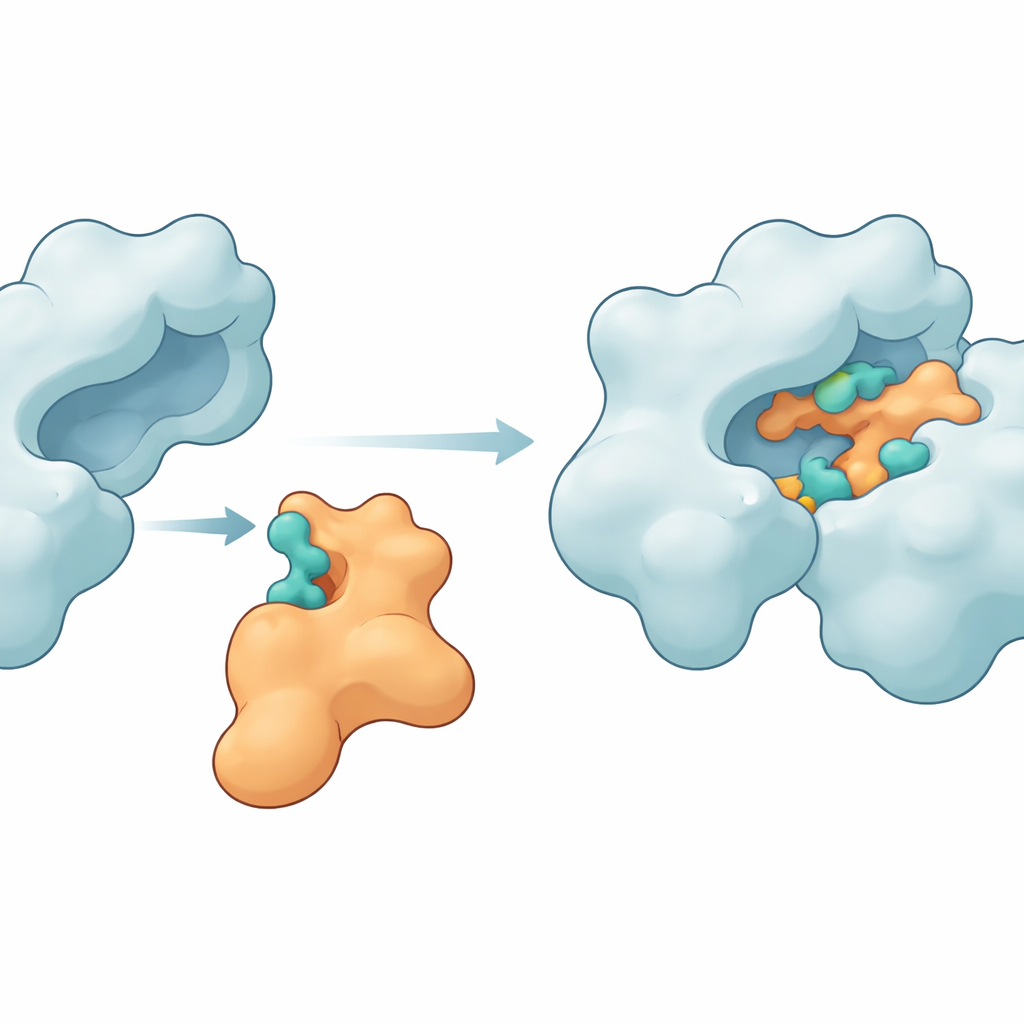
Punti di contatto chiave che tengono unite le proteine
Le simulazioni hanno rivelato che Im9 può effettivamente formare un complesso aderente e persistente con la DNA girasi. Diversi amminoacidi sull’enzima—come MET27, ASP47, LYS105, LEU198, ASN199, ARG191 e GLU194—hanno ripetutamente formato legami a idrogeno e altre forze attrattive con siti corrispondenti su Im9. In un modello di punta, i due partner hanno mantenuto tra sei e dieci legami a idrogeno per la maggior parte della simulazione, segno di un’interfaccia solida e ben organizzata. Altre misure strutturali, inclusa la compattezza delle proteine e l’ampiezza delle loro fluttuazioni conformazionali, hanno mostrato che l’enzima è rimasto integro mentre la proteina di immunità si è flette appena il necessario per modellarsi attorno alla superficie della girasi. I calcoli energetici mediante il metodo MM-GBSA hanno ulteriormente sostenuto l’idea che questi contatti generino una energia libera di legame favorevole, seppur modesta, dominata da contributi elettrostatici e di van der Waals.
Dai modelli al computer ai futuri antimicrobici
Nel complesso, i risultati suggeriscono che la proteina di immunità del Colicin E9 può legarsi stabilmente alla regione attiva della DNA girasi di Pseudomonas, formando un complesso persistente che, in linea di principio, potrebbe bloccare il ruolo normale dell’enzima nella gestione del DNA. Pur essendo questi risultati basati interamente su modelli computazionali e richiedendo ancora conferme sperimentali, forniscono un progetto dettagliato di dove e come un inibitore a base proteica potrebbe agganciarsi. Per i non specialisti, il messaggio chiave è che le armi e gli scudi naturali dei batteri possono ispirare nuove strategie contro le infezioni difficili da trattare. Comprendendo questa stretta di mano microscopica a livello atomico, gli scienziati si avvicinano a progettare nuovi antimicrobici in grado di disattivare enzimi batterici cruciali senza danneggiare le cellule umane.
Citazione: Alfaraj, R., Alkathiri, F. & Chikhale, R. Investigating Escherichia coli Colicin E9 immunity protein interactions with DNA gyrase of Pseudomonas aeruginosa: advanced computational approach for developing novel antimicrobial strategies. Sci Rep 16, 10786 (2026). https://doi.org/10.1038/s41598-026-44427-2
Parole chiave: resistenza agli antibiotici, DNA girasi, interazioni proteina–proteina, progettazione di farmaci computazionale, Pseudomonas aeruginosa