Clear Sky Science · it
Dati cristallografici per la dolichilphosphate mannose sintetasi di Pyrococcus furiosus suggeriscono che l’enzima potrebbe ribaltare il suo prodotto glicolipidico
Come i microrganismi termofili mantengono in forma il proprio rivestimento cellulare
Molti microrganismi che prosperano in ambienti bollenti sopravvivono grazie a un rivestimento protettivo di zuccheri sulla superficie cellulare. La costruzione di questo strato richiede speciali molecole grasso–zucchero che devono essere sintetizzate da un lato della membrana cellulare e poi spostate dall’altro. Questo studio analizza uno di questi enzimi sintetici proveniente da un microrganismo termofilo e suggerisce che, sorprendentemente, la stessa proteina potrebbe anche contribuire a ribaltare il suo prodotto attraverso la membrana—svolgendo dunque due funzioni contemporaneamente.
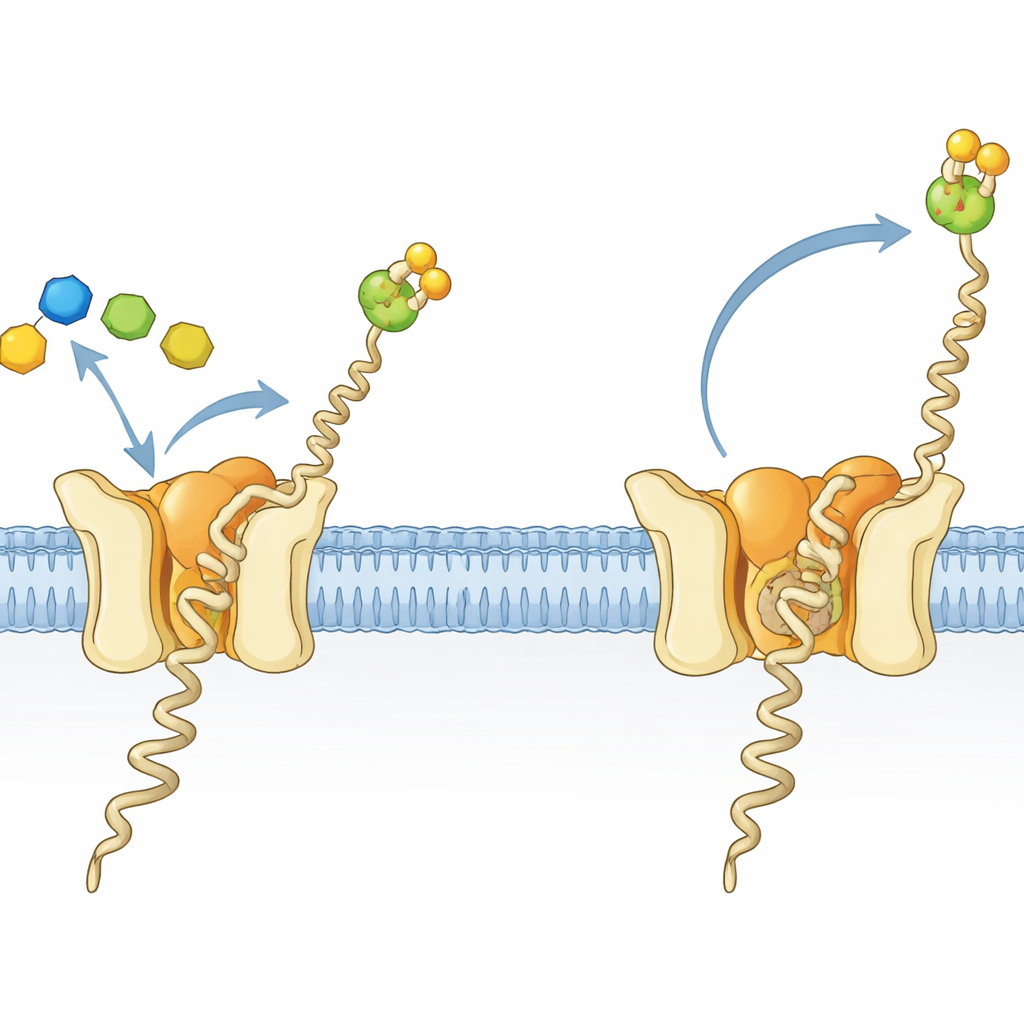
Una piccola fabbrica per una molecola zucchero–grasso cruciale
Le cellule in tutti i domini della vita decorano molte proteine con catene di zuccheri, un processo essenziale per il corretto ripiegamento, la stabilità e la comunicazione cellula–cellula. Negli archei e negli eucarioti, un elemento chiave per queste decorazioni è una molecola zucchero–grasso chiamata dolichilphosphate mannose (Dol-P-Man). Essa consiste in una lunga coda lipidica ancorata nella membrana e una testa zucchero–fosfato che sporge nell’ambiente acquoso. Dol-P-Man è prodotta dall’enzima dolichilphosphate mannose sintetasi (DPMS), che trasferisce uno zucchero mannoso da un donatore solubile su un lipide legato alla membrana. Nell’archeon ipertermofilo Pyrococcus furiosus, la DPMS è una proteina a catena singola, chiamata DPMS di tipo III, con una regione catalitica solubile collegata a una sezione transmembrana composta da quattro eliche il cui ruolo era rimasto poco chiaro.
Cogliere l’enzima in azione
I ricercatori hanno cristallizzato la DPMS di P. furiosus insieme ai suoi substrati e hanno seguito la reazione mediante cristallografia a raggi X. La loro nuova struttura, combinata con tre precedenti, cattura una serie di istantanee attorno al momento del trasferimento dello zucchero. In uno stato, la molecola donatrice (GDP‑mannosio) e un accettore simile a Dol‑P sono legati in una geometria precisa che pone il carbonio reattivo del mannoso direttamente di fronte al gruppo fosfato su Dol‑P—una disposizione “pre‑trasferimento” ideale. Anse dell’enzima funzionano come porte anteriore e posteriore: si chiudono per trattenere il donatore e lo ione metallico, poi si riarrangiano per aprire un percorso che permette a Dol‑P di entrare e al GDP esaurito di uscire una volta che lo zucchero è stato trasferito. Questi dettagli chiariscono come l’enzima garantisca un trasferimento dello zucchero efficiente e accurato sulla superficie della membrana.
Un prodotto capovolto nascosto nella membrana
Più sorprendente è stato un secondo stato distinto osservato negli stessi cristalli. Qui, la Dol‑P‑Man completata non si trova nel sito attivo ma è incastrata più in profondità nella parte transmembrana della proteina, in un’orientazione “capovolta”. La sua testa zucchero–fosfato siede in una tasca polare tra due coppie di eliche (TMD1 e TMD2), mentre la coda lipidica scorre lungo una scanalatura formata dalle eliche. Un amminoacido chiave, una fenilalanina, sembra agire come un cancello che può ostruire o aprire l’accesso a questa tasca. La qualità della densità elettronica e il modo in cui la proteina si impacchetta nel cristallo suggeriscono che questa Dol‑P‑Man capovolta non sia un artefatto dei contatti cristallini, ma uno stato genuino e ben popolato che l’enzima può assumere.
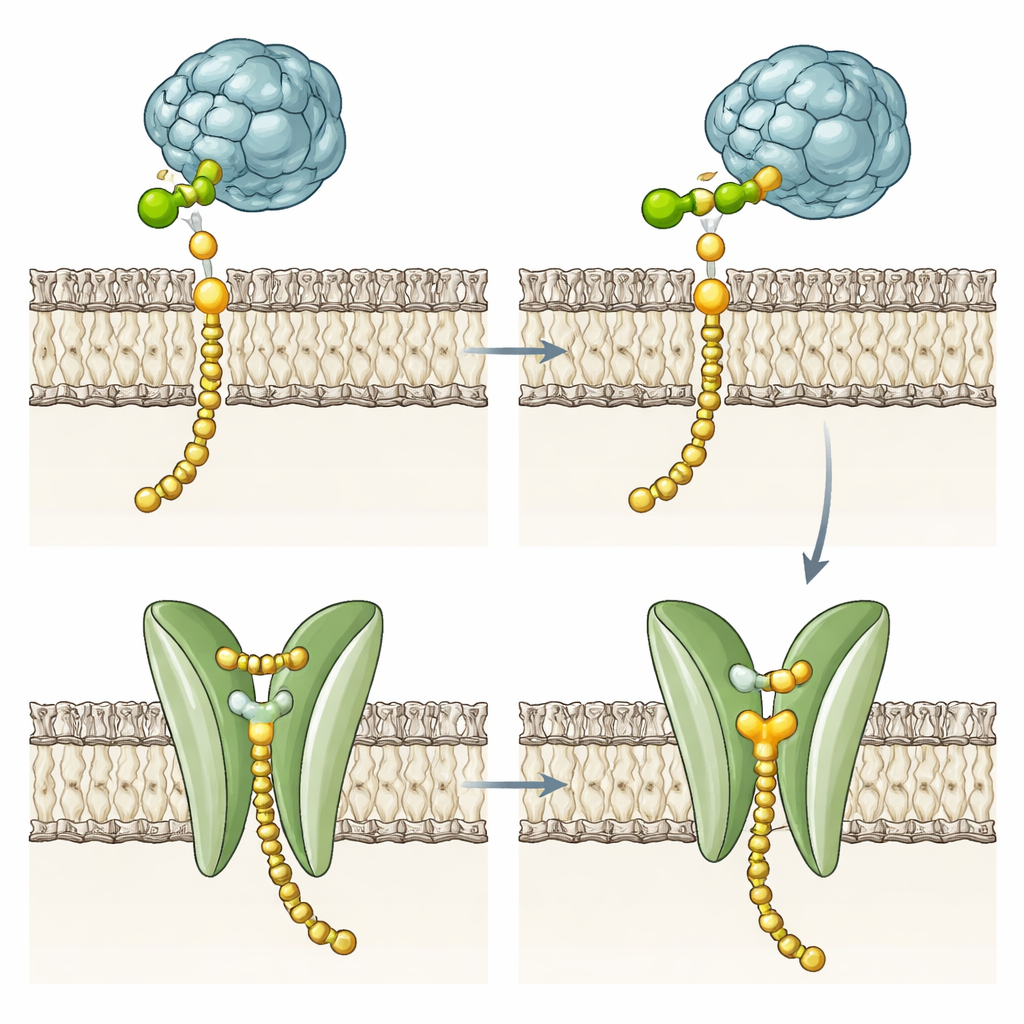
Enzimi mutanti suggeriscono un secondo compito
Per verificare se il dominio transmembrana fosse necessario per la chimica del trasferimento dello zucchero, il team ha ingegnerizzato molte varianti. Hanno eliminato la maggior parte o tutte le eliche, le hanno sostituite con un segmento di membrana diverso tratto dalla DPMS di lievito, oppure hanno alterato residui chiave della tasca e la fenilalanina di gating. Sorprendentemente, questi muti hanno continuato a produrre Dol‑P‑Man a velocità simili all’enzima intatto, sebbene alcuni fossero leggermente meno stabili nella membrana. Questo dimostra che la chimica fondamentale risiede nella regione catalitica solubile e che il fascio di quattro eliche non è necessario per attaccare il mannoso al Dol‑P. Al contrario, la sua tasca polare conservata, la scanalatura e il residuo di gating suggeriscono un ruolo specializzato nella gestione del prodotto finito, in particolare negli archei ipertermofili le cui membrane rigide rendono il ribaltamento spontaneo dei lipidi energeticamente costoso.
Perché un enzima a doppio scopo è importante
Mettere insieme le evidenze strutturali e mutazionali, gli autori propongono che la DPMS di tipo III sia una proteina “moonlighting”. Prima sintetizza Dol‑P‑Man sulla faccia interna della membrana plasmatica archeale; poi il suo dominio transmembrana potrebbe aiutare a ribaltare la molecola zucchero–grasso in modo che il gruppo testa emerga all’esterno della cellula, pronto per essere utilizzato da altri enzimi che costruiscono il rivestimento zuccherino cellulare. L’evoluzione sembra aver favorito questo progetto chimerico soprattutto negli archei estremamente termofili, dove portare il sito di sintesi vicino a una scanalatura dedicata al ribaltamento potrebbe minimizzare sprechi e danni termici. Sebbene questo lavoro non dimostri ancora direttamente l’attività di flipping, offre un modello strutturale concreto su come un enzima possa sia creare sia riposizionare un intermedio lipidico vitale attraverso una barriera di membrana ostile.
Citazione: Gandini, R., Keskitalo, M.M., Reichenbach, T. et al. Crystallographic data for Pyrococcus furiosus dolichylphosphate mannose synthase suggest that the enzyme could flip its glycolipid product. Sci Rep 16, 9076 (2026). https://doi.org/10.1038/s41598-026-44343-5
Parole chiave: dolichilphosphate mannose, flippasi lipidica, archea, glicosilazione delle proteine, enzimi di membrana