Clear Sky Science · it
Analisi delle protesi della valvola aortica mediante imaging cardiovascolare avanzato—un approccio traslazionale inverso specifico per il paziente
Perché la scelta della valvola cardiaca conta
Dato che sempre più persone vivono abbastanza a lungo da sviluppare valvole cardiache consumate, i medici sostituiscono questi piccoli passaggi nel cuore con valve artificiali. Oggi molti pazienti ricevono valvole introdotte attraverso un vaso sanguigno, evitando la chirurgia a cuore aperto, mentre altri ricevono nuove valvole chirurgiche “a rapido impianto” progettate per accelerare l’intervento. Tuttavia questi dispositivi non sono tutti uguali. Questo studio esamina in dettaglio quattro protesi aortiche ampiamente utilizzate per capire come influenzano realmente il flusso sanguigno, usando un modello a grandezza naturale dell’aorta di una paziente stampato in 3D e strumenti di imaging all’avanguardia.
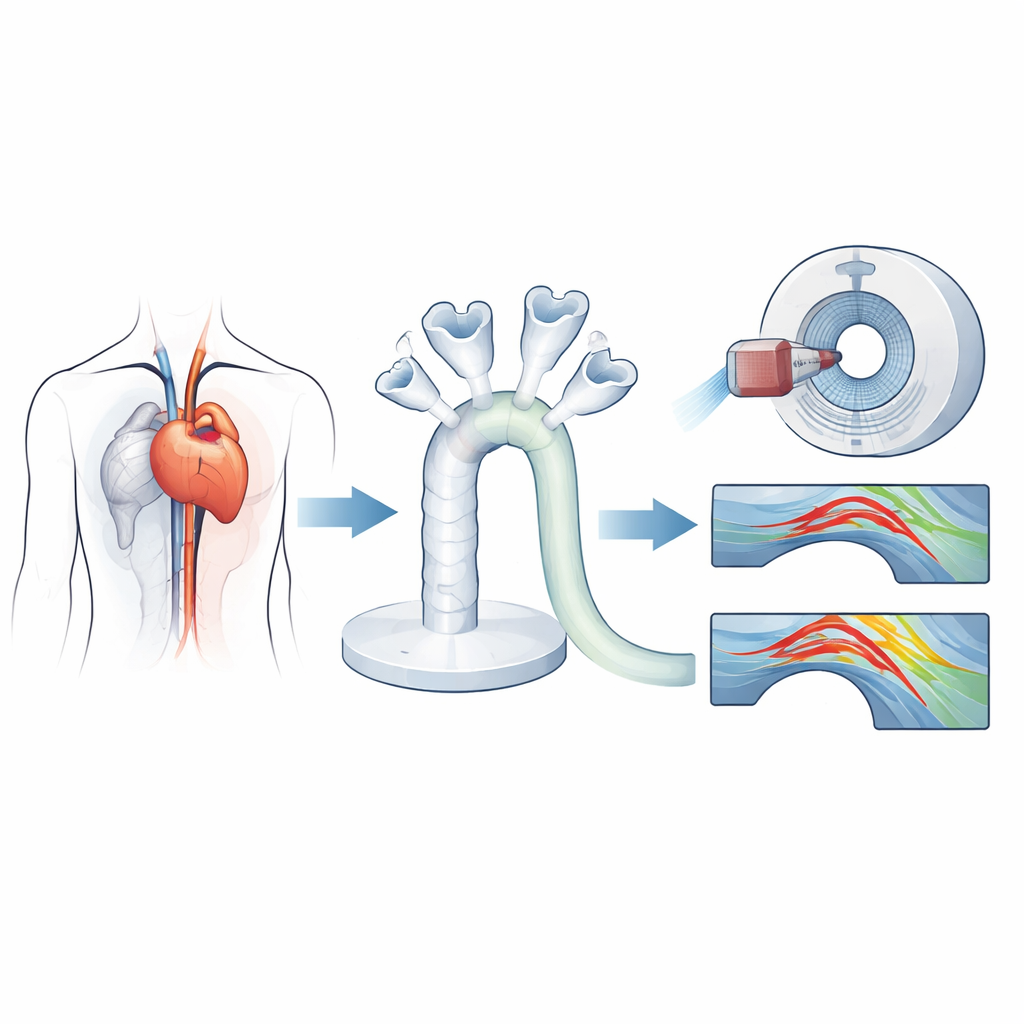
Costruire un banco di prova realistico
I ricercatori hanno iniziato con una scansione TC ad alta risoluzione di una donna la cui valvola aortica naturale necessitava di sostituzione e il cui orifizio valvolare era di dimensioni relativamente piccole—una situazione comune e clinicamente impegnativa. Da questa scansione hanno ricostruito digitalmente la radice e l’arco aortico, quindi hanno stampato in 3D un modello flessibile e trasparente della sua aorta. In copie identiche di questo fantoccio hanno impiantato quattro valvole biologiche moderne: due valvole chirurgiche a rapido impianto e due valvole transcatetere come nella procedura TAVR. Una pompa controllata da computer ha spinto un fluido simile al sangue attraverso il sistema, replicando un battito cardiaco normale, le pressioni e le portate in modo che ogni protesi potesse essere testata nelle stesse condizioni realistiche.
Osservare il sangue in quattro dimensioni
Per vedere come ciascuna valvola rimodellava il flusso sanguigno, il team ha combinato due metodi di imaging avanzati. L’ecografia a flusso vettoriale ha fornito mappe in tempo reale della velocità e della direzione del movimento del fluido in sezioni chiave dell’aorta ascendente. La risonanza magnetica 4D flow ha quindi catturato i modelli di flusso tridimensionali nel tempo, permettendo ai ricercatori di calcolare grandezze dettagliate come lo sforzo di taglio sulla parete (la frizione del sangue che scorre lungo la parete del vaso), le cadute di pressione lungo l’aorta, la perdita di energia cinetica e l’area di apertura efficace attraverso cui il sangue effettivamente passava. Insieme, queste misure hanno rivelato non solo se il sangue passava attraverso la valvola, ma quanto scorreva in modo uniforme o turbolento a valle.
Valvole diverse, storie di flusso diverse
Lo studio ha riscontrato che le due valvole transcatetere e le due valvole chirurgiche a rapido impianto producono comportamenti di flusso visibilmente differenti, nonostante tutte fossero formalmente dimensionate per adattarsi alla stessa anatomia della paziente. In generale, le valvole a rapido impianto hanno generato velocità medie di flusso più elevate rispetto alle valvole transcatetere, mentre queste ultime tendevano a produrre un getto d’apertura dalla forma più triangolare. Un modello a rapido impianto ha mostrato una perdita di energia cinetica e gradienti di pressione particolarmente elevati lungo l’aorta, il che significa che veniva sprecata più energia per spingere il sangue attraverso e oltre la valvola. Al contrario, un’altra valvola a rapido impianto con un’area di apertura efficace leggermente maggiore ha permesso al sangue di transitare con minore resistenza e minori perdite energetiche, nonostante fosse etichettata per lo stesso diametro nominale dell’anello aortico.
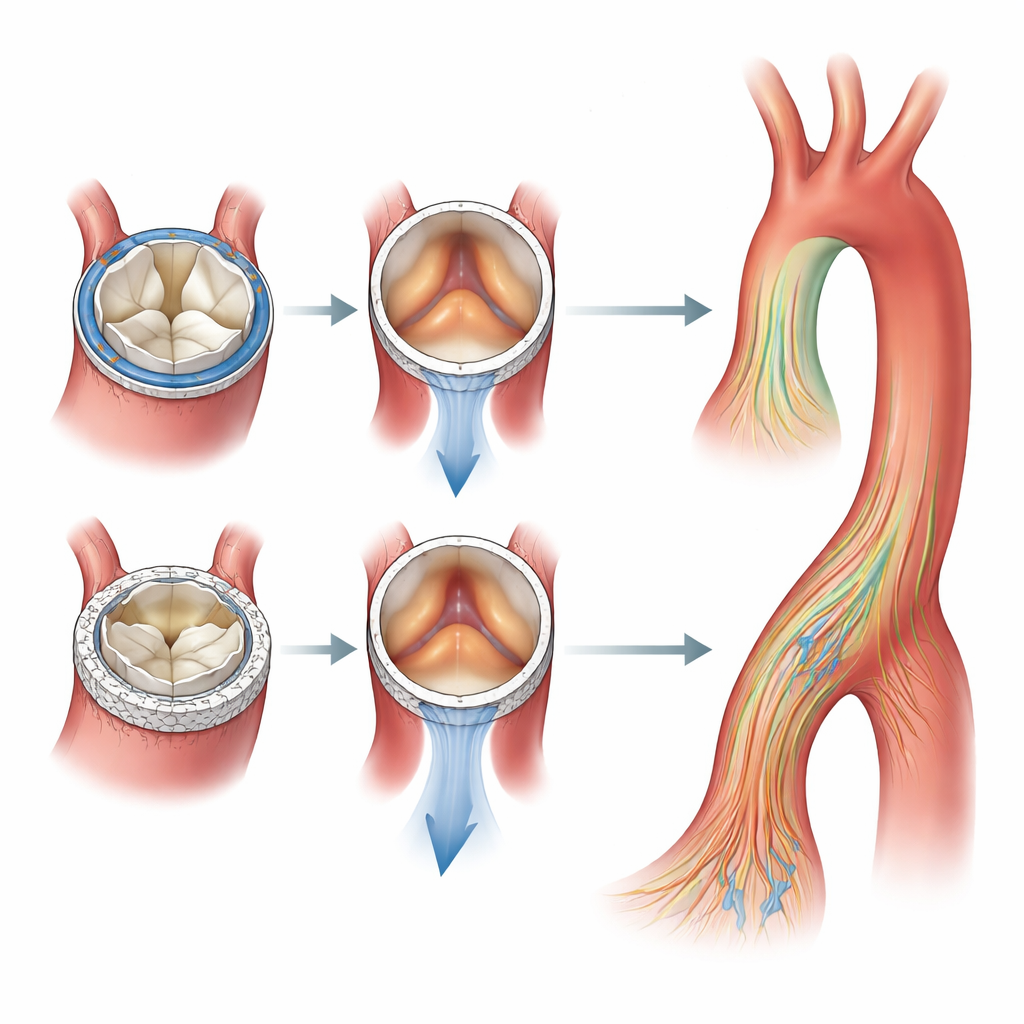
Pattern di flusso sottili e sollecitazioni sulla parete
Quando il team ha esaminato le forze che agiscono sulla parete vascolare, ha osservato zone di sforzo di taglio elevato in siti prevedibili: vicino alla radice aortica, lungo la curva esterna dell’aorta ascendente, intorno all’arco e in parti dell’aorta discendente. Questi punti caldi sono apparsi per tutte e quattro le valvole, e non ci sono state differenze drammatiche nella loro localizzazione tra dispositivi chirurgici e transcatetere. Tuttavia, la distribuzione e l’entità dei getti di flusso e dei pattern vorticosi differivano in modi che potrebbero avere rilevanza nel tempo, potenzialmente influenzando il rimodellamento della parete vascolare o la tolleranza di una specifica protesi da parte del paziente.
Verso una scelta della valvola più personalizzata
Per i non specialisti, il messaggio chiave è che scegliere una valvola cardiaca non è semplice come abbinare una misura sull’etichetta a un’apertura misurata. In questo modello paziente-specifico, attentamente controllato, valvole destinate alla stessa anatomia si sono comportate in modo piuttosto diverso, con una valvola a rapido impianto che è risultata la più efficiente dal punto di vista energetico e la più delicata sulla parete vascolare nel complesso. Il lavoro dimostra che aortas stampate in 3D combinate con imaging avanzato possono funzionare come una sorta di pista di prova per valvole nuove ed esistenti, aiutando i medici a prevedere come un dispositivo si comporterà in un corpo specifico. Nel tempo, approcci di questo tipo potrebbero portare a standard più chiari per la dimensionamento e la selezione delle valvole, ridurre gli scarti tra valvole e pazienti e facilitare la personalizzazione della terapia salvavita per ogni individuo.
Citazione: Grefen, L., Herz, C., Flexeder, J. et al. Analysis of aortic valve prostheses using advanced cardiovascular imaging—a patient-specific reversed translational approach. Sci Rep 16, 9334 (2026). https://doi.org/10.1038/s41598-026-44295-w
Parole chiave: sostituzione della valvola aortica, protesi della valvola cardiaca, aorta stampata in 3D, 4D flow MRI, valvola transcatetere