Clear Sky Science · it
Modellare la patogenesi delle tossine di Clostridioides difficile e la protezione dell antisiero in una piattaforma intestino‑on‑chip immunocompetente
Perché questo modello di infezione intestinale è importante
Gli antibiotici salvano vite, ma possono anche rendere l intestino vulnerabile a infezioni pericolose. Uno dei peggiori colpevoli è Clostridioides difficile, un batterio che può causare diarrea grave e un infiammamento del colon potenzialmente letale, soprattutto nei pazienti ospedalizzati. Questo studio presenta un piccolo “intestino su chip” che ricrea caratteristiche chiave dell intestino umano, incluse le vasi sanguigni e le cellule immunitarie, per osservare in tempo reale come le tossine di C. difficile danneggiano l intestino e come i trattamenti con anticorpi potrebbero prevenire tale danno.
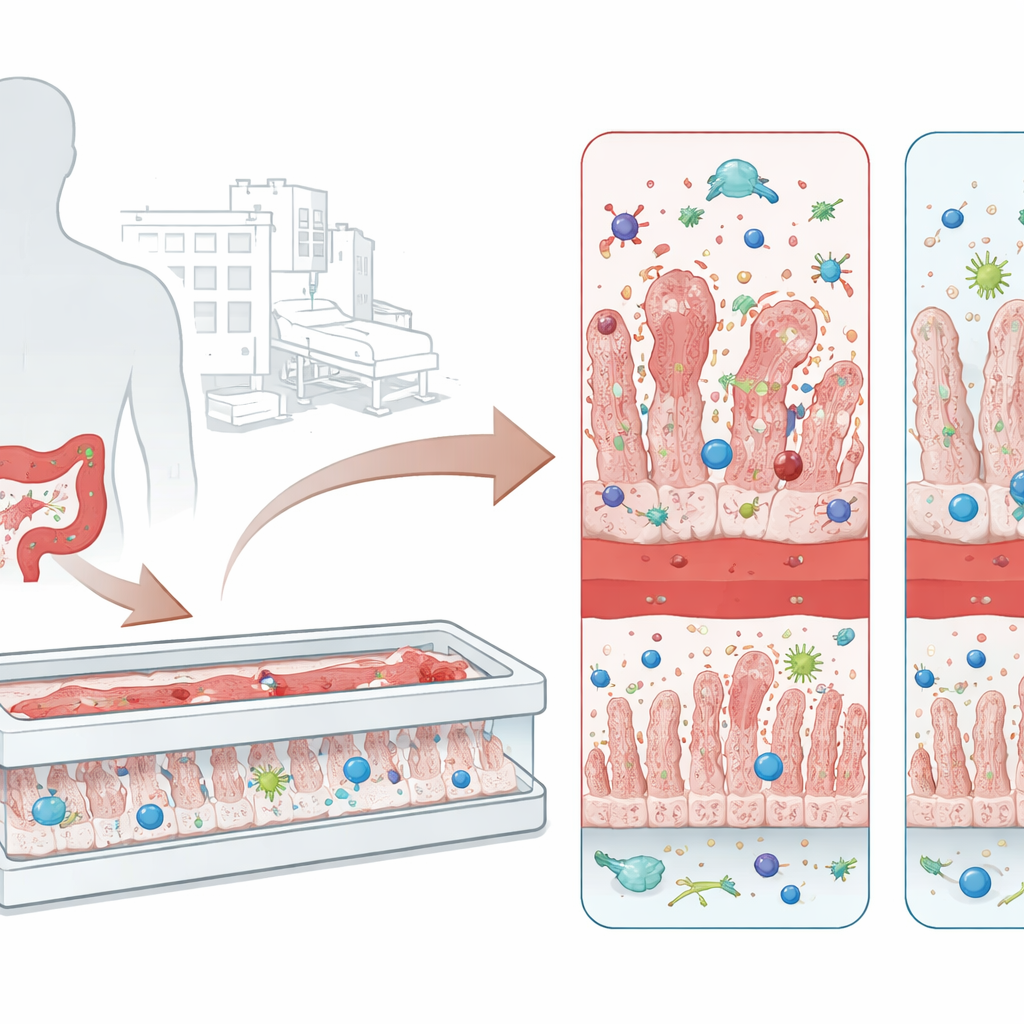
Da un ostinato batterio ospedaliero al danno intestinale
C. difficile prospera in persone il cui microbiota intestinale è stato alterato, spesso dopo un ciclo di antibiotici ad ampio spettro. Il microrganismo sopravvive a condizioni avverse come spore resistenti e, una volta stabilito nel colon, rilascia due tossine principali note come TcdA e TcdB. Queste tossine attaccano le cellule intestinali, allentano le giunzioni tra di esse e scatenano ondate di infiammazione. Il risultato può variare da una diarrea fastidiosa alla colite pseudomembranosa, una condizione caratterizzata da strati di tessuto e cellule immunitarie morte che rivestono la parete intestinale. I trattamenti attuali si basano soprattutto su altri antibiotici e talvolta su trapianti di feci; tuttavia molti pazienti subiscono reinfezioni, evidenziando la necessità di modi migliori per studiare la malattia e testare terapie che bloccano le tossine.
Costruire un piccolo intestino vivente su chip
I modelli tradizionali di laboratorio coltivano un foglio piatto di cellule intestinali in una piastra. Pur essendo utili, queste colture bidimensionali mancano di vasi sanguigni, cellule immunitarie e del flusso di fluidi delicato che caratterizza un intestino reale. I ricercatori hanno invece utilizzato un dispositivo microingegnerizzato “intestino‑on‑chip” con due canali paralleli separati da una membrana porosa. Un lato è rivestito da cellule intestinali che crescono formando creste simili a villi e costituiscono una barriera ermetica. Il lato opposto ospita cellule dei vasi sanguigni umani. In questo tessuto in miniatura il team ha aggiunto macrofagi derivati da monociti che si integrano nella parete intestinale e neutrofili circolanti che possono viaggiare attraverso il canale vascolare e infiltrarsi nel tessuto, creando un intestino‑on‑chip immunocompetente (i‑IoC) che imita più fedelmente l intestino vivente.
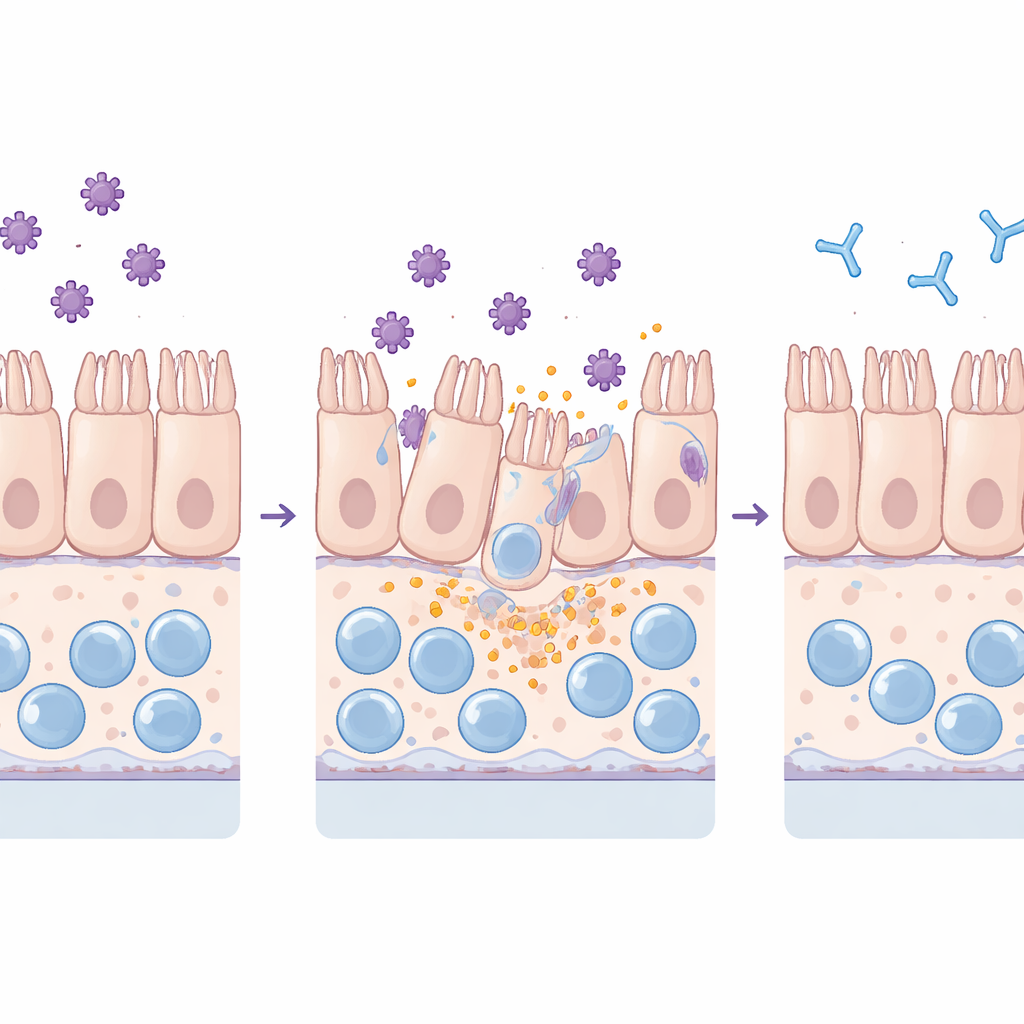
Osservare le tossine che danneggiano la barriera
Il team ha esposto sia le colture piatte standard sia il chip più complesso alle tossine purificate TcdA e TcdB. Hanno monitorato quanto la barriera intestinale trattenesse un colorante fluorescente, esaminato le proteine di giunzione che tengono unite le cellule adiacenti e misurato le molecole infiammatorie e i marcatori di danno cellulare nel fluido circostante. Entrambe le tossine danneggiavano il tessuto, ma in modi distinti: la TcdA interrompeva principalmente le giunzioni strette e causava il raggrinzimento delle cellule, mentre la TcdB provocava una perdita diffusa di cellule dallo strato. Crucialmente, il chip ha rilevato questi effetti a livelli di tossina molto più bassi rispetto alle colture piatte, riflettendo la sua maggiore sensibilità e un comportamento più simile al vivo sotto flusso continuo.
Le cellule immunitarie alimentano l infiammazione—e possono essere protette
L aggiunta di macrofagi e neutrofili al chip ha amplificato la risposta alle tossine. I macrofagi hanno aumentato il rilascio di messaggeri infiammatori chiave come IL‑6 e IL‑8 ma sono stati a loro volta esauriti, coerente con una forma infiammatoria di morte cellulare. I neutrofili si sono aderiti alla parete vascolare e sono migrati nel tessuto intestinale, richiamando l afflusso di cellule immunitarie osservato nei pazienti. Un esposizione prolungata alle tossine ha danneggiato non solo l epitelio intestinale ma infine anche lo strato vascolare. Quando i ricercatori hanno pre‑mescolato le tossine con sieri contenenti anticorpi neutralizzanti le tossine, tuttavia, i danni strutturali, la perdita di barriera, le impennate di citochine, la perdita di macrofagi e l infiltrazione di neutrofili sono stati tutti notevolmente ridotti. In esperimenti prolungati, i tessuti danneggiati da TcdB potevano recuperare parzialmente una volta rimosse le tossine, mentre la TcdA lasciava danni più persistenti, suggerendo diverse capacità di riparazione dopo ciascuna tossina.
Cosa significa per i pazienti e le terapie
Per il lettore non specialista, il messaggio chiave è che questo piccolo modello di intestino vivente può imitare realisticamente come le tossine di C. difficile danneggiano l intestino e attivano il sistema immunitario, rivelando al contempo quanto efficacemente gli anticorpi antitossina possono proteggere il tessuto. Rispetto ai semplici strati cellulari, l intestino‑on‑chip è più sensibile, include vasi sanguigni e cellule immunitarie e può funzionare per giorni per catturare sia il danno iniziale sia i tentativi di recupero. Ciò lo rende un banco di prova promettente per terapie di nuova generazione e vaccini che neutralizzano le tossine senza disturbare ulteriormente il microbiota intestinale, e potenzialmente uno strumento per personalizzare i trattamenti utilizzando cellule derivate dal paziente in futuro.
Citazione: Wegner, V.D., Warschinke, M., Brahim, I.B. et al. Modeling Clostridioides difficile toxin pathogenesis and antiserum protection in an immunocompetent intestine-on-chip platform. Sci Rep 16, 9233 (2026). https://doi.org/10.1038/s41598-026-44170-8
Parole chiave: Clostridioides difficile, intestino‑on‑chip, infezione intestinale, anticorpi neutralizzanti, modelli organ‑on‑chip