Clear Sky Science · it
Microscopia multiphotonica senza marcatori e apprendimento automatico per il riconoscimento del carcinoma epatocellulare
Perché è importante per le persone con tumore al fegato
Il cancro del fegato, in particolare il carcinoma epatocellulare, è sia comune sia letale, e l’intervento chirurgico rappresenta spesso l’unica possibilità di cura. Durante l’operazione i chirurghi devono rimuovere l’intero tumore preservando il più possibile il tessuto epatico sano, un difficile gioco di equilibrismo quando il fegato malato ha già un aspetto anomalo. Questo studio esplora un nuovo modo di “vedere” il cancro in tempo reale durante l’intervento, senza coloranti o laboriosi esami di laboratorio, combinando una microscopia laser avanzata con l’intelligenza artificiale. L’obiettivo è aiutare i chirurghi a identificare il vero margine del tumore più rapidamente e con maggiore precisione, potenzialmente migliorando gli esiti per i pazienti.
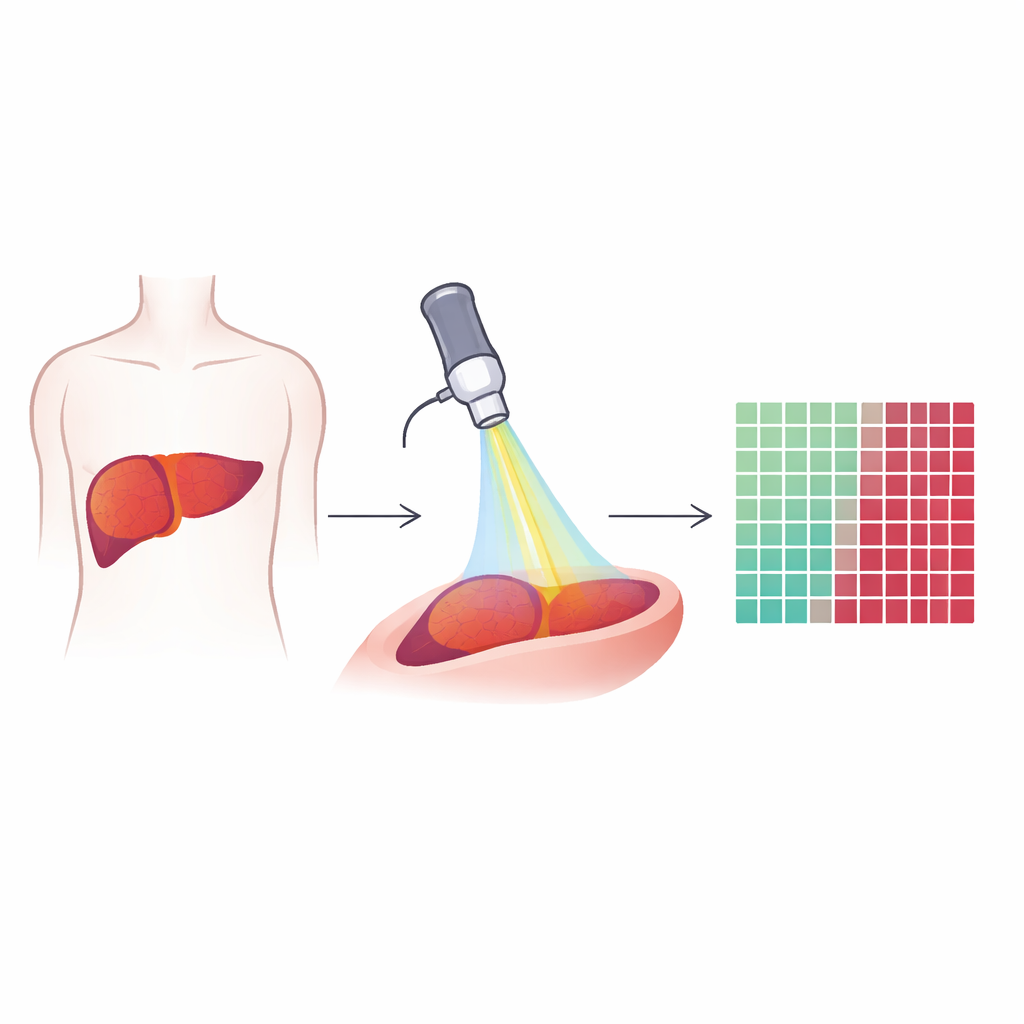
Guardare dentro il tessuto con una luce speciale
I ricercatori hanno usato una tecnica chiamata microscopia multiphotonica, che si basa su impulsi laser molto brevi per far brillare o generare segnali dalle molecole naturali nel tessuto. Invece di aggiungere coloranti o agenti di contrasto, il metodo legge ciò che è già presente: lipidi, fibre di collagene e sostanze naturalmente fluorescenti all’interno delle cellule. Da ciascun piccolo campo visivo nei campioni di fegato sono stati registrati tre tipi di segnali: uno che evidenzia i lipidi, uno che mostra l’autofluorescenza di molecole come NADH e vitamina A, e uno che rivela le fibre di collagene rigide. Insieme questi segnali creano immagini colorate ad alta risoluzione che mostrano sia le singole cellule sia l’architettura complessiva del tessuto epatico e dei tumori.
Catturare i molteplici volti del cancro del fegato
Il gruppo ha esaminato tessuti provenienti da 76 pazienti sottoposti a intervento per tumore al fegato, analizzando sia il tumore sia il fegato circostante. Hanno dimostrato che questo imaging senza marcatori può rappresentare i classici pattern di crescita del carcinoma epatocellulare, come lastre sottili o spesse di cellule tumorali, fogli compatti e strutture simili a ghiandole. Rivela anche i cambiamenti nel fegato circostante, inclusi l’accumulo di grasso e la cicatrizzazione, frequenti nei pazienti con malattia epatica cronica. Importante, questi pattern risultavano visibili anche quando le immagini venivano acquisite a risoluzione relativamente bassa, simile a quella che potrebbero fornire futuri dispositivi endoscopici all’interno del corpo. Ciò suggerisce che l’approccio potrebbe essere pratico in sala operatoria, non solo in laboratorio.
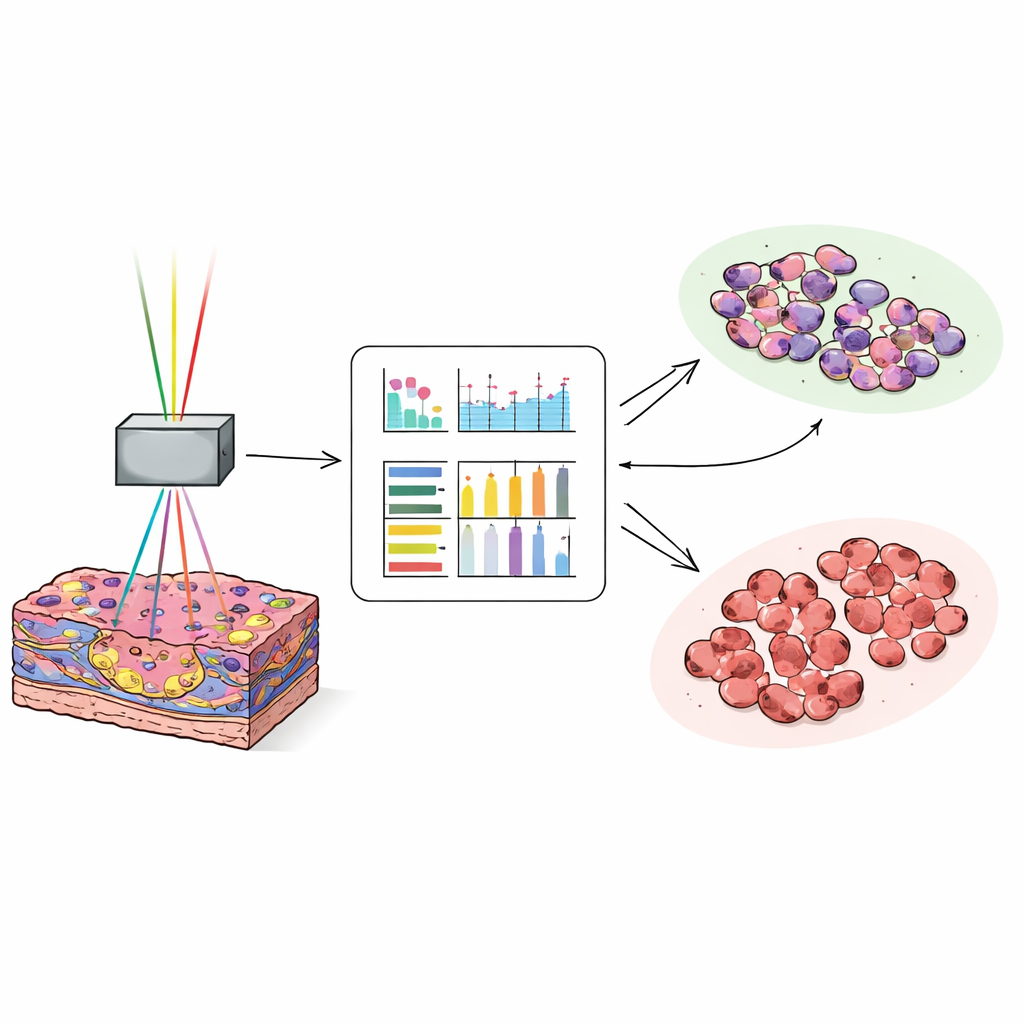
Insegnare a un computer a individuare il margine del tumore
Per trasformare immagini ricche ma complesse in decisioni rapide, gli scienziati hanno convertito ciascuna immagine in numeri che descrivono la texture, ad esempio quanto sono lisci, ruvidi o vari i pattern dei pixel. Per ogni canale d’immagine hanno calcolato 17 misure di questo tipo e poi hanno addestrato una rete neurale su circa 25.000 immagini provenienti da 35 pazienti per distinguere il tessuto tumorale dal fegato non canceroso. Hanno poi testato il modello su circa 27.000 nuove immagini da altri 38 pazienti. Quando il computer ha utilizzato una combinazione dei segnali di autofluorescenza e di quelli sensibili al collagene, ha classificato correttamente le immagini come tumorali o normali in circa 97 casi su 100. Anche i tumori meglio differenziati e più sottili, che possono essere difficili da riconoscere per i patologi su sezioni congelate rapide, sono stati classificati con alta accuratezza.
Cosa rivelano i pattern di luce sul cancro
Confrontando diverse combinazioni di segnali, lo studio ha rilevato che l’autofluorescenza contiene le informazioni più utili per distinguere il cancro dal non-cancro. Questo bagliore proviene da molte molecole naturali all’interno delle cellule e da strutture come elastina e collagene, quindi codifica densità cellulare, dimensione e forma del nucleo (viste come aree più scure), gocce lipidiche e la composizione del tessuto circostante. L’aggiunta del segnale specifico per il collagene ha ulteriormente migliorato il contrasto tra tumore e fegato di sfondo, riflettendo differenze note nell’organizzazione di fibre e vasi sanguigni. Sorprendentemente, il segnale focalizzato sui lipidi ha contribuito meno alla classificazione automatica, un’intuizione pratica perché potrebbe permettere progetti di dispositivi più semplici che si basano su un singolo fascio laser invece di configurazioni a due fasci più complesse.
Dal banco di laboratorio alla sala operatoria
Per simulare l’uso chirurgico reale, il team ha anche applicato il loro miglior modello a campioni di tessuto che includevano il reale confine tra tumore e fegato, creando mappe di probabilità che evidenziavano dove il cancro terminava e iniziava il tessuto normale. Queste mappe concordavano in genere bene con l’istologia convenzionale, sebbene regioni altamente grasse o ricche di collagene talvolta confondessero il classificatore. Gli autori segnalano ostacoli rimanenti prima che questa tecnologia possa guidare interventi in vivo, inclusa la limitata profondità dell’imaging ottico, la necessità di endoscopi robusti e sterili, il movimento e la presenza di sangue nel campo chirurgico, e la sfida di validare l’intelligenza artificiale su grandi dataset reali. Tuttavia, il lavoro mostra che l’imaging multiphotonico senza marcatori, combinato con l’apprendimento automatico, può comportarsi come un microscopio digitale rapido che un giorno potrebbe aiutare i chirurghi a tagliare in modo più preciso e sicuro, aumentando le probabilità di rimuovere tutto il cancro preservando quanto più fegato sano possibile.
Citazione: Galli, R., Korn, S., Aust, D. et al. Label-free multiphoton microscopy and machine learning for recognition of hepatocellular carcinoma. Sci Rep 16, 8734 (2026). https://doi.org/10.1038/s41598-026-43831-y
Parole chiave: imaging del cancro al fegato, microscopia multiphotonica, autofluorescenza, margini chirurgici, apprendimento automatico