Clear Sky Science · it
Chiarire la relazione tra affinità e potenza nelle prestazioni delle IgE terapeutiche
Rivoltare contro il cancro gli anticorpi delle allergie
Chi soffre di allergie conosce la potenza delle IgE — le molecole che innescano occhi che prudono e starnuti improvvisi. Questo studio pone una domanda sorprendente: quella stessa biologia potente può essere reindirizzata per combattere il cancro e, in tal caso, con quale precisione bisognerebbe modulare questi anticorpi per ottenere il massimo effetto? I ricercatori si sono concentrati sui tumori mammari che esprimono la proteina HER2, inclusi i casi in cui HER2 è presente a livelli molto bassi e i farmaci attuali spesso falliscono.
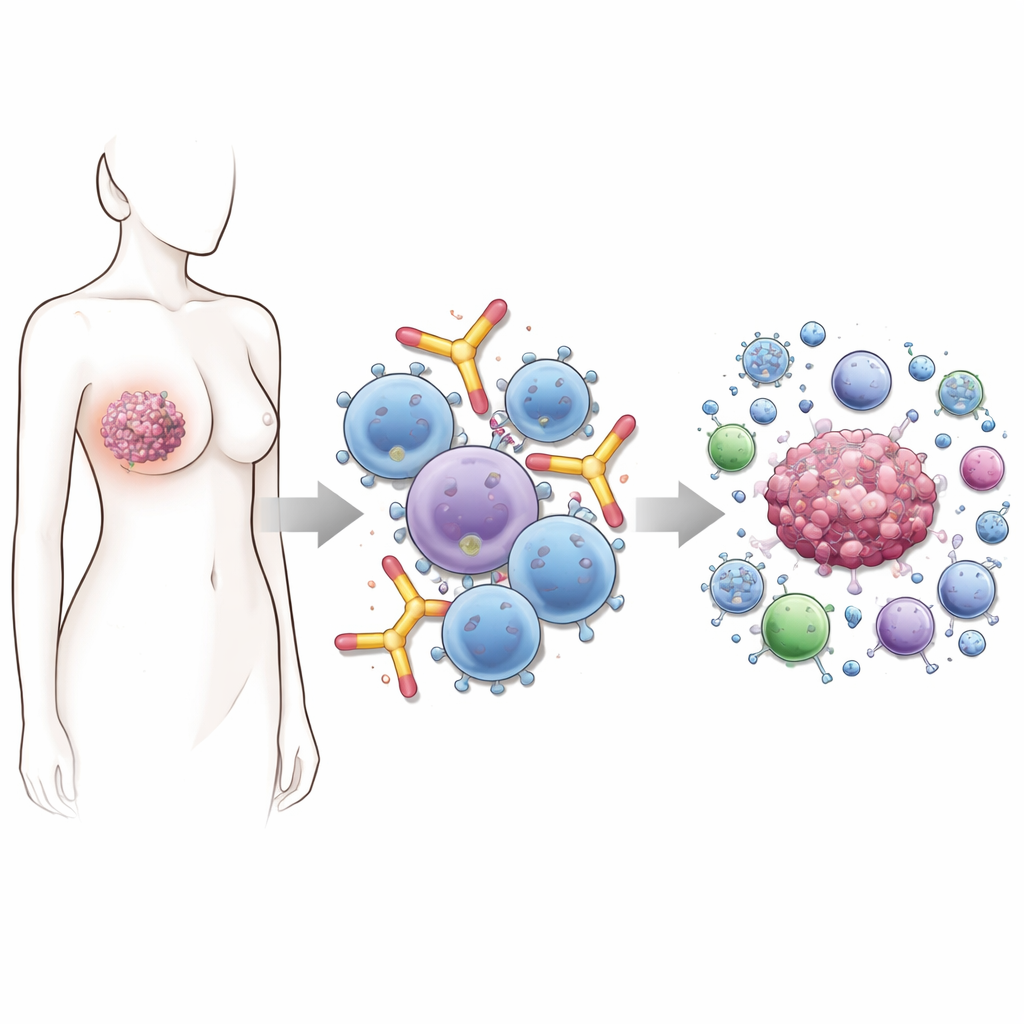
Perché questa classe di anticorpi è così speciale
La maggior parte dei farmaci a base di anticorpi oggi sul mercato appartiene alla classe IgG. Sono i cavalli di battaglia della terapia oncologica moderna, ma hanno dei limiti — soprattutto quando i tumori eludono l’attacco riducendo la quantità della proteina bersaglio sulla loro superficie. Le IgE sono diverse. Si legano naturalmente in modo molto stretto a cellule immunitarie come mastociti, basofili, monociti e macrofagi, predisponendole a risposte rapide. Nelle allergie ciò si traduce in reazioni esplosive a pollini o alimenti. Nel cancro, la stessa configurazione potrebbe significare attacchi rapidi e mirati alle cellule tumorali non appena la IgE incontra il suo bersaglio sulla superficie del tumore.
Progettare una IgE più efficace nel cercare il cancro
Il gruppo aveva già creato un anticorpo IgE, chiamato EPS 226, che riconosce HER2 nelle cellule del cancro al seno e può rallentare la crescita tumorale in modelli sperimentali. In questo nuovo lavoro hanno voluto rispondere a una domanda sottile ma cruciale di progettazione: aumentare la forza con cui l’anticorpo afferra HER2 migliora davvero la sua capacità di mobilitare il sistema immunitario, o la naturale «presa multi‑mano» delle IgE (detta avidità) fa già la maggior parte del lavoro? Per esplorarlo hanno usato un approccio di mutagenesi mirata e selezione in batteri per generare milioni di piccole varianti della regione che si lega a HER2 e poi hanno isolato 12 nuove varianti di IgE che si legavano a HER2 più fortemente dell’anticorpo originale.
Mettere alla prova la potenza su cellule e animali
Questi anticorpi migliorati sono stati poi sottoposti a una serie di esperimenti su cellule. Quando caricati sui mastociti ed esposti a cellule tumorali HER2-positive, la maggior parte delle IgE a legame più forte ha innescato una degranulazione più intensa — una risposta di attivazione che rilascia potenti sostanze immunitarie. Una variante, rinominata EPS 232, si è distinta per la capacità di attivare le cellule pur mantenendo un legame efficace con HER2 su cellule tumorali umane e di ratto. Test ulteriori hanno mostrato che EPS 232 armava meglio le cellule immunitarie per uccidere il cancro: ha potenziato la citotossicità dei basofili e favorito un inglobamento più efficiente delle cellule tumorali HER2-positive da parte di cellule immunitarie ingegnerizzate e di macrofagi umani primari. Interessante notare che aumentare la forza di legame aiutava solo fino a un certo punto; varianti con affinità estremamente elevata non superavano EPS 232, suggerendo l’esistenza di un «punto ottimale» in cui la presa è sufficientemente forte da essere efficace ma non così forte da ostacolare il numero di anticorpi e cellule immunitarie che possono impegnarsi su ciascuna cellula tumorale.
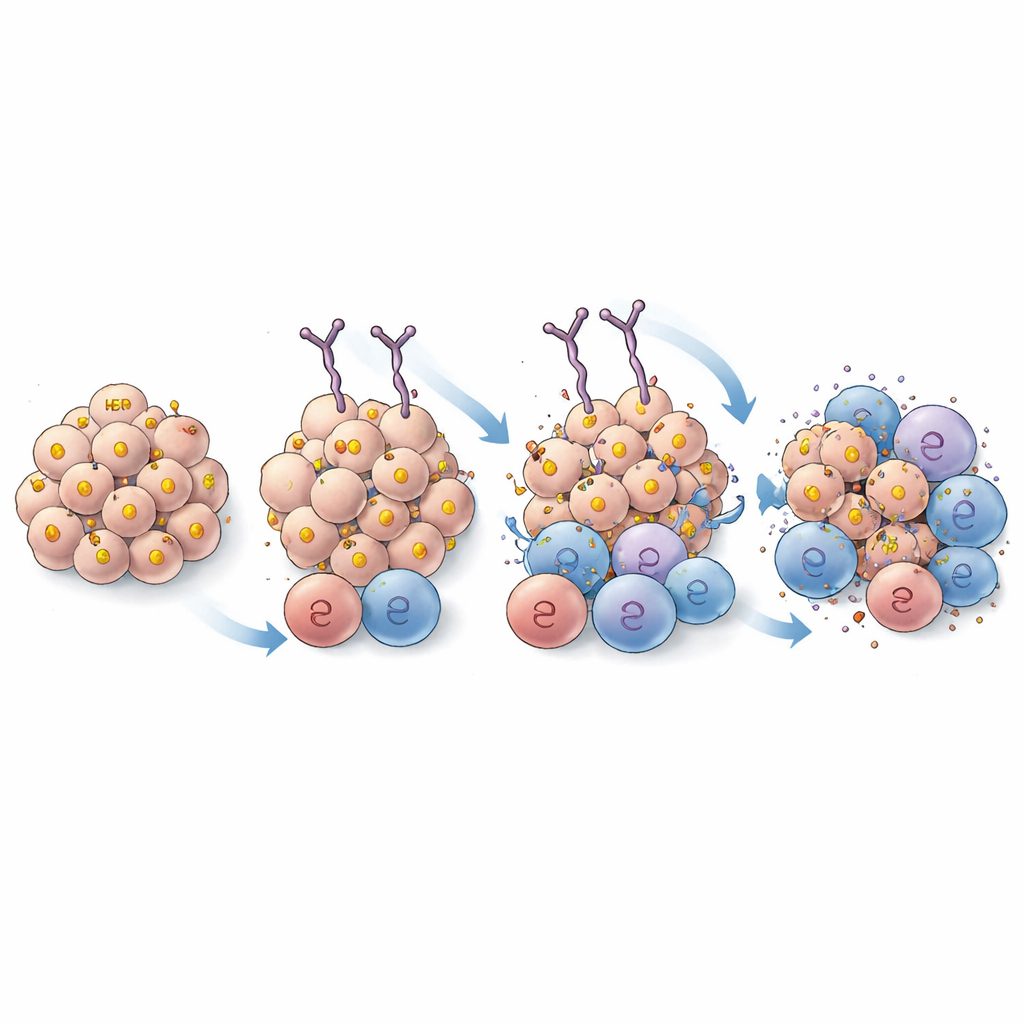
Esaminare nel dettaglio come si lega l’anticorpo
Per assicurarsi che i guadagni derivassero da una presa più forte piuttosto che dal riconoscere una nuova porzione di HER2, gli scienziati hanno utilizzato crio‑microscopia elettronica ad alta risoluzione per visualizzare come EPS 232 e l’originale EPS 226 si posizionano sulla proteina HER2. Le strutture hanno mostrato che entrambi gli anticorpi si legano alla stessa regione di HER2 e utilizzano punti di contatto molto simili, con solo differenze sottili che non dovrebbero alterare il sito di legame complessivo. Questo sostiene l’idea che la miglioria di EPS 232 derivi dall’aumento dell’affinità piuttosto che da un cambiamento del bersaglio.
Dal banco di laboratorio al controllo del tumore
La prova definitiva è arrivata nei modelli animali. In topi portatori di tumori mammari umani e dotati di cellule immunitarie umane, EPS 232 ha frenato la crescita tumorale in modo più efficace e a dosi inferiori rispetto a EPS 226. In ratti con un modello di cancro mammario aggressivo che esprime livelli ultra‑bassi di HER2 — simili ad alcuni tumori triple‑negativi — una versione adattata di EPS 232 per il ratto non solo ha rallentato la crescita tumorale più del suo predecessore, ma ha anche prolungato la sopravvivenza. I tumori degli animali trattati hanno mostrato una maggiore infiltrazione di cellule T e macrofagi, indicando che l’anticorpo migliorato riusciva meglio a rimodellare l’ambiente tumorale in favore di un attacco immunitario.
Cosa significa per le future terapie oncologiche
Per un lettore generale, il messaggio principale è che calibrare con precisione quanto intensamente una IgE afferri il suo bersaglio tumorale può fare una vera differenza sull’efficacia, anche se le IgE formano già molti contatti simultanei con le cellule. Lo studio identifica EPS 232 come un candidato IgE promettente contro i tumori mammari HER2‑positivi e HER2‑low, comprese forme che attualmente mancano di buone opzioni terapeutiche. Più in generale, dimostra che gli anticorpi «in stile allergico» possono essere ingegnerizzati con il giusto equilibrio di forza di legame per trasformare un sistema ipersensibile che normalmente provoca starnuti in uno che aiuta il sistema immunitario a individuare ed eliminare i tumori.
Citazione: Marano, F., McKenzie, C., Birtley, J.R. et al. Elucidating the relationship between affinity and potency in the performance of therapeutic IgE. Sci Rep 16, 10555 (2026). https://doi.org/10.1038/s41598-026-43772-6
Parole chiave: IgE terapeutiche, cancro al seno HER2, affinità degli anticorpi, immunoterapia del cancro, carcinoma mammario triple-negativo