Clear Sky Science · it
Verso una quantificazione ECV sintetica completamente automatizzata: un approccio open‑access basato su machine learning per una CMR rapida senza prelievo ematico
Perché è importante per la salute del cuore
I medici si affidano sempre più alle risonanze magnetiche cardiache per individuare precocemente le cicatrici nel muscolo cardiaco, una modifica subdola associata a molte malattie cardiache gravi. Oggi ottenere queste informazioni richiede tipicamente sia un’analisi delle immagini che richiede tempo sia un esame del sangue. Questo studio mostra che un computer può leggere automaticamente mappe speciali della risonanza cardiaca e stimare le stesse informazioni senza prelievo ematico, aprendo la strada a diagnostica cardiaca avanzata più rapida, confortevole e potenzialmente più accessibile.
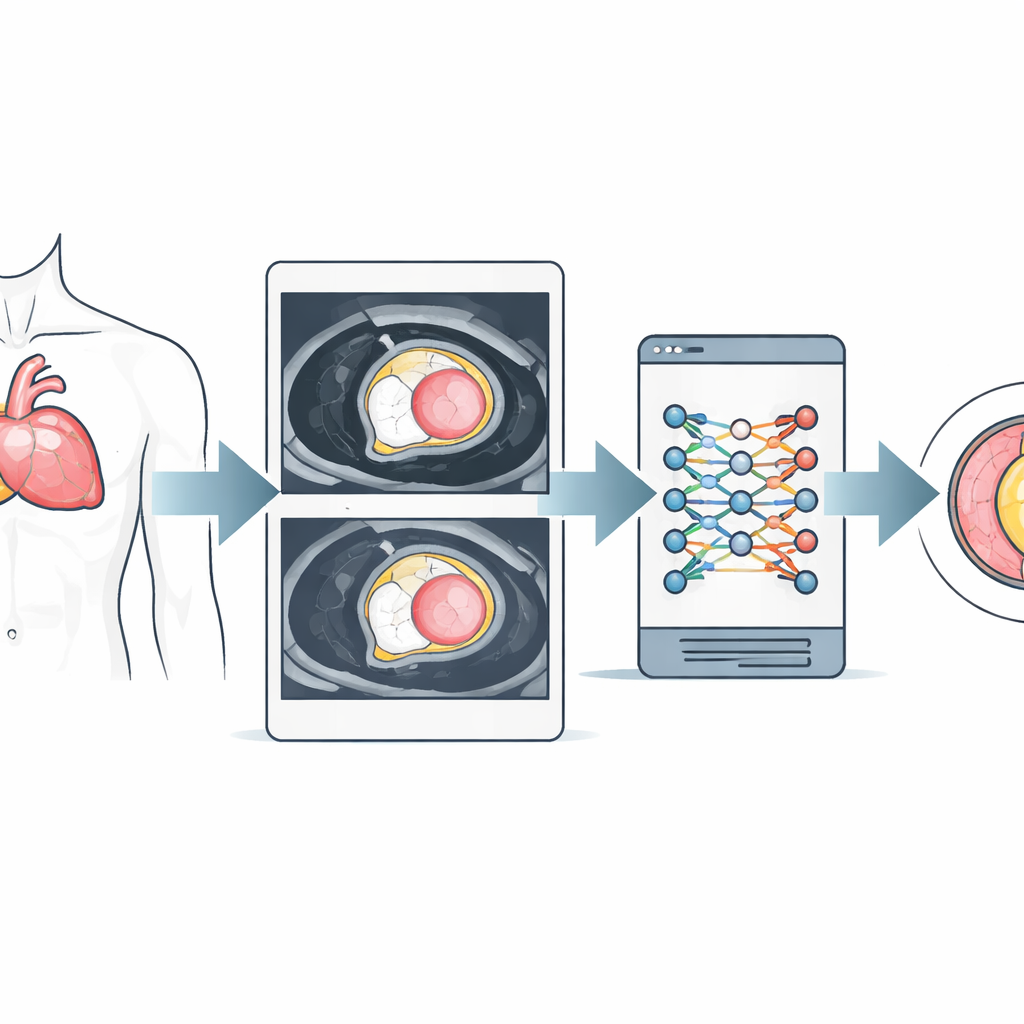
Vedere le cicatrici nascoste nel cuore
Molte condizioni cardiache croniche causano fibrosi—piccole aree di tessuto simile a cicatrice che irrigidiscono il muscolo cardiaco e peggiorano l’evoluzione a lungo termine. Le moderne risonanze magnetiche cardiache possono misurare il cosiddetto volume extracellulare (ECV), che riflette quanto del muscolo cardiaco è occupato da fluido e tessuto fibroso piuttosto che da cellule sane. L’ECV è diventato un potente marcatore di imaging per la fibrosi diffusa, ma la sua misurazione nella pratica è macchinosa. Di norma richiede il tracciamento manuale di regioni su più immagini RM, una correzione accurata del moto e un esame ematico recente per determinare l’ematocrito, la proporzione di globuli rossi nel sangue.
Il problema dei prelievi e del lavoro manuale
Negli ospedali reali, questo flusso operativo tradizionale è un collo di bottiglia. Non tutti i centri possono raccogliere un campione di sangue nello stesso momento della RM, e l’ematocrito stesso può variare per fattori semplici come la posizione del corpo. L’analisi delle immagini dipende inoltre da esperti formati, software specializzato e diversi passaggi manuali in cui gli operatori delineano le strutture cardiache fetta per fetta. Queste operazioni richiedono tempo e possono variare tra lettori o centri diversi, il che rende più difficile confrontare i risultati tra ospedali o in grandi studi di ricerca.
Insegnare a un computer a leggere le mappe cardiache
Basandosi su lavori precedenti che avevano mostrato come l’ematocrito possa essere stimato direttamente dal segnale RM nel compartimento sanguigno cardiaco, gli autori hanno messo a punto l’automazione del resto del processo. Hanno utilizzato dati RM di oltre 1000 pazienti esaminati a due diverse intensità di campo magnetico. Nella fase di addestramento, esperti hanno delineato con cura i contorni del muscolo cardiaco e delle cavità sanguigne su mappe T1 speciali acquisite prima e dopo l’iniezione di mezzo di contrasto. Questi esempi sono serviti per addestrare un modello di deep learning (una rete neurale di tipo U‑net) a trovare automaticamente le stesse strutture. L’algoritmo ha anche applicato passaggi di elaborazione delle immagini per separare il sangue dai tessuti circostanti e ridurre leggermente i bordi per evitare sfocature dovute al movimento.
Dalle scansioni grezze all’ECV sintetico in un unico step
Una volta addestrato, il modello è stato testato su un gruppo separato di pazienti. Per ciascuno ha misurato automaticamente i valori T1 tipici nel muscolo cardiaco e nel sangue, ha inserito quei valori in formule pubblicate che stimano l’ematocrito dalla sola RM e ha quindi calcolato un «ECV sintetico»—completamente senza prelievo ematico o contornamento manuale. I ricercatori hanno confrontato questo ECV sintetico completamente automatizzato con l’ECV convenzionale calcolato usando contorni esperti e ematocrito misurato in laboratorio. Nel complesso i due metodi hanno mostrato elevata concordanza: i valori medi erano quasi identici e la correlazione tra essi era forte. L’accordo è risultato particolarmente buono nell’intervallo clinicamente importante fino a circa il 35% di ECV, dove ricade la maggior parte dei pazienti.
Cosa ha funzionato bene e dove fatica
I contorni automatizzati sono stati generalmente valutati da specialisti indipendenti in imaging cardiaco come accettabili o eccellenti, e il modello ha gestito in modo affidabile immagini provenienti da entrambe le intensità di campo RM. Tuttavia, le differenze tra le misure automatizzate e quelle convenzionali aumentavano a valori di ECV molto elevati, un intervallo che spesso riflette malattia grave. Gli autori suggeriscono che ciò dipenda in parte dal fatto che casi tanto estremi erano rari nel dataset e in parte perché la qualità dell’immagine e anatomie complesse possono confondere l’algoritmo. Notano anche che il riferimento tradizionale utilizza una piccola regione nel setto cardiaco, mentre il metodo automatizzato fa la media sull’intera fetta, il che introduce naturalmente alcune differenze.
Cosa significa per il futuro
Per ora questo approccio va considerato soprattutto come uno strumento di ricerca più che come un sostituto clinico pronto all’uso. Rimane però la dimostrazione che un computer può prendere mappe cardiache standard pre‑ e post‑contrasto e, senza esame del sangue e con un contributo umano minimo, produrre valori di ECV che seguono da vicino le misurazioni odierne, laboriose, nella maggior parte dei pazienti. Poiché il codice e il modello addestrato sono disponibili pubblicamente, altri centri possono testare, affinare e adattare il metodo ai propri scanner. Se validato ulteriormente—specialmente in pazienti con ECV molto elevato—l’ECV completamente automatizzata e senza prelievo potrebbe rendere la valutazione della fibrosi avanzata più rapida, coerente e più ampiamente disponibile.
Citazione: Beyer, R.E., Hüllebrand, M., Doeblin, P. et al. Towards fully automated synthetic ECV quantification: an open-access machine learning-based approach for fast blood draw-free CMR. Sci Rep 16, 8552 (2026). https://doi.org/10.1038/s41598-026-43624-3
Parole chiave: risonanza magnetica cardiaca, fibrosi miocardica, volume extracellulare, deep learning, automazione nell’imaging medico