Clear Sky Science · it
La stratificazione per dose di prescrizione migliora la predizione delle dosi VMAT basata sul deep learning in NSCLC localmente avanzato
Perché i piani di radiazione più intelligenti sono importanti
Quando i medici trattano il cancro polmonare avanzato con la radioterapia, camminano su una sottile linea: somministrare energia sufficiente per controllare il tumore preservando al contempo gli organi sensibili vicini. Progettare questi piani è lento, complesso e dipende molto dall’esperienza del pianificatore. Questo studio esplora come l’intelligenza artificiale possa prevedere la distribuzione della dose nel torace e, cosa cruciale, dimostra che addestrare l’IA con livelli di dose raggruppati con cura rende le sue predizioni più accurate e clinicamente utili.
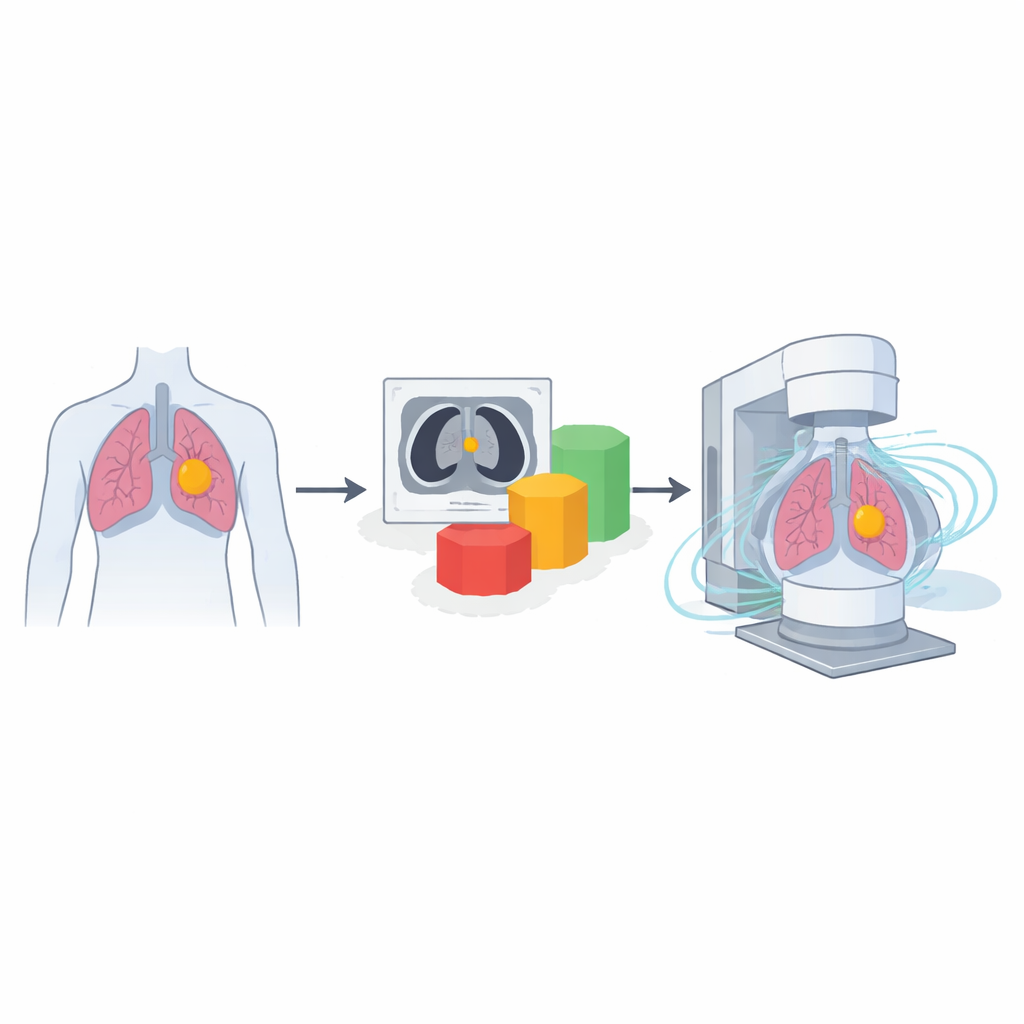
Come viene trattato il cancro polmonare con fasci concentrati
La maggior parte delle persone con carcinoma polmonare non a piccole cellule localmente avanzato non può sottoporsi a resezione chirurgica del tumore. Invece, spesso riceve chemioterapia insieme a fasci di radiazione altamente sagomati che ruotano intorno al torace in archi, una tecnica nota come VMAT. L’obiettivo è irradiare il tumore con una dose elevata e uniforme limitando l’esposizione ai polmoni, al cuore, all’esofago e al midollo spinale. Raggiungere questo equilibrio richiede generalmente molteplici cicli di tentativi e aggiustamenti, che consumano tempo e possono ritardare le decisioni sul trattamento. Se i medici potessero stimare rapidamente quale schema di dose è realisticamente ottenibile per un paziente, potrebbero scegliere prima la strategia di trattamento migliore.
Addestrare un algoritmo a riconoscere gli schemi di dose
I ricercatori si sono rivolti al deep learning, una forma di IA che apprende gli schemi direttamente dalle immagini. Hanno raccolto TAC e piani di trattamento completi di 72 pazienti con cancro polmonare trattati con VMAT. Per ciascun paziente hanno ricalcolato come lo stesso assetto di fasci avrebbe erogato tre diverse dosi totali: 50, 54 e 60 gray (Gy), le unità standard per le radiazioni. Ogni caso è stato convertito in una griglia tridimensionale che segnava il tumore, gli organi chiave e l’immagine TC sottostante. Questi nove canali di informazione sono stati forniti a una 3D U-Net, un’architettura di rete neurale comune che può imparare come la dose tende a distribuirsi nel corpo in base all’anatomia.
Perché la stratificazione per dose di prescrizione conta
Una domanda centrale era come gestire il fatto che i pazienti ricevono prescrizioni totali di dose differenti. Il team ha costruito quattro modelli di IA per il resto identici. Tre erano modelli “a singola prescrizione”, ciascuno addestrato solo su piani con un livello di dose (50, 54 o 60 Gy). Il quarto modello ha mischiato i casi da 50 e 60 Gy senza dire alla rete quale prescrizione stava vedendo. Quando testati su nuovi pazienti, i modelli specifici per prescrizione hanno fatto un lavoro migliore nel riprodurre la dose reale nel tumore, mantenendo copertura e picchi di dose vicini ai piani clinici, tipicamente entro pochi Gy. Al contrario, il modello misto ha commesso errori visibilmente maggiori nelle regioni a dose più alta del tumore e intorno al midollo spinale, dove la dose deve rimanere al di sotto di limiti di sicurezza rigorosi.
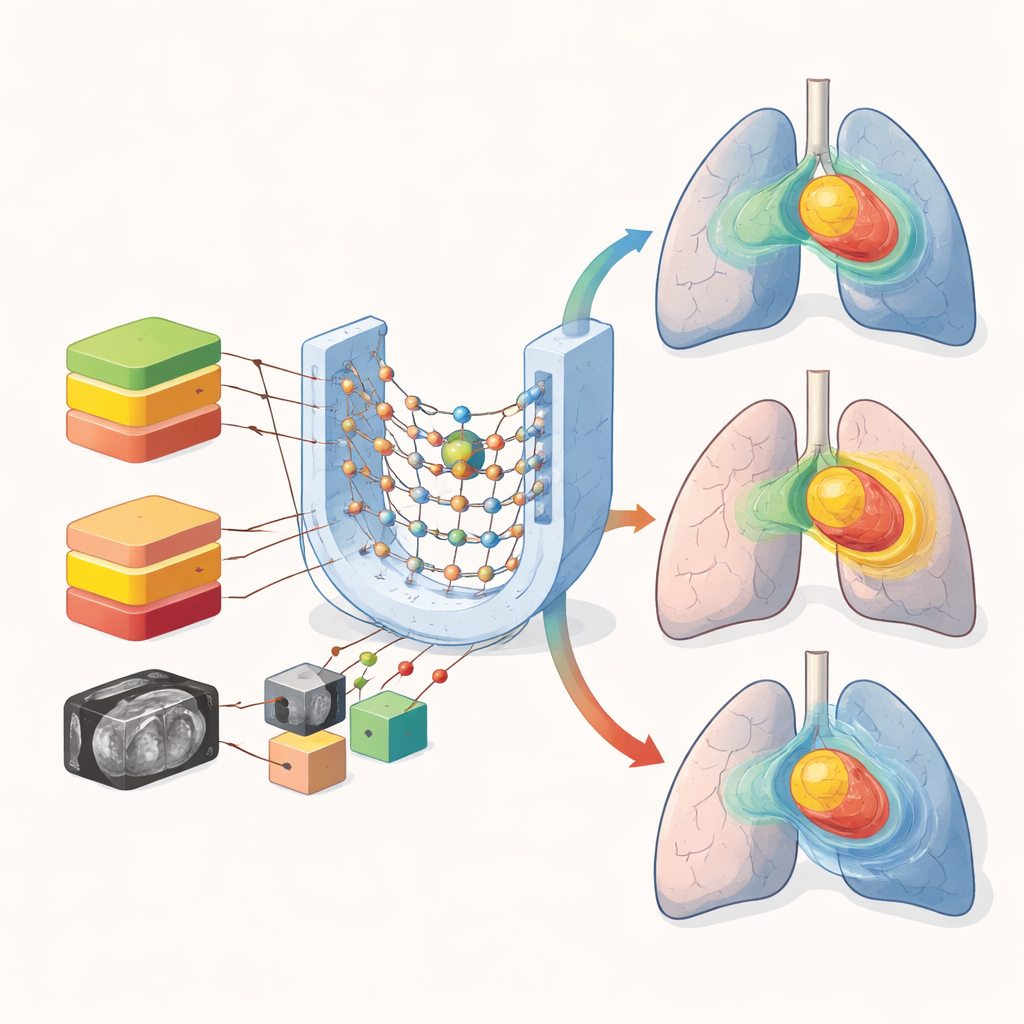
Proteggere gli organi vitali accelerando la pianificazione
Interessante notare che, per molti organi come polmoni, cuore ed esofago, i modelli misti e stratificati hanno mostrato prestazioni simili. Gli errori medi di dose per queste strutture più grandi sono rimasti contenuti in tutti gli approcci. La principale debolezza dell’unire prescrizioni è emersa in strutture piccole e sensibili come il midollo spinale, dove è essenziale un rapido calo della dose. Le verifiche visive delle mappe di dose previste hanno mostrato che tutti i modelli catturavano la forma generale della regione ad alta dose nel tumore, ma la miscelazione delle prescrizioni portava a un maggiore sfocamento nei gradienti netti e nelle aree a bassa dose dei polmoni. Queste differenze, sebbene sottili numericamente, possono diventare rilevanti quando i medici devono decidere se una prescrizione più elevata è sicura.
Cosa significa per i pazienti e le cliniche
Per i pazienti, questo lavoro non sostituisce i calcoli di dose accurati già eseguiti dai sistemi clinici, ma potrebbe aiutare a concentrare tempo e risorse su piani che sono davvero realizzabili e sicuri. Mostrando che raggruppare i dati di addestramento per dose di prescrizione affina in modo significativo le predizioni dell’IA—soprattutto per la copertura del tumore e la protezione del midollo spinale—lo studio evidenzia una scelta di progettazione pratica che può rendere l’assistenza computerizzata più affidabile. Con ulteriori test su gruppi di pazienti più numerosi e diversificati, tali modelli potrebbero diventare strumenti di uso quotidiano che offrono ai medici un’anteprima rapida, basata sull’anatomia, dei probabili compromessi radioterapici, supportando una pianificazione del trattamento migliore e più coerente.
Citazione: Chaipanya, T., Nimjaroen, K., Chamchod, S. et al. Prescription‑dose stratification improves deep learning‑based VMAT dose prediction in locally advanced NSCLC. Sci Rep 16, 8707 (2026). https://doi.org/10.1038/s41598-026-43192-6
Parole chiave: radioterapia del cancro polmonare, predizione della dose con deep learning, pianificazione VMAT, ottimizzazione dei piani di trattamento, organi a rischio