Clear Sky Science · it
I modelli dietetici influenzano la capacità in silico di produrre GABA di Bifidobacterium adolescentis HD17T2H e di altri batteri intestinali umani
Perché la tua cena potrebbe influire sul tuo umore
Molti hanno sentito dire che l'intestino è come un “secondo cervello”, ma resta poco chiaro come ciò che mangiamo plasmi quel mondo nascosto di microbi e, a sua volta, la nostra salute mentale e digestiva. Questo studio esplora un messaggero chiave, l'acido gamma-aminobutirrico (GABA), una molecola che attenua l'attività nervosa e viene prodotta non solo nel cervello ma anche da batteri intestinali. I ricercatori si sono posti una domanda apparentemente semplice: se si cambia la dieta, come varia la capacità dei microbi intestinali di produrre GABA?
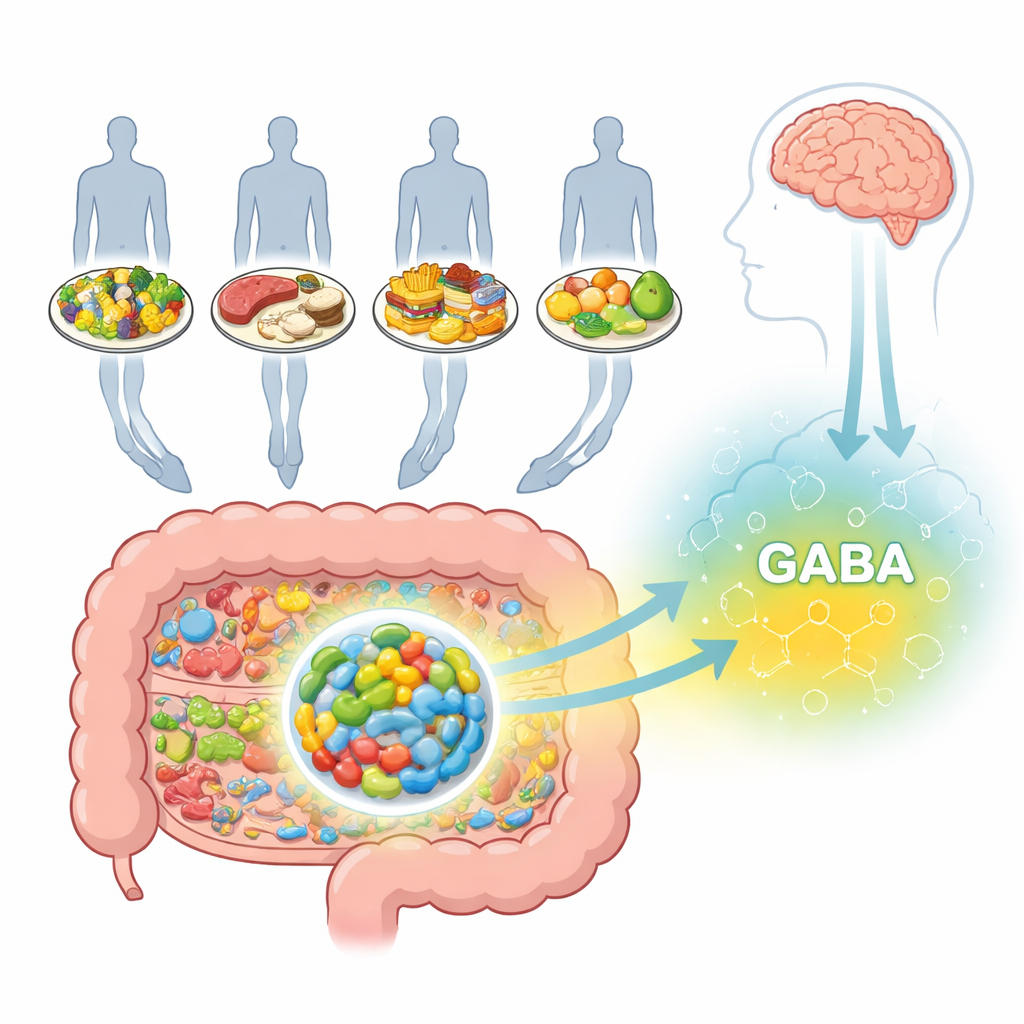
Una sostanza calmante prodotta nell’intestino
Il GABA è noto soprattutto come segnale inibitorio nel cervello, dove contribuisce a impedire che i neuroni diventino iperattivi ed è stato collegato a ansia e depressione. Ma il GABA è attivo anche nell'intestino, dove influenza il movimento intestinale, la secrezione di fluidi e il rilascio di ormoni. Alcuni batteri intestinali possono convertire nutrienti comuni in GABA tramite percorsi biochimici ben caratterizzati. Uno di questi microbi, Bifidobacterium adolescentis HD17T2H, è un produttore particolarmente efficace di GABA e appartiene a un gruppo di batteri spesso presenti nei prodotti probiotici. Tuttavia, fino ad ora gli scienziati non avevano un quadro sistematico di come diversi modelli alimentari possano modificare la capacità di questo batterio di produrre GABA.
Usare modelli al computer come un intestino virtuale
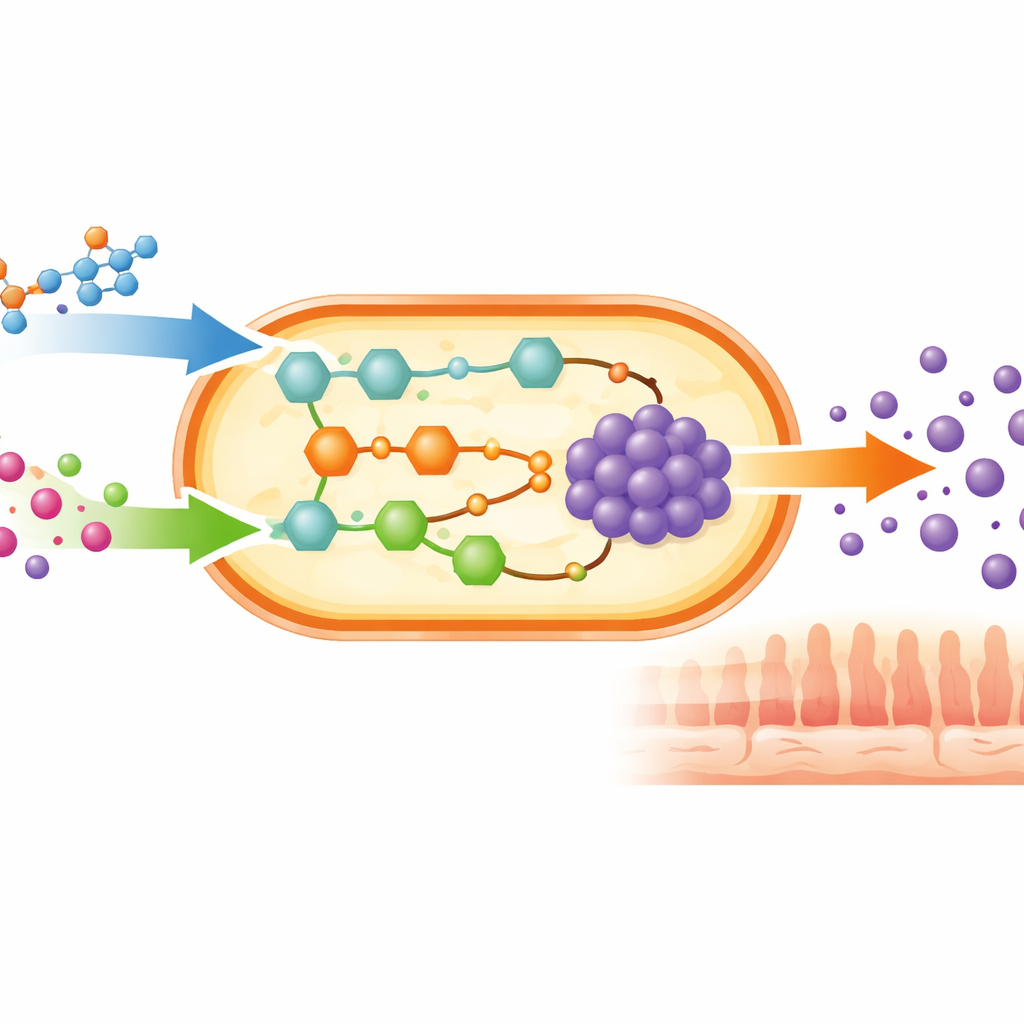
Invece di eseguire decine di esperimenti di laboratorio laboriosi, il team ha costruito un modello al computer dettagliato di B. adolescentis basato sul suo genoma. Hanno quindi “nutrito” questo microbo virtuale con undici diete realistiche giornaliere ricavate da un database nutrizionale, incluse diete vegetariane, vegane, ad alto contenuto proteico, la media europea, mediterranea, a basso contenuto di carboidrati e chetogenica. Con strumenti matematici che stimano come i nutrienti scorrono attraverso il metabolismo, i ricercatori hanno calcolato quanto GABA il batterio potrebbe in principio secernere sotto ciascuna dieta, mantenendo allo stesso tempo la crescita. Hanno anche eseguito migliaia di test virtuali di “integrazione”, aggiungendo in silico quantità extra di singoli nutrienti per vedere quali aumentavano maggiormente la produzione di GABA.
Come diverse diete modulano il potenziale di GABA
Le simulazioni hanno rivelato differenze marcate tra i modelli alimentari. In condizioni di base, una dieta vegetariana ha fornito il più alto potenziale di produzione di GABA per questo batterio, seguita da vicino da una dieta ad alto contenuto proteico e da una dieta pensata per il diabete di tipo 2. All'estremità opposta, un piano chetogenico, molto povero di carboidrati, ha prodotto il più basso output basale di GABA, con la dieta vegana anch'essa tra le più basse. Quando il team ha aumentato artificialmente l'apporto di singoli composti, due classi nutritive hanno ripetutamente potenziato la produzione di GABA: i carboidrati e le molecole ricche di azoto, in particolare gli amminoacidi. Nelle diete a basso contenuto di carboidrati, l'aggiunta di composti simili allo zucchero ha avuto l'effetto maggiore, suggerendo che l'energia carboniosa fosse il fattore limitante. Al contrario, nelle diete ricche di carboidrati come quelle vegetariane e vegane, amminoacidi extra e fonti azotate correlate hanno avuto l'impatto più forte, indicando che in quel contesto il collo di bottiglia era l'azoto.
Oltre un singolo batterio
Per capire come questi risultati possano tradursi negli esseri umani, i ricercatori hanno usato registri dietetici dettagliati di oltre mille adulti della coorte di Kiel. Per ciascuna persona, hanno calcolato quanto GABA la popolazione personale di B. adolescentis avrebbe teoricamente potuto produrre a partire dall'apporto di nutrienti dichiarato. Un approccio di machine learning ha confermato che gli amminoacidi sono di gran lunga i principali fattori alimentari, seguiti da altre molecole contenenti azoto, alcuni zuccheri, acidi grassi e vitamine del gruppo B che favoriscono l'attività enzimatica. Il team ha poi esteso la modellizzazione alle intere comunità microbiche della stessa coorte, utilizzando una vasta libreria di modelli di microbi intestinali. Hanno individuato 87 ceppi batterici appartenenti a 47 generi in grado di produrre GABA, includendo sia abitanti “buoni” sia potenziali patogeni, sottolineando che la produzione di GABA è una strategia di sopravvivenza diffusa nell'ecosistema intestinale piuttosto che un tratto di pochi microbi “benefici”.
Cosa significa per la salute e la ricerca futura
Complessivamente, lo studio mostra che la capacità dei batteri intestinali di produrre GABA è altamente sensibile alla dieta e che i nutrienti limitanti chiave dipendono dal modello alimentare complessivo: zuccheri ricchi di carbonio nei contesti a basso contenuto di carboidrati e blocchi di costruzione ricchi di azoto nei regimi ad alto contenuto di carboidrati. Questo non significa che le persone debbano aumentare il consumo di zuccheri o proteine per ottenere più GABA — diete ad alto contenuto di zucchero, per esempio, sono collegate a rischi per la salute e possono peggiorare i disturbi dell'umore nonostante eventuali effetti microbici. Piuttosto, il lavoro fornisce una mappa meccanicistica di quali nutrienti contano di più per la produzione microbica di GABA e mette in luce che molte specie intestinali, non solo i probiotici classici, possono contribuire a questa sostanza calmante. Studi di laboratorio e clinici futuri saranno necessari per verificare come queste intuizioni in silico si traducano in cambiamenti concreti nella funzione intestinale e cerebrale, e se diete o integratori progettati con cura possano sfruttare in modo sicuro la produzione microbica di GABA a beneficio della salute mentale e digestiva.
Citazione: Homscheid, A., Moors, K.A., Nap, B. et al. Dietary patterns influence the in silico GABA production capacity of Bifidobacterium adolescentis HD17T2H and other human gut bacteria. Sci Rep 16, 8961 (2026). https://doi.org/10.1038/s41598-026-43006-9
Parole chiave: microbiota intestinale, GABA, abitudini alimentari, Bifidobacterium adolescentis, asse intestino-cervello