Clear Sky Science · it
Esplorare il duplice ruolo delle vescicole extracellulari nella coagulazione e nella modulazione immunitaria nel glioblastoma
Perché i coaguli sono importanti nel cancro al cervello
Le persone diagnosticate con glioblastoma, la forma più aggressiva di tumore cerebrale, spesso affrontano un pericolo inatteso: coaguli di sangue pericolosi nelle gambe o nel cervello. Questi coaguli possono ridurre la sopravvivenza e complicare terapie già impegnative. Questo studio pone una domanda semplice ma cruciale: cosa c’è nelle cellule del glioblastoma che rende il sangue intorno a loro così incline alla coagulazione, e come le minuscole particelle che queste cellule rilasciano nel sangue rimodellano anche le difese immunitarie dell’organismo?
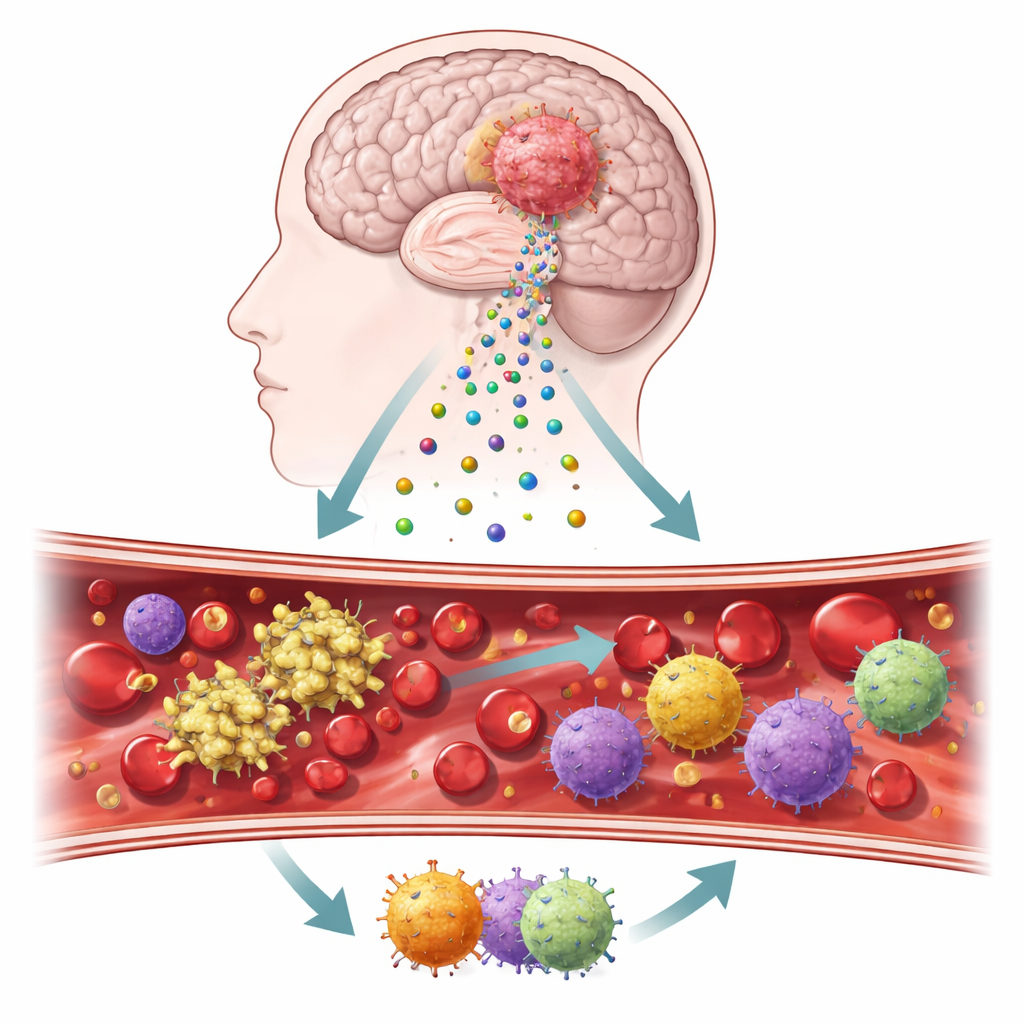
Piccoli messaggeri che lasciano un tumore cerebrale
I ricercatori si sono concentrati su bolle microscopiche chiamate vescicole extracellulari, che si staccano dalle cellule tumorali e fluttuano nel sangue e nel tessuto cerebrale. Queste vescicole portano sulla loro superficie due proteine chiave, il fattore tissutale e la podoplanina, note per innescare la formazione di coaguli e influenzare l’infiammazione. Utilizzando campioni tumorali, sangue raccolto durante l’intervento chirurgico e colture cellulari derivate dai tumori dei pazienti, il gruppo ha costruito un flusso di lavoro graduale per tracciare come questi elementi si comportano in pazienti reali e in test di laboratorio controllati. Hanno inoltre confrontato il tessuto tumorale con il cervello normale per valutare quanto fossero attivate queste segnali legati alla coagulazione.
Un flusso sanguigno tranquillo ma una zona tumorale predisposta
I test standard ospedalieri suggerivano che, prima dell’intervento, il sangue di molti pazienti appariva sorprendentemente normale: i tempi di coagulazione comuni e i valori di rigidità del coagulo erano per lo più nei range di riferimento. Tuttavia, quando gli scienziati hanno esaminato i tumori stessi è emerso un quadro diverso. Il tessuto del glioblastoma mostrava livelli costantemente elevati di fattore tissutale e podoplanina e livelli molto bassi di un freno naturale chiamato inibitore della via del fattore tissutale. Le linee cellulari tumorali derivate dai pazienti mantenevano in gran parte questo profilo in coltura, confermando che la firma “pro‑coagulante” è una caratteristica intrinseca delle cellule tumorali. Quando queste cellule, o le vescicole che rilasciavano, venivano miscelate con il plasma in laboratorio, i coaguli si formavano più rapidamente, soprattutto attraverso la cosiddetta via estrinseca che dipende dal fattore tissutale.
Diverse cellule tumorali, diverse strategie di coagulazione
Non tutti i glioblastomi si comportavano allo stesso modo. Alcune linee cellulari derivate dai pazienti avevano livelli molto alti di fattore tissutale, altre esprimevano più podoplanina, e alcune avevano poco di entrambi. Le cellule ricche di fattore tissutale erano le più efficaci nel ridurre il tempo di coagulazione, mentre le cellule ricche di podoplanina contribuivano in modo modesto tramite effetti sulle piastrine. Quando una di queste linee cellulari è stata separata in sottogruppi che esprimevano solo fattore tissutale, solo podoplanina, entrambi o nessuno dei due, le cellule non sono rimaste tali a lungo. Nell’arco di tre settimane sono tornate verso profili misti, rivelando un elevato grado di plasticità. Questo rimaneggiamento dinamico è stato accompagnato da cambiamenti nello stress ossidativo all’interno delle cellule, suggerendo che lo stress chimico nel tumore potrebbe spingere le cellule verso stati più pro‑coagulanti.
Le vescicole come plasmatori dell’immunità cerebrale e sanguigna
Il gruppo si è poi concentrato su come le vescicole derivate dal tumore influenzano le cellule immunitarie del cervello, chiamate microglia, e i globuli bianchi circolanti e i neutrofili. Le vescicole provenienti da linee tumorali altamente pro‑coagulanti venivano facilmente assorbite dalle microglia e rallentavano la loro migrazione, spingendole verso uno stato più infiammatorio, di tipo “M1”, e verso segni di invecchiamento cellulare. Nel sangue, le vescicole ricche di fattore tissutale attivavano i leucociti, aumentavano la produzione di specie reattive dell’ossigeno e favorivano il rilascio di strutture appiccicose a rete dai neutrofili note come trappole extracellulari. Le vescicole contenenti podoplanina erano meno potenti nel provocare queste reazioni immunitarie esplosive ma incentivavano fortemente un programma simile alla senescenza, in cui le cellule immunitarie smettono di dividersi e cambiano comportamento. Anche le vescicole prive di entrambe le proteine chiave potevano ancora indurre una certa senescenza, il che implica che anche altri carichi al loro interno sono importanti.
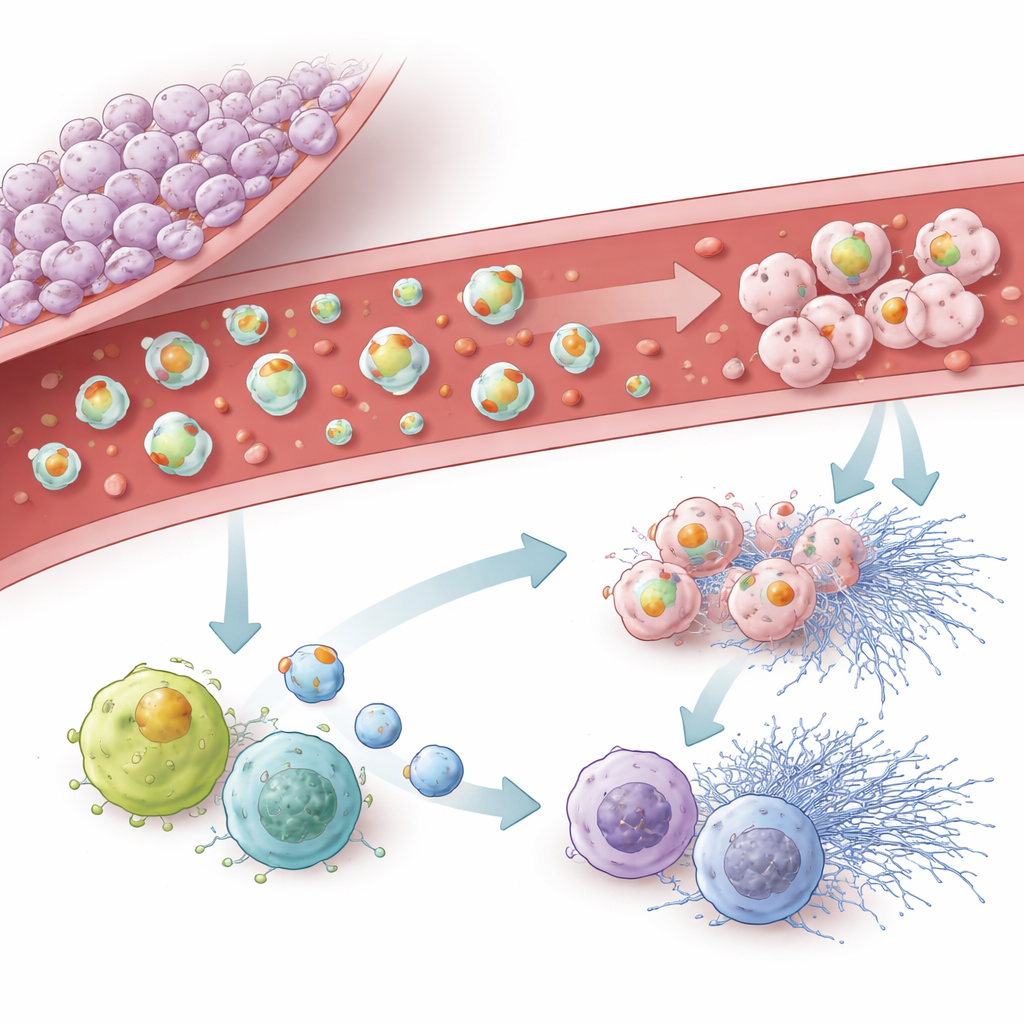
Cosa significa per i pazienti e per la cura futura
Complessivamente, i risultati mostrano che il glioblastoma non si limita ad addensare il sangue ovunque. Al contrario, il tumore e le vescicole che rilascia creano una zona localizzata e altamente complessa in cui coagulazione e infiammazione si alimentano a vicenda. Il fattore tissutale emerge come il principale motore della formazione del coagulo e dell’attivazione infiammatoria, mentre la podoplanina aggiunge la propria influenza sulle piastrine, sull’invecchiamento immunitario e sul comportamento delle microglia. Poiché queste vescicole circolano e rispecchiano lo stato del tumore, potrebbero fungere da futuri marcatori ematici per identificare i pazienti a rischio particolarmente elevato di coaguli. Potrebbero inoltre indicare strategie di prevenzione più mirate che prendano di mira la macchina pro‑coagulante del tumore senza assottigliare il sangue in modo generalizzato.
Citazione: Wolff, A., Waitz, G., Kaps, P. et al. Exploring the dual role of extracellular vesicles in coagulation and immune modulation in glioblastoma. Sci Rep 16, 9534 (2026). https://doi.org/10.1038/s41598-026-42867-4
Parole chiave: glioblastoma, coaguli sanguigni, vescicole extracellulari, microambiente tumorale, risposta immunitaria