Clear Sky Science · it
Valutazione del supporto dodecina di Mycobacterium tuberculosis come piattaforma di multimerizzazione sull’immunogenicità degli antigeni L2 di HPV
Perché questa ricerca è importante per i vaccini futuri
I papillomavirus umani (HPV) causano quasi tutti i tumori della cervice uterina e una quota crescente di altri tumori, ma i vaccini attuali sono complessi da produrre e non coprono completamente tutti i tipi virali pericolosi. Questo studio esplora un nuovo modo di costruire un vaccino anti-HPV più semplice e più ampiamente protettivo, potenzialmente più economico, più stabile e più facile da usare nel mondo, in particolare nei paesi a basso e medio reddito. Riorganizzando il modo in cui frammenti chiave delle proteine virali vengono presentati al sistema immunitario, i ricercatori mirano a stimolare la produzione di anticorpi potenti contro molti tipi di HPV contemporaneamente.
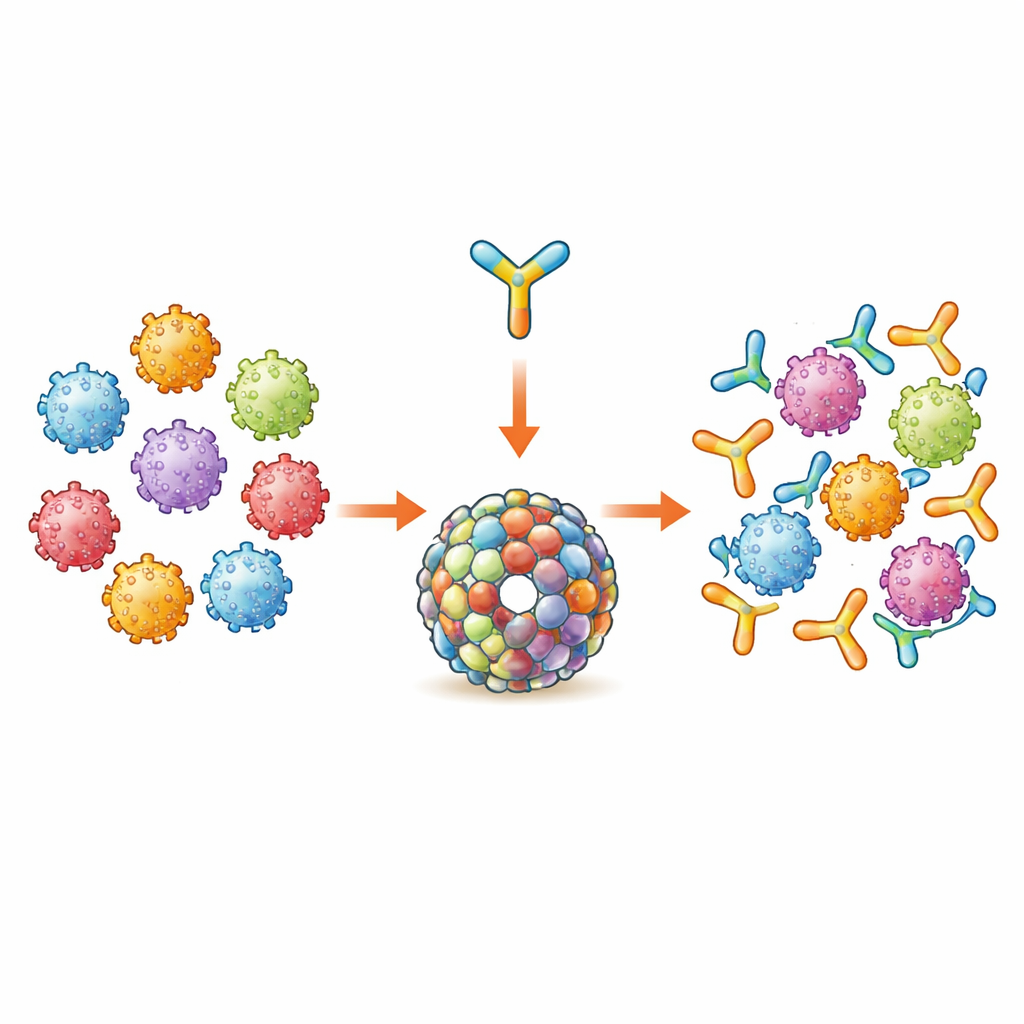
Un nuovo mattone per la protezione contro HPV
Le vaccinazioni anti-HPV odierne si basano sulla proteina del capside virale chiamata L1, assemblata in particelle simili al virus che stimolano fortemente la produzione di anticorpi ma principalmente contro i pochi tipi di HPV inclusi in ciascun vaccino. Il team si è invece concentrato su una seconda proteina virale, L2, che contiene brevi regioni simili tra molti tipi di HPV e che può pertanto indurre una protezione più ampia. Hanno utilizzato un antigene precedentemente progettato chiamato Trx-8mer, in cui piccoli frammenti conservati di L2 provenienti da otto tipi di HPV sono cuciti insieme e mostrati su una proteina vettore stabile. Lavori precedenti avevano già dimostrato che raggruppare sette di queste unità Trx-8mer in un complesso ad anello (un vaccino chiamato PANHPVAX) produce forti risposte anticorpali cross-protettive ed è ora in sperimentazione umana in fase iniziale.
Trasformare una proteina batterica in una piattaforma vaccinale
In questo studio i ricercatori hanno provato ad andare oltre le sette copie e a inserire ancora più antigeni L2 in ciascuna particella, sulla base della teoria che modelli altamente ripetitivi sono particolarmente efficaci nell’attivare le cellule B, produttrici di anticorpi. Hanno scelto una piccola proteina termoresistente del batterio della tubercolosi, chiamata dodecina, che si assembla naturalmente in sfere cave composte da dodici subunità identiche. Fusando geneticamente Trx-8mer alla dodecina, hanno creato diversi nuovi candidati vaccinali progettati per autoassemblarsi in nanoparticelle multimeriche che mostrano molte copie di L2. Queste particelle possono essere prodotte in batteri, purificate ad alte temperature grazie alla loro robustezza e verificate con vari metodi biofisici per confermare la formazione delle strutture nanoscalari previste.
Quando la fusione diretta non basta
Sorprendentemente, attaccare semplicemente il carico L2 direttamente al supporto di dodecina non ha superato il vaccino di riferimento eptamerico PANHPVAX nei topi. Sebbene le particelle multimeriche si siano formate come previsto e abbiano indotto anticorpi neutralizzanti contro tipi HPV presenti e non presenti nel vaccino, i titoli sono risultati generalmente inferiori rispetto a quelli ottenuti con PANHPVAX. L’aggiunta di un epitopo ausiliario per le cellule T integrato, che a volte potenzia le risposte anticorpali, non ha migliorato le prestazioni. La modellazione strutturale e i dati funzionali hanno suggerito che unità Trx-8mer voluminosi e direttamente fusi potrebbero ingombrarsi a vicenda e nascondere regioni critiche di L2 ai recettori delle cellule B, attenuando la risposta immunitaria nonostante una maggiore presenza teorica di copie di antigene.
La decorazione click-on aumenta dramaticamente le risposte
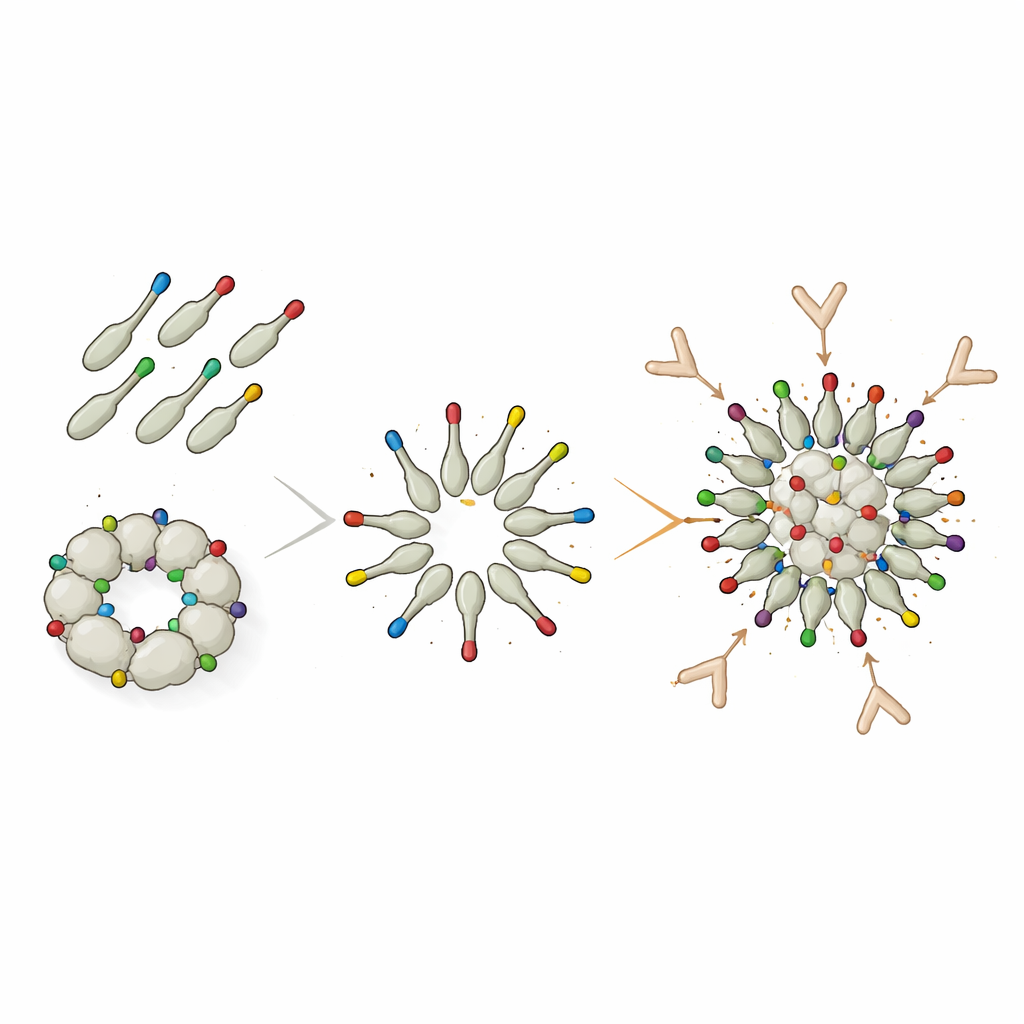
Per superare questi vincoli strutturali, il gruppo ha adottato un sistema modulare di “colla proteica” chiamato DogTag/DogCatcher. In questo progetto, la dodecina è stata prodotta inizialmente con solo un piccolo peptide DogTag sulla sua superficie, permettendole di assemblarsi liberamente in nanoparticelle pulite. Separatamente, l’antigene Trx-8mer è stato fuso con la controparte DogCatcher corrispondente. Mescolando le due componenti, Tag e Catcher si legano tramite un legame covalente spontaneo, fissando le unità Trx-8mer portatrici di L2 sulle particelle di dodecina preformate. Anche se solo circa la metà dei Trx-8mer risultava attaccata alle nanoparticelle e il resto rimaneva libero in soluzione, i topi immunizzati con questa costruzione decorata hanno prodotto titoli di anticorpi neutralizzanti molto più alti contro diversi tipi di HPV ad alto rischio rispetto alle particelle a fusione diretta. Per alcuni tipi, come HPV16, le particelle decorate hanno persino superato PANHPVAX.
Implicazioni per vaccini HPV ampi ed economici
Nel complesso, lo studio mostra che il modo in cui gli antigeni sono disposti nello spazio può contare più del semplice numero di copie presente sulla carta. Pre-assemblare un robusto scaffold nanoparticellare e poi fissarvi gli antigeni ha garantito ai frammenti L2 un migliore spaziamento e orientamento, portando a risposte anticorpali più forti e più ampie nei topi. Poiché le particelle a base di dodecina sono piccole, altamente termostabili e prodotte in batteri, rappresentano candidati promettenti per vaccini anti-HPV di nuova generazione che potrebbero essere più economici da fabbricare e meno dipendenti dalla catena del freddo. Con ulteriori ottimizzazioni e test, questa piattaforma modulare potrebbe supportare vaccini in grado di proteggere contro molti tipi di HPV in un’unica iniezione accessibile, e potrebbe persino essere adattata per combinare componenti preventivi e terapeutici nella stessa nanoparticella.
Citazione: Kaplan, E., Mariz, F.C., Zhao, X. et al. Assessment of Mycobacterium tuberculosis dodecin scaffold as a multimerization platform on the immunogenicity of HPV L2 antigens. Sci Rep 16, 9086 (2026). https://doi.org/10.1038/s41598-026-42678-7
Parole chiave: vaccino contro HPV, immunogeno nanoparticellare, antigene L2, supporto dodecina, coniugazione proteica