Clear Sky Science · it
Studio clinicopatologico multicentrico delle lesioni dello spettro del mixoma odontogenico mediante patologia quantitativa
Perché è importante per pazienti e dentisti
In profondità nell’osso mascellare, tumori rari possono crescere silenziosamente per mesi o anni prima di essere scoperti. Queste formazioni, chiamate mixomi odontogenici e mixofibromi odontogenici, non sono tumori maligni, ma possono espandersi, indebolire l’osso e complicare l’intervento chirurgico. Per decenni i patologi li hanno valutati in gran parte a occhio, portando a differenze nel modo in cui gli ospedali descrivono e classificano lo stesso tipo di lesione. Questo studio porta potenti strumenti di analisi delle immagini al vetrino, mostrando come l’intelligenza artificiale (IA) possa aiutare i medici a vedere questi tumori in modo più chiaro e coerente.
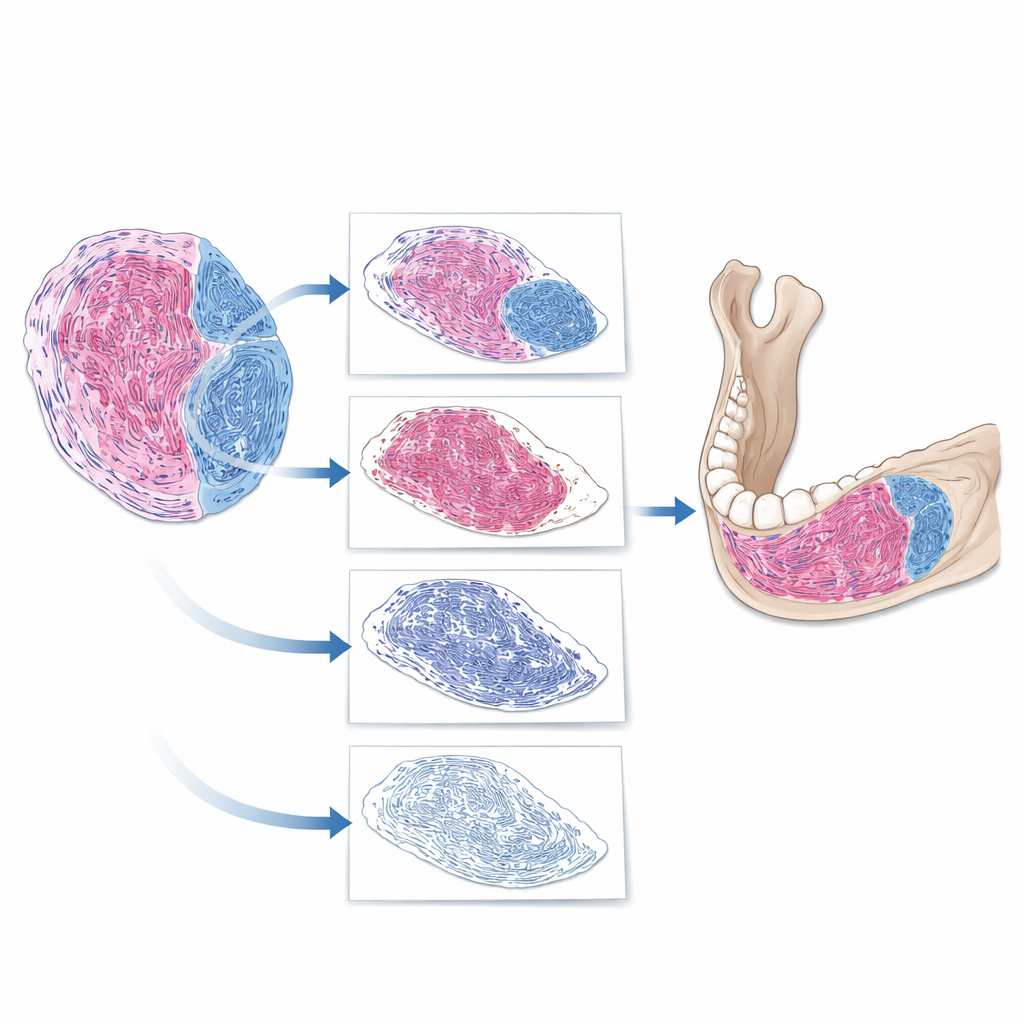
Tumori mandibolari rari che sembrano sorprendentemente simili
Il mixoma odontogenico e il mixofibroma odontogenico originano dai tessuti coinvolti nella formazione dei denti. Entrambi sono tumori morbidi, di consistenza gelatinosa, che si trovano all’interno dell’osso mascellare. Al microscopio contengono una miscela di aree lassi, di tipo mixoide, e fasci più densi di tessuto fibroso. Tradizionalmente i patologi hanno cercato di distinguerli stimando quanto del tumore sia fibroso rispetto alla componente mixoide. Ma questi tumori sono rari e non esistono regole universalmente concordate su quale percentuale di tessuto fibroso sia sufficiente per spostare la diagnosi da un’etichetta all’altra. Di conseguenza, diversi ospedali possono assegnare nomi diversi a lesioni molto simili, anche quando i pazienti presentano sintomi e reperti radiografici comparabili.
Trasformare i vetrini in numeri
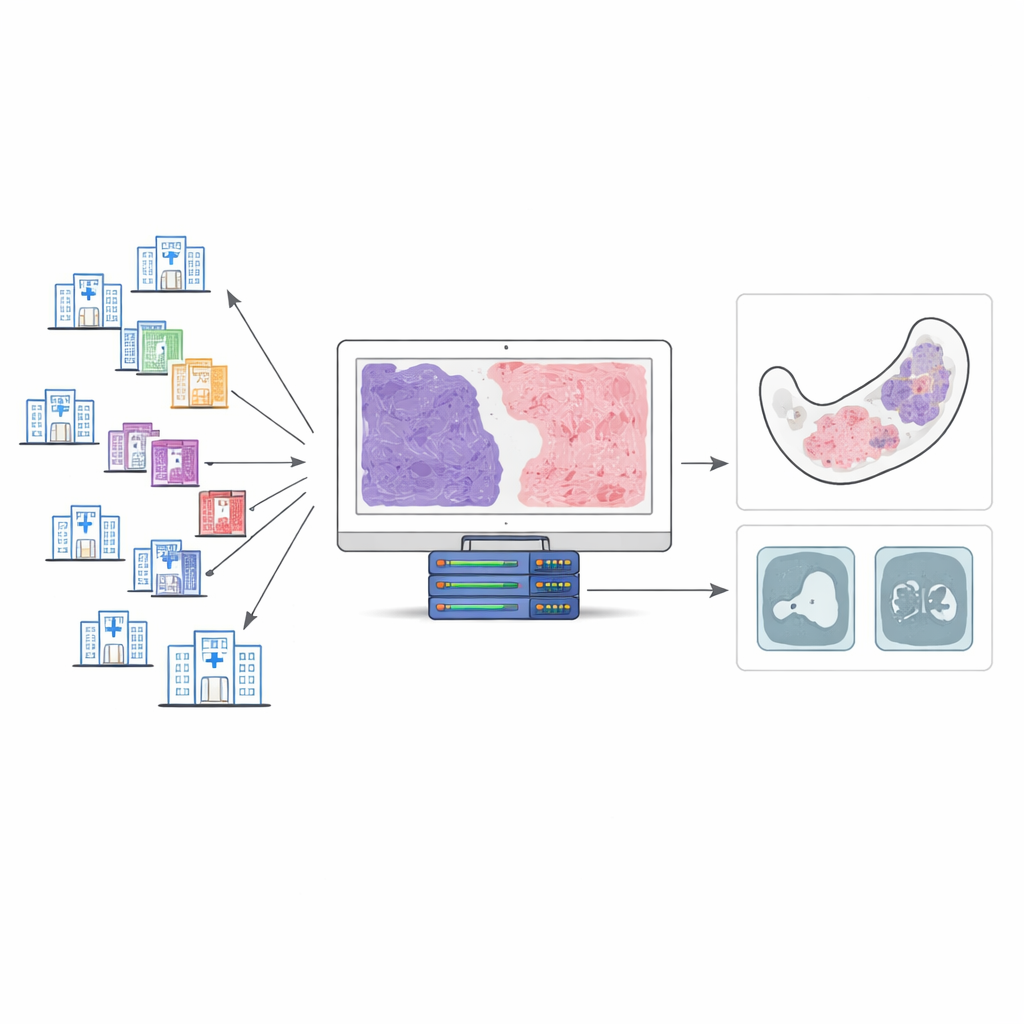
Il team di ricerca ha raccolto 143 campioni tissutali da pazienti trattati in 34 ospedali nell’arco di due decenni, concentrandosi infine su 100 casi che soddisfacevano rigidi criteri di qualità. Tutti i campioni sono stati colorati con un colorante speciale (tricromico di Masson) che colora in modo diverso il tessuto fibroso rispetto al tumore circostante. Due esperti patologi orali hanno esaminato attentamente ogni caso e stimato la percentuale di tessuto fibroso in step del 10%. Queste stime degli esperti hanno fatto da riferimento per addestrare un sistema di IA a svolgere lo stesso compito automaticamente, ma in modo pienamente quantitativo.
Come l’IA “legge” un vetrino tumorale
Il team ha costruito una pipeline digitale passo dopo passo per analizzare immagini dell’intero vetrino. Per prima cosa il software ha separato il vero tessuto dallo sfondo vuoto del vetrino. Poi ha isolato il tumore dalle strutture vicine, come osso e denti. Infine, all’interno del tumore, ha rimosso i nuclei cellulari e si è concentrato sul materiale rimanente, identificando le regioni che avevano assorbito la colorazione del tessuto fibroso. A partire da questo, l’IA ha calcolato una proporzione di tessuto fibroso: l’area di tessuto fibroso divisa per l’area tumorale totale. Quando i ricercatori hanno confrontato i valori generati dall’IA con le valutazioni degli esperti, l’accordo è risultato solido, con solo circa 10 punti percentuali di variabilità nella maggior parte dei singoli casi. Ciò suggerisce che l’IA può rispecchiare in modo affidabile il giudizio degli specialisti, esprimendolo però come misurazioni precise invece che come impressioni approssimative.
Cosa rivela la composizione fibrosa sull’aspetto del tumore
Muniti di queste misurazioni, i ricercatori hanno esaminato come il contenuto fibroso si relazionasse alle caratteristiche cliniche e radiologiche. Hanno scoperto che la quantità di tessuto fibroso variava ampiamente tra le istituzioni, riflettendo le differenze nel modo in cui i patologi avevano originariamente etichettato i tumori. Analizzando le caratteristiche d’imaging, è emerso un pattern: i tumori che apparivano come una singola cavità nelle scansioni (lesioni uniloculate) tendevano ad avere una proporzione più elevata di tessuto fibroso rispetto a quelli con molte piccole compartimentazioni (lesioni multiloculate). Questo si concilia con l’idea che un tessuto più fibroso e denso possa formare una massa più solida e a una sola camera, mentre un tessuto più lasso e ricco di fluido possa frammentarsi in più spazi.
Cosa significa per la diagnosi e l’assistenza future
Lo studio non intende rinominare le malattie né sostituire i patologi con le macchine. Mostra invece che la patologia quantitativa basata sull’IA può fornire un metro di misura condiviso per tumori mandibolari rari in molti ospedali. Trasformando le trame sottili del tessuto tumorale in numeri riproducibili, questo approccio mette in luce quanto le diagnosi quotidiane dipendano dal giudizio soggettivo e offre un modo per ridurre quella variabilità. Per i pazienti, un’interpretazione più coerente di queste lesioni potrebbe sostenere decisioni terapeutiche più chiare e un confronto migliore degli esiti tra centri. Man mano che metodi simili vengono estesi ad altri tumori rari, la microscopia assistita dall’IA potrebbe, silenziosamente, rimodellare il modo in cui i patologi osservano le malattie—rendendo le loro valutazioni più comparabili e, in definitiva, più utili, ovunque il paziente venga curato.
Citazione: Harazono, Y., Fukawa, Y., Iwasaki, T. et al. Multicenter clinicopathological study of odontogenic myxoma spectrum lesions using quantitative pathology. Sci Rep 16, 11221 (2026). https://doi.org/10.1038/s41598-026-42019-8
Parole chiave: mixoma odontogenico, tumori della mandibola, patologia digitale, intelligenza artificiale, proporzione di tessuto fibroso