Clear Sky Science · it
Analisi genetica degli attori chiave nella cascata di segnalazione PI3K del carcinoma colorettale
Perché i tuoi geni contano per la salute del colon
Il carcinoma colorettale è uno dei tumori più comuni e letali a livello mondiale, e la sua incidenza sta aumentando in molti Paesi che attraversano rapidi cambiamenti nello stile di vita. Tuttavia, non tutti con abitudini o diete simili affrontano lo stesso rischio. Questo studio pone una domanda semplice ma potente: differenze ereditarie in geni chiave del controllo della crescita possono spiegare chi sviluppa il carcinoma colorettale, quanto diventa aggressivo e quanto bene funzionano i farmaci standard—soprattutto in un ampio gruppo di pazienti pakistani, una popolazione finora poco studiata?
Una trafficata linea di controllo dentro le nostre cellule
Le cellule dell’intestino ricevono costantemente segnali che indicano quando crescere, dividersi o autodistruggersi. Una delle vie di comunicazione più attive è la via PI3K–AKT–mTOR—una cascata di interruttori molecolari che promuove la crescita cellulare, la sopravvivenza, la formazione di nuovi vasi e la resistenza alla morte cellulare. Quando questa via è iperattiva, le cellule possono iniziare a moltiplicarsi in modo incontrollato e formare tumori. I geni PIK3CA, AKT1 e mTOR si trovano in punti di controllo cruciali lungo questa via. Sottili variazioni ereditarie in questi geni, chiamate polimorfismi a singolo nucleotide (SNP), e modifiche più forti note come mutazioni “hotspot” possono spostare l’equilibrio verso il cancro o alterare la risposta dei tumori ai trattamenti.
Scansionare il DNA di pazienti e volontari sani
Per esplorare questo, i ricercatori hanno condotto uno studio caso‑controllo che ha incluso 495 persone con carcinoma colorettale e 495 volontari sani senza cancro, abbinati per età e sesso. Campioni di sangue hanno fornito il DNA, esaminato per sette SNP distribuiti su PIK3CA, AKT1 e mTOR, insieme a due ben note mutazioni hotspot chiamate E542K (in PIK3CA) ed E17K (in AKT1). Usando metodi PCR mirati e sequenziamento del DNA, il team ha confrontato la frequenza di ciascuna variante genetica nei pazienti rispetto ai controlli e ha quindi collegato questi schemi a caratteristiche cliniche come età, storia familiare, malattia intestinale, stadio del tumore e schemi terapeutici ricevuti dai pazienti. 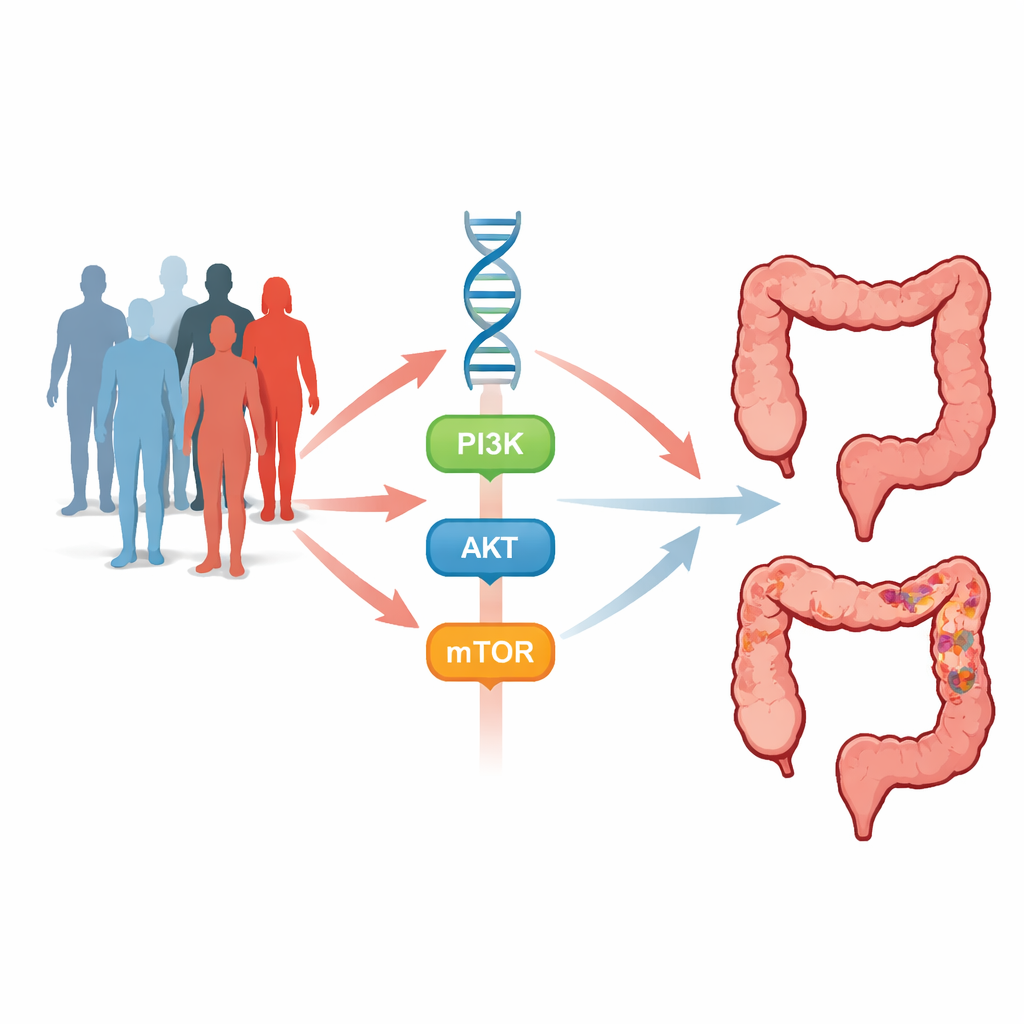
Varianti a rischio e mutazioni potenti
L’analisi ha rivelato che la maggior parte delle varianti testate era molto più comune nelle persone con carcinoma colorettale rispetto ai controlli sani, suggerendo fortemente che contribuiscono al rischio di malattia. Diverse varianti di AKT1 e mTOR, in particolare, hanno mostrato frequenze significativamente più alte nei pazienti, mentre alcune versioni “normali” di questi geni erano più comuni nei controlli, suggerendo un ruolo protettivo. Le mutazioni hotspot hanno raccontato una storia ancora più netta: la sostituzione E542K in PIK3CA è comparsa in circa il 15% dei pazienti, e la E17K in AKT1 in circa il 29%, entrambe molto più frequenti che nei controlli. La modellizzazione computazionale ha indicato che queste mutazioni non deformano drasticamente la forma complessiva della proteina ma sembrano invece bloccare la via in uno stato più “attivato”, generando segnali di crescita continui che favoriscono lo sviluppo tumorale.
Dai geni al trattamento e alla sopravvivenza
La genetica da sola non agisce in isolamento, quindi i ricercatori hanno investigato come queste varianti interagiscono con fattori di rischio e terapie del mondo reale. Molti degli SNP sono stati collegati al fumo, alle malattie infiammatorie intestinali, alla storia familiare, al tipo e stadio di cancro e al fatto che i pazienti avessero ricevuto chemioterapia o radioterapia. Seguendo i pazienti nel tempo, il team ha scoperto che alcune versioni geniche erano associate a una sopravvivenza globale migliore o peggiore. Per esempio, le persone portatrici delle versioni “normali” di diverse varianti di AKT1 e mTOR tendevano a vivere più a lungo rispetto a chi aveva le versioni ad alto rischio. Lo studio ha anche confrontato la sopravvivenza tra pazienti trattati con combinazioni farmacologiche comuni. La capecitabina, una compressa chemioterapica ampiamente usata, è risultata associata alle migliori stime di sopravvivenza, e diverse varianti della via sembravano influenzare l’efficacia dei diversi regimi, suggerendo che la genetica ereditaria potrebbe guidare scelte terapeutiche più personalizzate. 
Come le variazioni viaggiano insieme
Oltre alle singole varianti, gli autori hanno esaminato come gruppi di cambiamenti tendano a essere ereditati insieme—un modello noto come disequilibrio di linkage. Hanno scoperto un blocco di varianti vicine che copre PIK3CA e AKT1 che venivano ereditate insieme più spesso nei pazienti che nei controlli. Questo suggerisce che combinazioni di piccole differenze del DNA lungo la via PI3K possano congiuntamente modellare il rischio di base di una persona e il comportamento di un tumore, piuttosto che una singola modifica agire da sola.
Cosa significa per i pazienti e la medicina di precisione
Per il lettore non specialistico, la conclusione è che questo lavoro rafforza l’idea che “taglia unica” è un modello inadeguato per la cura del carcinoma colorettale. In questa coorte pakistana, specifiche varianti ereditarie e mutazioni hotspot nei geni di controllo della crescita sono chiaramente correlate al rischio di cancro, alle caratteristiche del tumore e alla sopravvivenza, e sembrano persino modulare la risposta dei pazienti alla chemioterapia standard. Sebbene questi risultati debbano essere confermati in gruppi più grandi e più diversi, indicano un futuro in cui un semplice esame del sangue per le varianti PI3K–AKT–mTOR potrebbe aiutare a identificare chi è a rischio maggiore, segnalare quali pazienti potrebbero beneficiare di farmaci specifici e risparmiare ad altri trattamenti inefficaci o inutilmente tossici.
Citazione: Pervaiz, H., Masood, N., Malik, P.A. et al. Genetic analysis of key players in PI3K signaling cascade of colorectal carcinoma. Sci Rep 16, 11317 (2026). https://doi.org/10.1038/s41598-026-42006-z
Parole chiave: genetica del cancro colorettale, via PI3K AKT mTOR, polimorfismi a singolo nucleotide, oncologia di precisione, risposta alla chemioterapia