Clear Sky Science · it
Analisi delle vescicole extracellulari derivate dalle cellule epiteliali bronchiali mediante citometria a flusso convenzionale, di imaging e nanoscalare
Perché le bollicine microscopiche nei polmoni contano
I nostri polmoni sono rivestiti da cellule che comunicano costantemente con il sistema immunitario, soprattutto quando inspiriamo polvere, inquinamento o germi. Gran parte di questa “conversazione” avviene tramite bolle microscopiche chiamate vescicole extracellulari: pacchetti di lipidi e proteine rilasciati dalle cellule. Queste vescicole possono peggiorare o attenuare le malattie polmonari e, un giorno, potrebbero fungere da segnali di allerta precoce per condizioni come asma, broncopneumopatia cronica ostruttiva (BPCO) e fibrosi. Questo studio esplora come misurare al meglio queste particelle elusive usando diversi tipi di strumenti laser avanzati, con l’obiettivo di rendere tali misurazioni praticabili per la ricerca e per futuri test clinici.
Messaggi invisibili dalle cellule delle vie aeree
Le vescicole extracellulari (EV) sono piccoli pacchetti avvolti da membrana rilasciati da quasi tutte le cellule in fluidi come sangue, urina e il sottile film liquido che riveste le vie respiratorie. Le EV derivate dalle cellule epiteliali bronchiali umane—le cellule che rivestono i condotti respiratori—sono già state associate a diversi processi polmonari: possono influenzare lo sviluppo di allergie, contribuire alla difesa contro le infezioni polmonari, modellare la struttura delle vie aeree nella BPCO e persino limitare la formazione di cicatrici nel tessuto polmonare. Poiché trasportano frammenti di proteine, lipidi e materiale genetico dalla cellula madre, le EV potrebbero funzionare come impronte digitali della salute o della malattia polmonare e, in futuro, essere impiegate anche come terapie. La sfida è che sono estremamente piccole, molto eterogenee e presenti in quantità ridotte, il che rende difficile vederle e contarle con precisione.
Oltre test lenti e frammentati
Tradizionalmente, gli scienziati hanno fatto affidamento su diversi metodi separati per studiare le EV. L’ultracentrifugazione o la cromatografia a esclusione dimensionale vengono utilizzate per isolarle; l’analisi del tracciamento delle nanoparticelle misura il loro movimento per stimare dimensione e numero; e i microscopi elettronici forniscono immagini dettagliate. Pur essendo potenti, questi approcci sono lenti, richiedono molto lavoro e non sono ideali per l’uso di routine o clinico. Crucialmente, sono poco efficaci nell’indicare quali specifiche proteine porta ciascuna vescicola. La citometria a flusso—una tecnologia ampiamente usata per analizzare sangue e cellule immunitarie—offre un’alternativa più snella. Fa passare le particelle una per una davanti a dei laser, misurando la diffusione della luce (relativa alla dimensione) e la fluorescenza (da coloranti o anticorpi). Progettazioni strumentali recenti promettono di spingere la citometria a flusso fino alla scala delle vescicole più piccole, aprendo la possibilità che una singola macchina possa dimensionare, contare e caratterizzare le EV in una singola corsa.
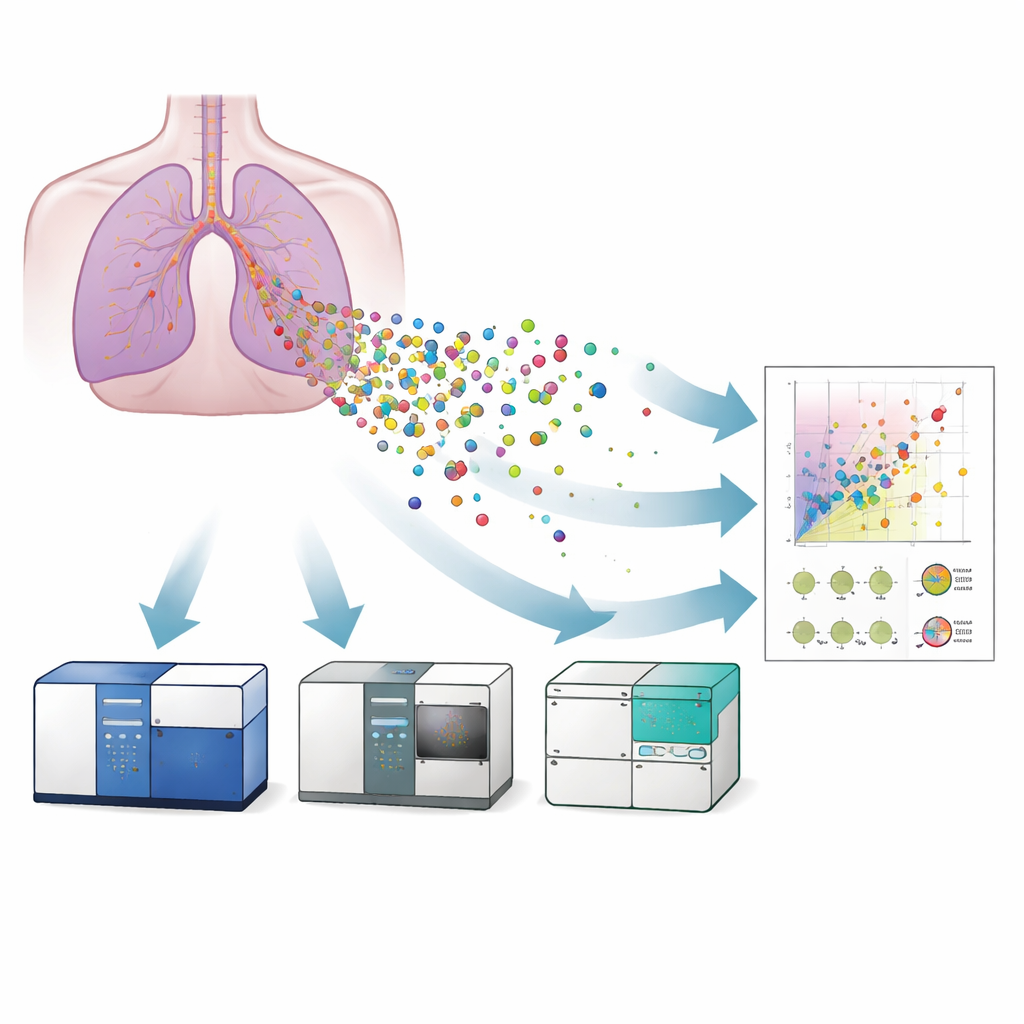
Tre macchine, un obiettivo
I ricercatori hanno confrontato tre versioni di citometria a flusso per studiare le EV rilasciate da un modello coltivato in laboratorio dell’epitelio bronchiale umano: un citometro a flusso convenzionale, un citometro a flusso di imaging e un citometro a flusso nanoscalare. Innanzitutto hanno confermato la presenza e l’aspetto tipico delle vescicole usando microscopia elettronica e microscopica a super-risoluzione, che hanno anche mostrato che le vescicole portavano proteine di superficie note come tetraspanine (CD9, CD63, CD81)—marcatori standard per identificare le EV. Hanno poi usato bead di riferimento accuratamente calibrati e standard di liposomi per tradurre i segnali di luce di ciascuno strumento in dimensioni approssimative delle vescicole. Il citometro nanoscalare riusciva a rilevare vescicole di circa 40 nanometri, lo strumento di imaging fino a circa 55 nanometri, mentre il macchinario convenzionale aveva difficoltà al di sotto di circa 120 nanometri. Ciò significava che solo i sistemi più sensibili potevano catturare pienamente le vescicole più piccole e potenzialmente più rilevanti dal punto di vista medico.
Etichettare e contare le vescicole
Per assicurarsi di misurare vescicole integre e biologicamente attive piuttosto che detriti, il gruppo ha utilizzato un colorante chiamato calceina-AM. Questo colorante si illumina solo dopo aver attraversato una membrana intatta ed essere stato processato da enzimi all’interno della vescicola. Hanno ottimizzato la concentrazione del colorante in modo che segnasse fortemente le vescicole minimizzando il segnale di fondo, arrivando a una concentrazione che produceva risposte chiare e lineari attraverso diluizioni dei campioni. La calceina è stata poi combinata con anticorpi fluorescenti che si legano alle tetraspanine sulla superficie delle vescicole, permettendo agli strumenti di separare vescicole che portavano diverse combinazioni di questi marcatori. Il gruppo ha anche misurato la sensibilità di ciascuna macchina a questi tag fluorescenti—quante molecole di anticorpo dovevano essere presenti su una vescicola prima che potesse essere rilevata in modo affidabile. La citometria a flusso di imaging generalmente offriva soglie di rilevamento inferiori rispetto al citometro convenzionale, rendendola più adatta per particelle con solo un piccolo numero di proteine marker.
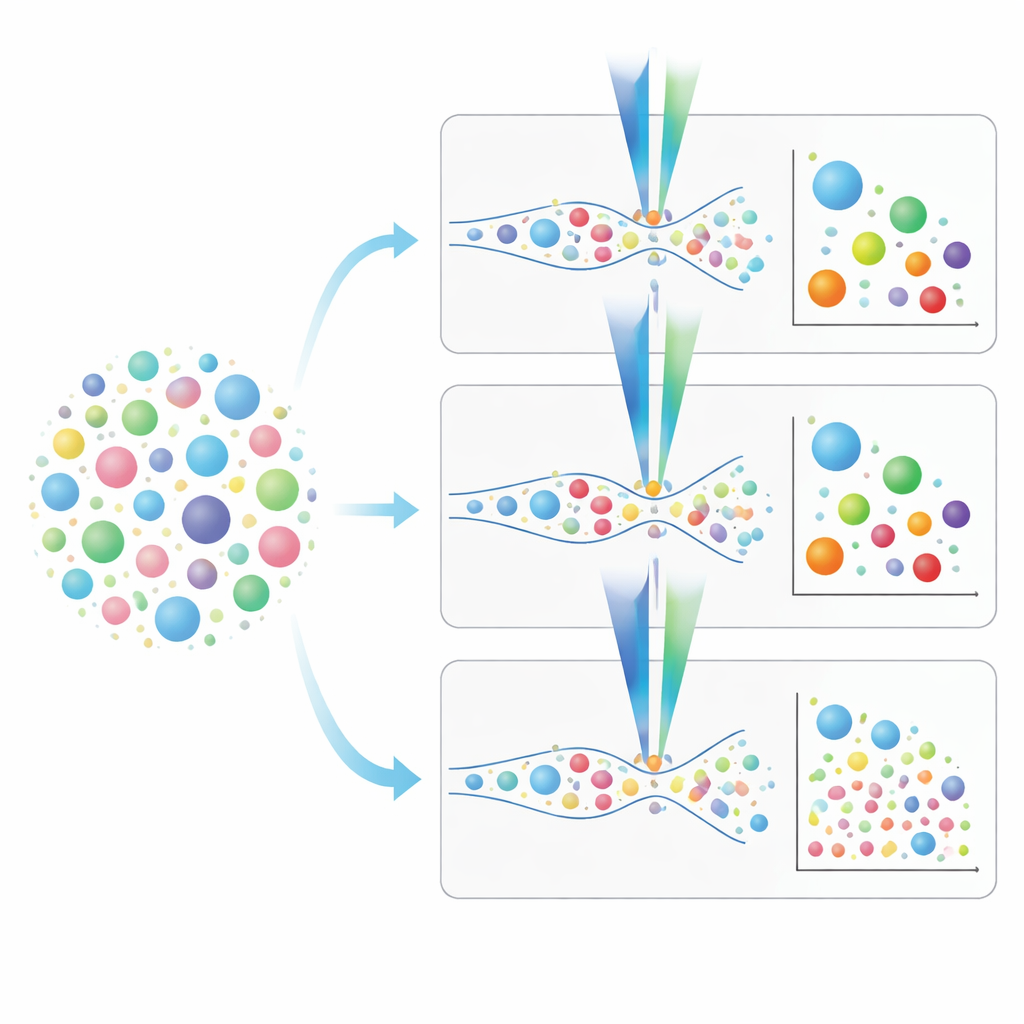
Scegliere lo strumento giusto per gli studi sulle vescicole polmonari
Da questo confronto diretto emerge un quadro pratico. I citometri a flusso convenzionali sono più rapidi e possono analizzare i campioni senza un’isolamento preliminare, ma perdono molte delle vescicole più piccole che potrebbero contenere segnali diagnostici cruciali. I citometri a flusso di imaging e nanoscalari, pur essendo più lenti e, nel caso dello strumento nano, più dipendenti da una pulizia preventiva del campione, possono rilevare dimensioni molto inferiori e supportare una più ricca “impronta” dei marcatori di superficie delle vescicole. Gli autori delineano strategie passo-passo di colorazione e calibrazione, sottolineano l’importanza di conoscere il limite di rilevamento di ogni tag fluorescente e mostrano come evitare segnali fuorvianti da coloranti che marcano anche frammenti o particelle non vescicolari. In termini semplici, forniscono una roadmap per aiutare i ricercatori a decidere quale strumento e quale protocollo si adattino meglio alle loro domande sulle EV polmonari, avvicinando il campo all’uso di questi messaggeri microscopici come strumenti pratici per comprendere, diagnosticare e, infine, trattare le malattie respiratorie.
Citazione: Hopkins, G., Browne, W., Tucis, D. et al. Bronchial epithelial cell-derived extracellular vesicle analysis using conventional, imaging, and nanoscale flow cytometry technologies. Sci Rep 16, 11162 (2026). https://doi.org/10.1038/s41598-026-41848-x
Parole chiave: vescicole extracellulari, epitelio polmonare, citometria a flusso, malattie respiratorie, analisi di biomarcatori