Clear Sky Science · it
Combinare microRNA derivati dal tessuto con modelli di rischio clinico per predire la recidiva di HCC dopo trapianto di fegato: uno studio proof-of-concept
Perché questa ricerca è importante per pazienti e famiglie
Il cancro del fegato è uno dei tumori più letali al mondo e, per alcuni pazienti, l’unica reale possibilità di cura è ricevere un nuovo fegato. Anche così, il tumore può ripresentarsi nell’organo trapiantato, accorciando vite e consumando fegati donatori scarsi. Questo studio esplora se minuscole molecole presenti nel tumore rimosso, chiamate microRNA, possano aiutare i medici a prevedere meglio in chi è più probabile che il cancro ritorni dopo il trapianto, così da adattare più accuratamente le cure di follow-up a ciascuna persona.
Uno sguardo più approfondito al cancro del fegato dopo il trapianto
Il carcinoma epatocellulare, la forma più comune di cancro primario del fegato, spesso insorge in persone con danno epatico cronico dovuto a cause come consumo di alcool, epatiti virali o steatosi epatica. Per tumori piccoli che non possono essere asportati in modo sicuro, il trapianto di fegato offre un potente trattamento doppio: sostituisce il fegato lesionato e rimuove il tumore nello stesso tempo. Poiché gli organi donatori sono limitati, i centri trapianto si basano su regole rigide fondate principalmente su dimensione e numero dei tumori — i noti criteri di Milano e UCSF — per decidere chi potrà trarre maggior beneficio. Tuttavia, anche quando queste regole vengono rispettate, l’8–20% dei pazienti vede comunque la ricomparsa del tumore, a indicare che la sola misura delle dimensioni non coglie quanto un tumore sia realmente aggressivo.
Piccole molecole di RNA con grande potenziale
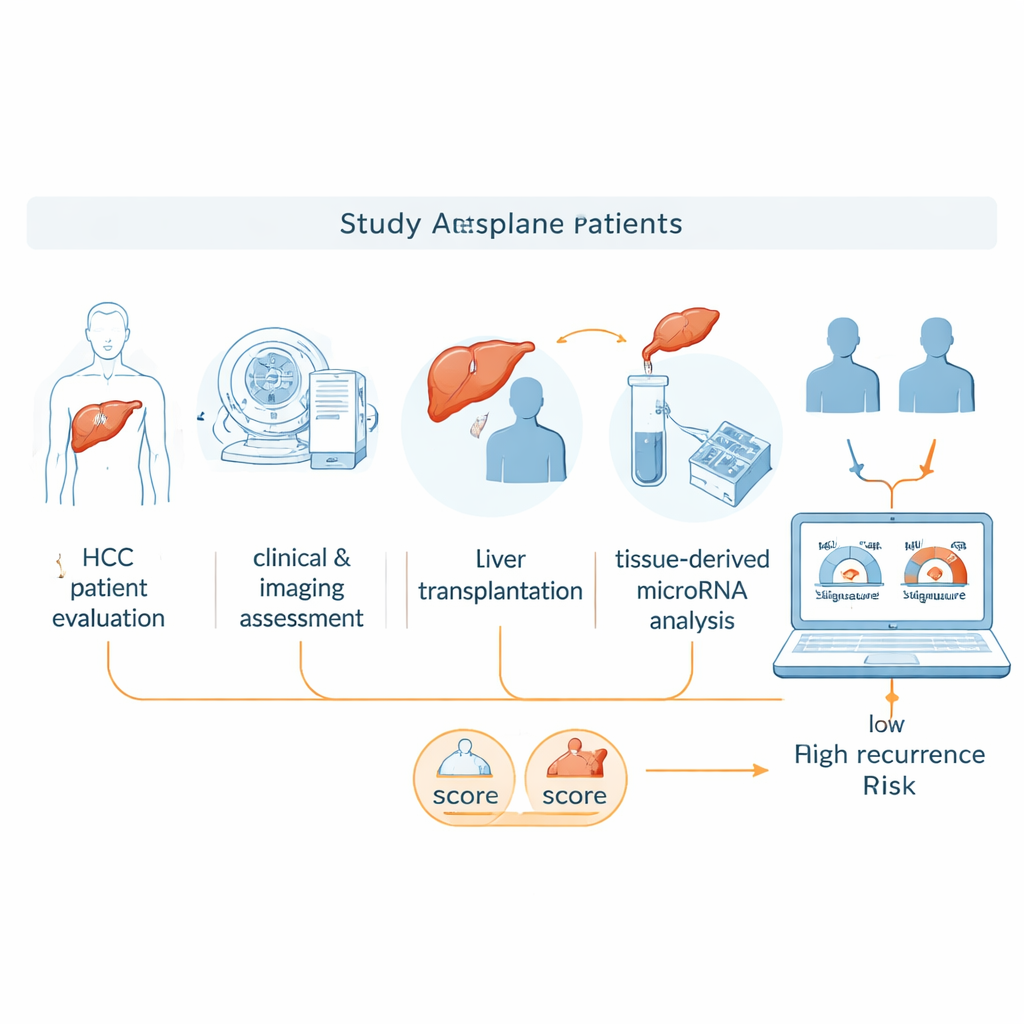
I microRNA sono brevi frammenti di materiale genetico che non codificano proteine ma aiutano a regolare l’accensione e lo spegnimento di altri geni. Diversi tumori possono avere una loro “impronta” di microRNA, e questi schemi possono rivelare quanto velocemente un tumore cresce o quanto è probabile che si diffonda. In questo studio proof-of-concept i ricercatori si sono chiesti se i microRNA prelevati dal tessuto del carcinoma epatocellulare rimosso al momento del trapianto potessero essere combinati con le regole cliniche esistenti per affinare le predizioni sulla recidiva del tumore. Si sono concentrati su campioni di tessuto conservati in blocchi di paraffina, una procedura di routine negli ospedali, per verificare se tale test molecolare sarebbe praticabile nella realtà clinica.
Come è stato condotto lo studio
Il gruppo ha riesaminato 20 pazienti sottoposti a trapianto di fegato per cancro tra il 2007 e il 2021. Metà di loro ha sperimentato la recidiva del tumore dopo il trapianto, mentre l’altra metà è rimasta libera da recidive per almeno cinque anni. Tutti avevano effettuato valutazioni cliniche standard e TAC prima dell’intervento. Dal tumore rimosso di ciascun paziente gli scienziati hanno estratto RNA e misurato l’attività di circa 3.600 microRNA usando una microarray. Hanno inizialmente cercato microRNA i cui livelli differivano marcatamente tra i gruppi con e senza recidiva, quindi hanno ridotto la lista basandosi sulla solidità statistica e su evidenze precedenti che collegavano certi microRNA al comportamento del cancro del fegato.
Un segnale di allarme a tre microRNA
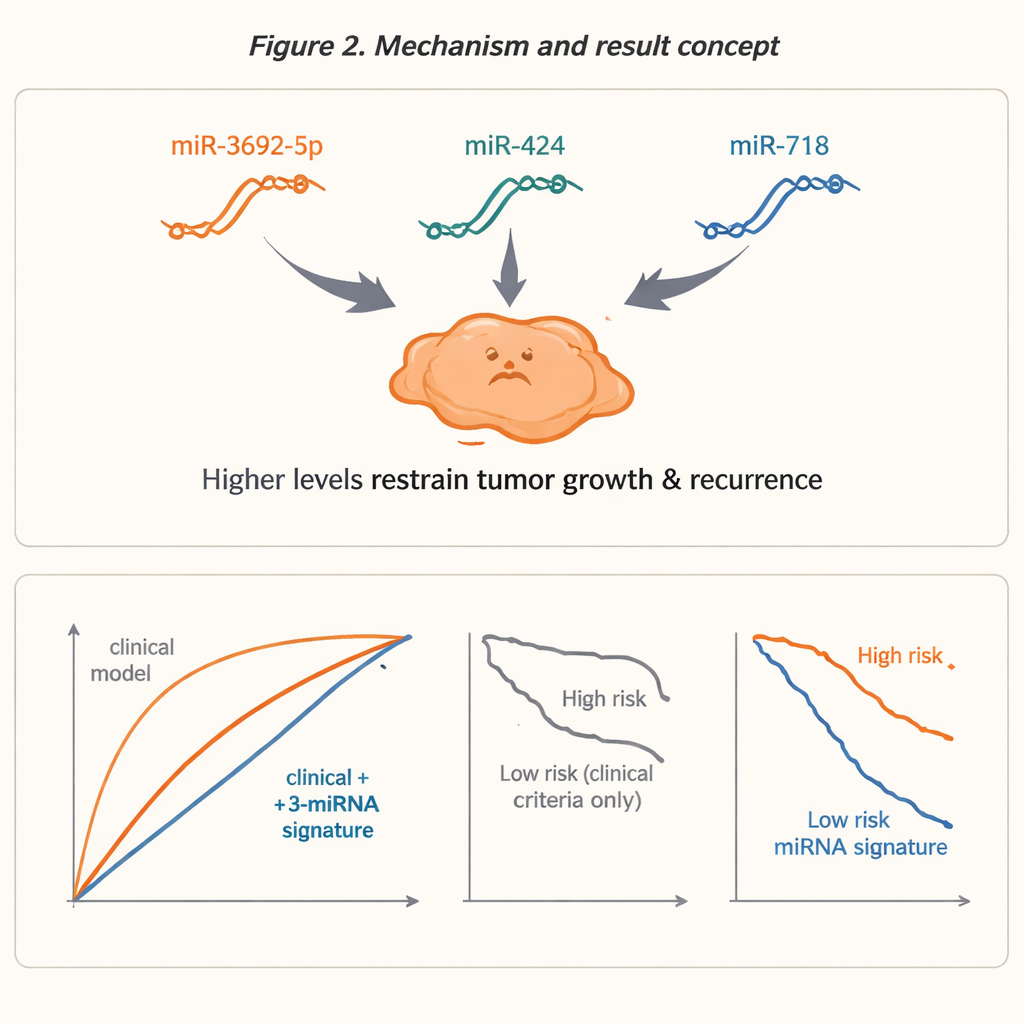
Questo processo ha evidenziato un microRNA fortemente informativo, chiamato miR-3692-5p, che risultava nettamente più basso nei pazienti il cui tumore poi è ricomparso. Altri due microRNA — miR-424 e miR-718 — sono stati aggiunti perché studi precedenti li avevano collegati agli esiti nel carcinoma epatocellulare e perché mostravano simili riduzioni nel gruppo con recidiva. Insieme, questo trio ha costituito una “firma a 3 microRNA” che, da sola, riusciva già a distinguere con elevata accuratezza recidiva e non-recidiva in questo piccolo gruppo. Quando i ricercatori hanno sovrapposto questa firma di microRNA a quattro modelli clinici comunemente usati, inclusi i criteri di Milano e UCSF e un punteggio basato sul dosaggio sierico dell’AFP, i modelli combinati hanno funzionato molto meglio rispetto alle sole regole cliniche nel predire chi sarebbe ricaduto.
Come si traduce in una migliore previsione nella pratica
Per valutare le prestazioni, il team ha usato strumenti statistici standard che misurano quanto bene un test separa pazienti ad alto e basso rischio. I modelli clinici da soli distinguevano solo in modo modesto tra questi gruppi. Dopo l’aggiunta dei tre microRNA, il potere predittivo è aumentato nettamente, con misure di accuratezza che si avvicinavano a 0,94–0,96 su una scala in cui 1,0 rappresenta un test perfetto. I modelli migliorati hanno ricategorizzato circa la metà dei pazienti in una diversa classe di rischio, suggerendo che molte persone attualmente etichettate come “a basso rischio” o “ad alto rischio” potrebbero essere classificate in modo errato dalle sole regole basate sulle dimensioni. È importante sottolineare che i pazienti classificati ad alto rischio dai modelli combinati hanno avuto una sopravvivenza libera da recidiva molto più breve — circa 17 mesi contro 38,5 mesi in un esempio — indicando che questi segnali molecolari si correlavano in modo significativo con gli esiti reali.
Cosa significa per le cure future
Per i non specialisti, il messaggio è che esaminare i “segnali di controllo” interni del tumore, catturati qui da tre specifici microRNA, può rivelare più sulla sua natura reale rispetto alla sola dimensione o al numero. Pur trattandosi di uno studio piccolo ed esplorativo che necessita di conferme in gruppi più grandi, multicentrici e su campioni più facilmente accessibili come il sangue, dimostra che tale test è tecnicamente fattibile su tessuto di routine ospedaliera. Se validato, questo approccio potrebbe aiutare le équipe trapiantologiche a scegliere in modo più intelligente le scansioni e i trattamenti di follow-up, concentrando il monitoraggio e le strategie preventive più intensive su chi presenta un avvertimento molecolare di probabile recidiva, e potenzialmente risparmiando ai pazienti a rischio inferiore esami non necessari.
Citazione: Lederer, T., Lehr, K., Bobe, S. et al. Combining tissue-derived microRNAs with clinical risk models for prediction of HCC recurrence after liver transplantation: A proof-of-concept study. Sci Rep 16, 7742 (2026). https://doi.org/10.1038/s41598-026-41688-9
Parole chiave: cancro del fegato, trapianto di fegato, biomarcatori microRNA, rischio di recidiva del cancro, oncologia di precisione