Clear Sky Science · it
Valutazione quantitativa ex vivo della temperatura target e della durata dell’ablazione per l’ottimizzazione dei protocolli di ablazione a microonde con termometria RM
Osservare i trattamenti del tumore in tempo reale
Quando i medici distruggono i tumori al fegato con il calore, desiderano vedere esattamente quali porzioni dell’organo vengono eliminate durante la procedura. La risonanza magnetica (RM) offre un modo per “vedere la temperatura” all’interno del corpo mentre il calore si propaga. Questo studio esplora quanto calore e per quanto tempo i medici possono riscaldare in sicurezza il tessuto epatico durante l’ablazione a microonde ottenendo allo stesso tempo mappe di temperatura chiare e affidabili dalla RM—un passo importante verso trattamenti oncologici più precisi e meno invasivi.
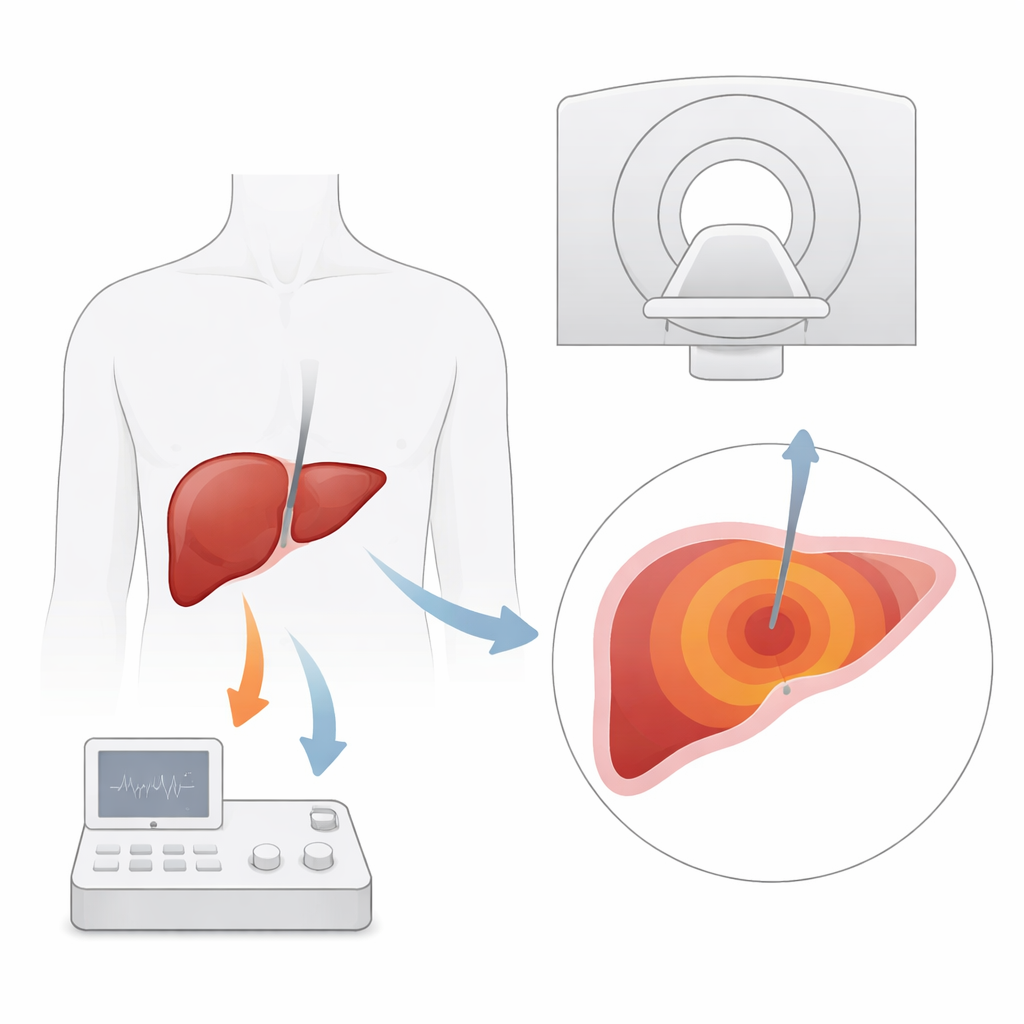
Perché i trattamenti termici del fegato hanno bisogno di occhi migliori
L’ablazione a microonde utilizza un ago sottile per erogare energia che cuoce e distrugge il tessuto tumorale all’interno del fegato. È particolarmente importante per i pazienti con cancro al fegato o metastasi che non possono essere sottoposti a chirurgia. Strumenti di imaging tradizionali come l’ecografia e la TC guidano il posizionamento dell’ago, ma faticano a mostrare chiaramente lesioni piccole o a tracciare quanto il calore si è diffuso durante il trattamento. La RM si distingue perché non solo mostra i tessuti molli con elevato dettaglio, ma può anche misurare le variazioni di temperatura sfruttando una proprietà delle molecole d’acqua. In teoria, ciò permette ai medici di osservare in tempo reale una mappa termica del fegato e assicurarsi che l’intero tumore, più un margine di sicurezza, venga distrutto.
Quando troppo calore offusca la vista
In pratica, le mappe di temperatura RM possono diventare inaffidabili quando il tessuto diventa molto caldo. A temperature elevate, l’acqua nel tessuto bolle, formando piccole sacche di gas che distorcono il campo magnetico. Queste distorsioni si manifestano come letture di temperatura errate e forme anomale sulla mappa, rendendo difficile stabilire dove termini la vera zona di ablazione. I ricercatori hanno ipotizzato che l’uso di temperature target leggermente più basse potesse produrre mappe RM più pulite e attendibili, anche se ciò significasse aree trattate più piccole. L’obiettivo era trovare combinazioni di temperatura target e durata del riscaldamento che bilanciassero al meglio la chiarezza delle immagini con una distruzione tissutale sufficiente.
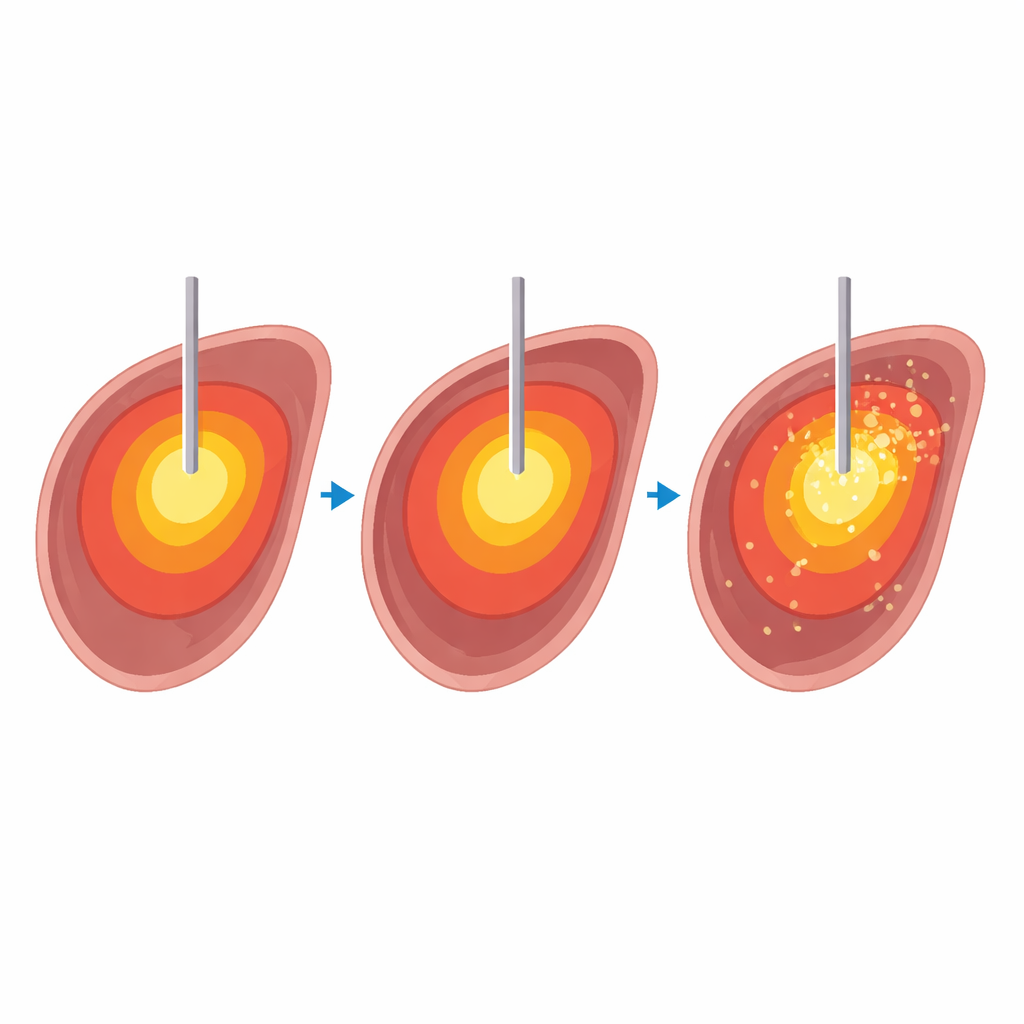
Testare le impostazioni di calore su fegati di animali donatori
Per indagare in modo sicuro e preciso, il team ha eseguito 32 ablazioni a microonde su dieci fegati bovini rimossi poco dopo la macellazione. All’interno di uno scanner RM a 1,5 tesla, hanno riscaldato il tessuto epatico a quattro temperature target—60, 80, 100 e 120 gradi Celsius—for quattro differenti durate comprese tra 5 e 15 minuti. Durante ogni ablazione, una sequenza RM rapida generava mappe tridimensionali di temperatura e di “dose termica” ogni pochi secondi. Dopo il riscaldamento, i fegati sono stati sezionati lungo la traccia dell’ago e le aree visibili di tessuto necrotico sono state misurate e confrontate con le aree previste dalle mappe RM. Due radiologi hanno valutato la qualità delle mappe RM su una scala a cinque punti, considerando quanto la zona riscaldata apparisse rotonda e regolare e quanto gli artefatti dovuti al gas e all’ago interferissero.
Bruciature più fredde, mappe più nitide
Gli esperimenti hanno mostrato un compromesso evidente. Temperature più elevate hanno prodotto zone di tessuto necrotico più ampie, come ci si aspetta, ma le mappe di temperatura RM si deterioravano nettamente oltre i 100 gradi. A queste impostazioni più calde, le forme di ablazione diventavano più irregolari e le distorsioni legate al gas provocavano valori di temperatura apparentemente in calo o addirittura negativi vicino all’ago. Al contrario, a 60 e 80 gradi le mappe RM erano più uniformi, più circolari e molto più in linea con le dimensioni reali della lesione osservate nei tagli del tessuto. Le analisi statistiche hanno confermato una forte concordanza tra le aree derivate dalla RM e la necrosi reale a temperature più basse, con correlazioni che si attenuavano o scomparivano a temperature più elevate. Allungare il tempo di riscaldamento compensava in parte le temperature inferiori in termini di danno totale, ma non riusciva a eguagliare completamente le lesioni maggiori osservate a 120 gradi.
Una strategia in due fasi per un’ablazione più sicura e intelligente
Basandosi su questi risultati, gli autori propongono un compromesso pratico per futuri trattamenti guidati da RM. Una prima fase di riscaldamento intorno agli 80 gradi Celsius per 15 minuti ha fornito un buon equilibrio: la qualità dell’immagine era elevata, la zona di ablazione era ragionevolmente ampia e gli studi tissutali mostravano una morte cellulare efficace. Per i casi che richiedono zone di trattamento ancora più grandi, suggeriscono un approccio in due fasi: iniziare con una fase a temperatura più bassa per ottenere una mappa termica pulita e verificarne la copertura, quindi, una volta che il posizionamento e i margini risultano soddisfacenti, aumentare la temperatura in una seconda fase per ampliare l’area necrotica, accettando che la mappa di temperatura sarà meno affidabile durante questo ultimo impulso.
Che cosa significa per la cura dei pazienti in futuro
Per un non specialista, il messaggio chiave è che “abbassare un po’ il calore” può in realtà rendere i trattamenti termici del cancro più sicuri e più precisi—almeno in condizioni di laboratorio controllate. Temperature target più basse hanno fornito mappe di temperatura RM molto più chiare, rendendo più semplice vedere dove il tessuto era veramente stato distrutto. Lo svantaggio è che bruciature più fredde producono lesioni più piccole, quindi i medici potrebbero aver bisogno di trattamenti più lunghi o a più fasi per coprire tumori di grandi dimensioni. Poiché questa ricerca è stata condotta su fegati animali non viventi privi di flusso sanguigno e movimento respiratorio, sono necessari ulteriori studi sui pazienti. Tuttavia, lo studio indica protocolli di trattamento che utilizzano la RM non solo per indirizzare l’ago, ma per osservare e perfezionare la combustione in tempo reale, migliorando potenzialmente gli esiti per le persone con tumori al fegato.
Citazione: Nardone, L., Tan, A.S.M., Bour, P. et al. Quantitative ex vivo assessment of target temperature and ablation duration for protocol optimization of microwave ablation procedures with mr thermometry. Sci Rep 16, 8153 (2026). https://doi.org/10.1038/s41598-026-41656-3
Parole chiave: ablazione a microonde, termometria RM, cancro al fegato, ablazione termica, terapia guidata da immagini