Clear Sky Science · it
Effetti antagonisti degli amminoacidi favoriscono nano-ambienti abiotici nelle argille
Come minuscole nicchie nell’argilla potrebbero nutrire la prima chimica della vita
La vita potrebbe essere iniziata non negli oceani aperti, ma all’interno di spazi inconcepibilmente piccoli tra gli strati di comuni minerali argillosi. Questo studio esplora come molecole semplici legate agli odierni amminoacidi possano rimodellare l’argilla su scala nanometrica, scavando compartimenti accoglienti che intrappolano e organizzano la chimica. Mostrando come diversi amminoacidi rafforzino o destabilizzino gli strati argillosi, il lavoro suggerisce un modo naturale in cui la Terra primitiva — o altri mondi rocciosi — potrebbero aver creato piccoli “laboratori” in cui i mattoni della vita si sono potuti assemblare.
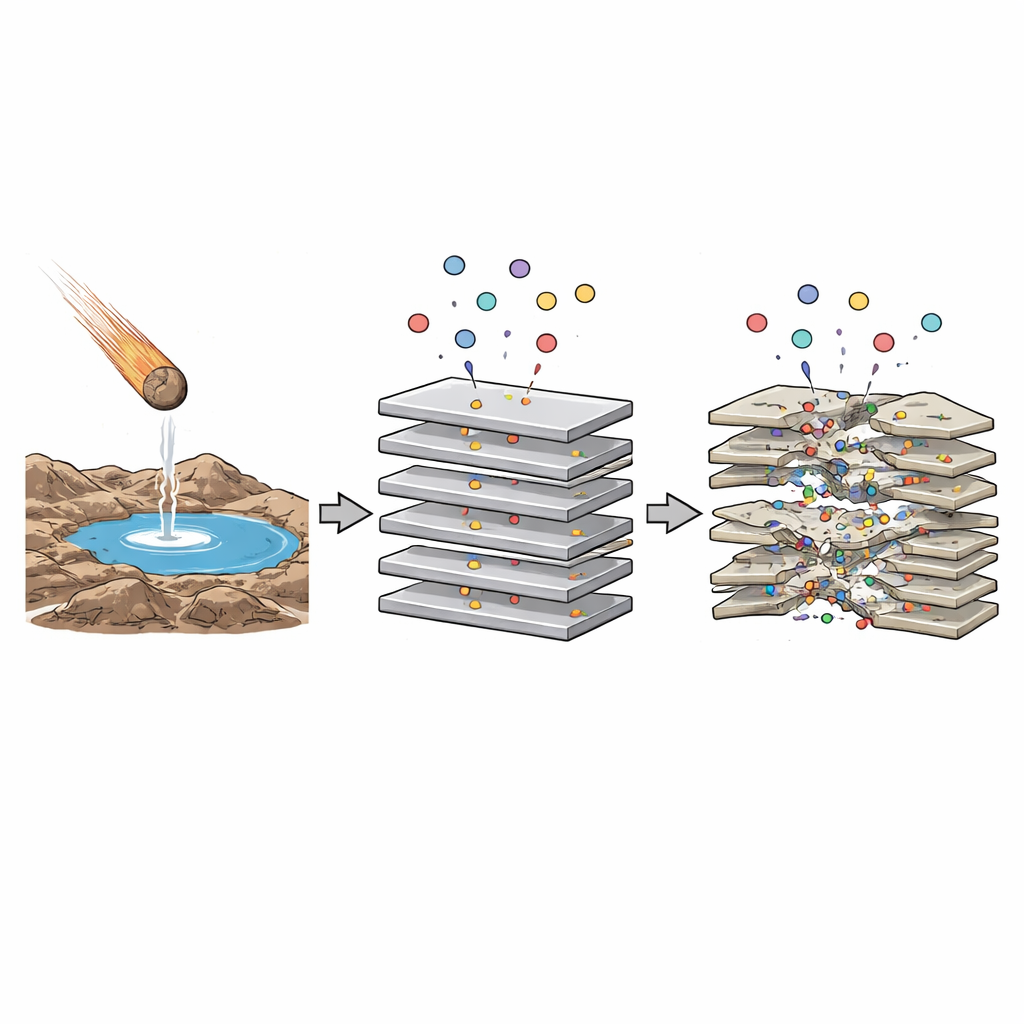
La promessa degli spazi nascosti
Gli scienziati sospettano da tempo che i minerali non si limitassero a giacere sotto gli oceani e gli stagni primitivi: potrebbero aver contribuito ad assemblare le prime catene molecolari. In particolare, argille come la montmorillonite possono gonfiarsi e contrarsi quando acqua e piccole molecole si insinuano fra i loro fogli impilati. All’interno di questi stretti interstizi l’acqua si comporta in modo diverso, le forze elettriche sono più intense e reazioni difficili in acqua ordinaria possono diventare più agevoli. Questi spazi confinati potrebbero favorire il legame tra mattoni semplici — come amminoacidi e nucleotidi — in catene più lunghe, un passaggio chiave verso la vita. Ma gli ambienti prebiotici reali erano zuppe chimiche con molte molecole organiche diverse presenti contemporaneamente. Ciò solleva una domanda: quando più tipi di amminoacidi interagiscono con l’argilla insieme, si annullano a vicenda o i loro effetti contrastanti possono effettivamente creare ambienti più ricchi per la chimica?
Costruttori amichevoli e maliziosi destabilizzatori
I ricercatori si sono concentrati su una forma di montmorillonite ricca di calcio e su tre amminoacidi. Due, lisina e arginina, sono amminoacidi tipici per la costruzione delle proteine, noti dai manuali di biologia. Il terzo, l’acido gamma-aminobutirrico (GABA), non è impiegato nelle proteine moderne ma è comune nelle meteoriti e quindi plausibilmente consegnato alla Terra primitiva. Lavori precedenti avevano mostrato che lisina e arginina si sistemano negli spazi interstrato e si legano saldamente, contribuendo a mantenere gli strati ordinati e relativamente piatti. Il GABA, al contrario, aderisce poco — eppure ha un effetto sproporzionato: piega e parzialmente scolla i fogli argillosi, creando cavità su scala nanometrica. Questo studio ha chiesto cosa accade quando una piccola quantità di amminoacido di tipo proteico è miscelata con un grande eccesso di GABA di tipo meteoritico, emulando uno stagno pesantemente seminato di organici extraterrestri.
Osservare la trasformazione degli strati argillosi
Per seguire questi cambiamenti il gruppo ha combinato diverse tecniche che rivelano ciascuna un aspetto differente dell’argilla. La spettroscopia infrarossa ha sondato come vibrano le parti silicio–ossigeno del reticolo argilloso, che cambia quando gli strati sono deformati, separati o riempiti da diverse specie. La diffrazione di raggi X ha misurato lo spaziamento e l’ordinamento dei fogli impilati, sia nei campioni secchi sia dopo reidratazione con vapore acqueo. L’analisi termogravimetrica ha monitorato quanto saldamente molecole organiche e acqua venivano trattenute nell’argilla. Infine, la microscopia elettronica ad alta risoluzione ha fornito immagini dirette delle strutture di strato e di eventuali piccole cavità tra di esse. Complessivamente, questi strumenti hanno permesso agli autori di distinguere le azioni stabilizzanti di lisina e arginina dall’influenza perturbatrice del GABA, anche quando tutti erano presenti nella stessa miscela.
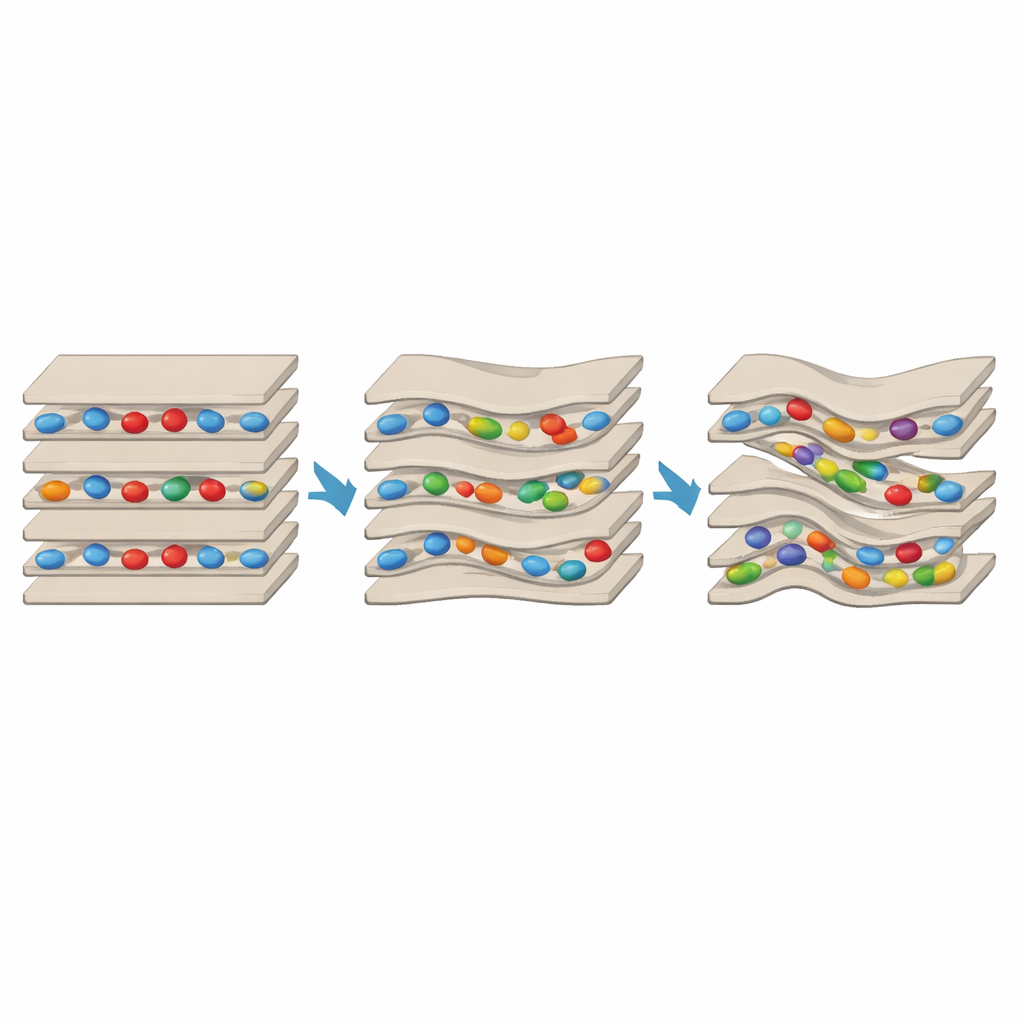
Uno yin–yang su scala nano nell’argilla
I risultati rivelano un marcato gioco di spinta e trazione. Quando erano presenti solo lisina o arginina, questi si intercalavano negli spazi interstrato, agendo come traversi che legano un foglio al successivo. Ciò riduceva la capacità dell’argilla di gonfiarsi con l’acqua e rendeva la struttura più ordinata e resistente allo scollamento. Ma quando il GABA veniva aggiunto in grande eccesso, in molte regioni prevaleva sull’effetto stabilizzante. Le firme spettroscopiche mostrarono la presenza di domini parzialmente esfoliati e i pattern a raggi X indicarono maggiore disordine e ridotta allineamento degli strati. La microscopia elettronica andò oltre, rivelando pile fortemente distorte con chiare nanocavità inserite a metà strato — piccole nicchie di un paio di nanometri che non apparivano nel controllo o nei campioni contenenti solo amminoacidi proteici. È importante che regioni con strati ponte strettamente tenuti coesistessero accanto a regioni con strati distorti e ricchi di cavità nello stesso granulo di argilla, dimostrando che entrambi gli effetti possono operare fianco a fianco.
Nano-compartimenti naturali per la chimica primordiale
Per un non specialista, il messaggio chiave è che semplici miscele di amminoacidi possono scolpire l’argilla in un mosaico di minuscoli compartimenti con proprietà diverse. Gli amminoacidi costituenti le proteine aiutano a tenere insieme gli strati, mentre il GABA d’origine meteoritica li scolla delicatamente e scava nanocavità. Queste nicchie confinate probabilmente ospitano acqua e molecole disciolte in condizioni diverse rispetto all’ambiente circostante, favorendo potenzialmente reazioni come la formazione di polimeri, centrali per l’origine della vita. Poiché le meteoriti forniscono abbondanti amminoacidi non proteici a mondi ricchi di argilla, questo antagonismo «yin–yang» tra molecole stabilizzanti e perturbatrici potrebbe essere una via comune per pianeti rocciosi e asteroidi per generare e sostenere diversi nano-ambienti dove la biochimica primitiva potrebbe avere inizio.
Citazione: Bezaly, O.R., King, H.E. & Petrignani, A. Antagonistic effects of amino acids support abiotic nano-environments in clay. Sci Rep 16, 8959 (2026). https://doi.org/10.1038/s41598-026-41502-6
Parole chiave: origine della vita, chimica prebiotica, minerali argillosi, amminoacidi, nanoconfinamento