Clear Sky Science · it
Implementazione di un test di biopsia liquida su 1021 geni per il profilaggio genomico dei tumori nella pratica oncologica reale
Perché un esame del sangue per il cancro è importante
La maggior parte delle persone sa che i medici spesso devono asportare un frammento di tumore per capire meglio il cancro di un paziente. Ma questa biopsia tradizionale è invasiva, può essere dolorosa e potrebbe non catturare l’intero quadro di una malattia già diffusa. Questo studio esplora un approccio diverso: usare un semplice prelievo di sangue per analizzare le variazioni genetiche in più di mille geni legati al cancro. Mostrando quanto bene funziona questo ampio test del sangue nella pratica oncologica quotidiana, i ricercatori evidenziano un futuro in cui le scelte terapeutiche, il monitoraggio e persino la valutazione del rischio ereditario possono essere guidati da un tubo di sangue piuttosto che da uno scalpello.
Dall’ago nel tumore all’ago nella vena
Il cancro rilascia frammenti minuscoli del suo DNA nel flusso sanguigno quando le cellule tumorali muoiono e si frammentano. Questi frammenti, chiamati DNA tumorale circolante, sono mescolati al DNA normale delle cellule sane. Il gruppo ha studiato 1.110 persone con tumori metastatici (avanzati) di molti tipi, compresi polmone, seno, colon-retto, pancreas, prostata, ovaio e altri. Hanno utilizzato un test esteso che legge 1.021 geni da un campione di sangue e, quando disponibile, hanno confrontato i risultati del sangue con il DNA del tessuto tumorale del paziente. Hanno inoltre sequenziato i globuli bianchi prelevati dallo stesso campione di sangue per distinguere i segnali tumorali veri dalle variazioni correlate all’età nelle cellule ematopoietiche. 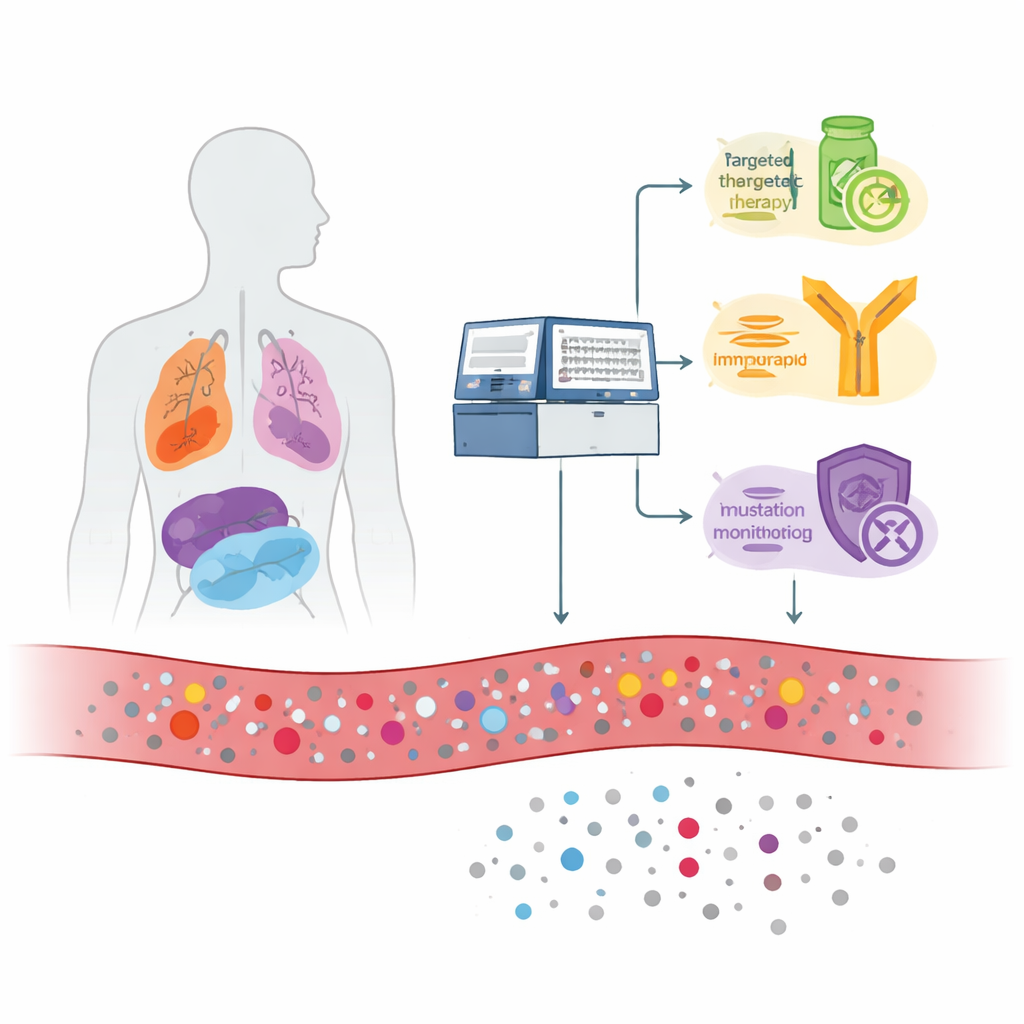
Cosa ha rivelato il sangue sui tumori
Il test del sangue ha rilevato variazioni del DNA legate al cancro in circa due terzi dei pazienti. Molte di queste variazioni indicavano direttamente opportunità terapeutiche. In circa il 16% dei pazienti, il test ha individuato bersagli “on‑label”—mutazioni associate a farmaci già approvati per quel tipo specifico di tumore, come alcune alterazioni di EGFR nel tumore polmonare o PIK3CA ed ESR1 nel tumore al seno. Quando i ricercatori hanno anche considerato i bersagli “off‑label” (mutazioni con farmaci approvati in altri tumori), le alterazioni oggetto di studi clinici e le mutazioni note per causare resistenza ai farmaci, più della metà dei pazienti presentava almeno una scoperta potenzialmente utile. Il test ha inoltre calcolato due caratteristiche genetiche più ampie—il carico mutazionale tumorale e l’instabilità dei microsatelliti—che possono segnalare pazienti che potrebbero rispondere agli inibitori del checkpoint immunitario; quasi il 9% dei pazienti risultava potenzialmente idoneo a tale immunoterapia basandosi solo sul sangue.
Cancro diversi, intensità del segnale diversa
Non tutti i tumori rilasciano DNA nel sangue allo stesso modo. Tumori come quelli del colon-retto, della prostata e del seno spesso cedono abbastanza DNA da permettere al test di rilevare multiple alterazioni, mentre i tumori cerebrali e molti sarcomi rilasciano pochissimo, in parte a causa di barriere fisiche come la barriera emato‑encefalica o perché i loro cambiamenti genetici sono di tipi più difficili da rilevare. I ricercatori hanno stimato, per ogni paziente, la frazione di DNA libero nel sangue che proveniva dal tumore. Questa “frazione tumorale” era generalmente bassa—circa il 2% in media—probabilmente perché molti pazienti erano già in trattamento, il che riduce il carico tumorale e la quantità di DNA tumorale in circolo. Anche così, il pannello genico ampio ha aiutato a confermare quando il DNA tumorale era realmente presente, rendendo un risultato “negativo” più affidabile nei tumori che rilasciano DNA a livelli moderati.
Seguire il cancro nel tempo e scoprire il rischio ereditario
Un sottoinsieme di pazienti ha eseguito il test del sangue più di una volta. Per alcuni che erano inizialmente negativi, test successivi sono risultati positivi man mano che i livelli di DNA tumorale aumentavano, suggerendo una progressione della malattia più che la comparsa improvvisa di resistenza. In altri, in test successivi sono emerse nuove mutazioni note per causare resistenza alle terapie mirate o ormonali, illustrando come prelievi seriali possano cogliere vie di fuga del tumore prima che le sole immagini lo mostrino. Allo stesso tempo, il sequenziamento dei globuli bianchi ha permesso al gruppo di rilevare mutazioni ereditate (germinali) in geni di rischio per il cancro come BRCA1 e BRCA2. Circa l’11% dei pazienti portava tali variazioni ereditarie, che potrebbero influenzare sia la loro terapia—come l’accesso agli inibitori PARP—sia le raccomandazioni di screening per i loro familiari. 
Come sangue e tessuto lavorano insieme
Per 145 pazienti, i ricercatori hanno potuto confrontare direttamente i risultati del sangue con quelli del tessuto tumorale. Per le mutazioni più importanti legate ai farmaci, la corrispondenza tra sangue e tessuto è stata forte: circa il 90% delle volte concordavano sulla presenza o assenza di un bersaglio chiave. In alcuni casi, il test del sangue ha rilevato cambiamenti di resistenza che il campione di tessuto precedente non aveva mostrato, probabilmente perché il tumore si era evoluto sotto il trattamento. In altri, il tessuto ha rivelato alterazioni non rilevabili nel sangue, spesso in tumori che rilasciano poco DNA. Questo schema suggerisce che sangue e tessuto non sono avversari ma partner: il tessuto rimane essenziale quando circola poco DNA tumorale, mentre la biopsia liquida offre rapidità, minore invasività e la possibilità di ripetere i test man mano che la malattia cambia.
Cosa significa questo per i pazienti
Per un lettore non specialistico, il messaggio di questo studio è che un singolo prelievo di sangue può oggi fornire un ritratto genetico sorprendentemente completo di molti tumori avanzati. Esaminando un’ampia selezione di oltre mille geni e separando con cura i segnali tumorali dal rumore di fondo e dalle variazioni ereditarie, il test ha individuato opzioni terapeutiche e indizi di resistenza nella maggioranza dei pazienti, e ha segnalato quasi uno su dieci come possibile candidato all’immunoterapia. Se combinato con l’analisi tradizionale del tessuto, questo approccio aumenta le probabilità di trovare un bersaglio azionabile, aiuta gli oncologi a scegliere e aggiustare le terapie più rapidamente e può rivelare rischi ereditari rilevanti per l’intera famiglia. Pur non sostituendo tutte le biopsie—soprattutto nei tumori che rilasciano poco DNA nel sangue—mostra come la biopsia liquida stia diventando un potente e pratico complemento all’assistenza standard nella pratica oncologica reale.
Citazione: Florou-Chatzigiannidou, C., Papadopoulou, E., Metaxa-Mariatou, V. et al. Implementation of a 1021-gene liquid biopsy assay for real-world tumor genomic profiling in oncology practice. Sci Rep 16, 10064 (2026). https://doi.org/10.1038/s41598-026-40923-7
Parole chiave: biopsia liquida, DNA tumorale circolante, genomica del cancro, terapia mirata, inibitori del checkpoint immunitario