Clear Sky Science · it
IA spiegabile per la sorveglianza delle lesioni gastrointestinali e la somministrazione mirata di farmaci
Esami più intelligenti, terapie più sicure
Molte persone temono i farmaci oncologici a causa dei loro effetti collaterali drastici. Questa ricerca esplora un futuro in cui minuscole videocamere ingeribili, algoritmi intelligenti e vettori farmacologici microscopici collaborano affinché i farmaci potenti vengano somministrati solo dove sono davvero necessari. Chiudendo il ciclo tra l’individuazione di un problema nell’intestino e il trattamento immediato, gli autori mirano a rendere l’assistenza gastrointestinale più precisa, meno invasiva e molto più sicura.
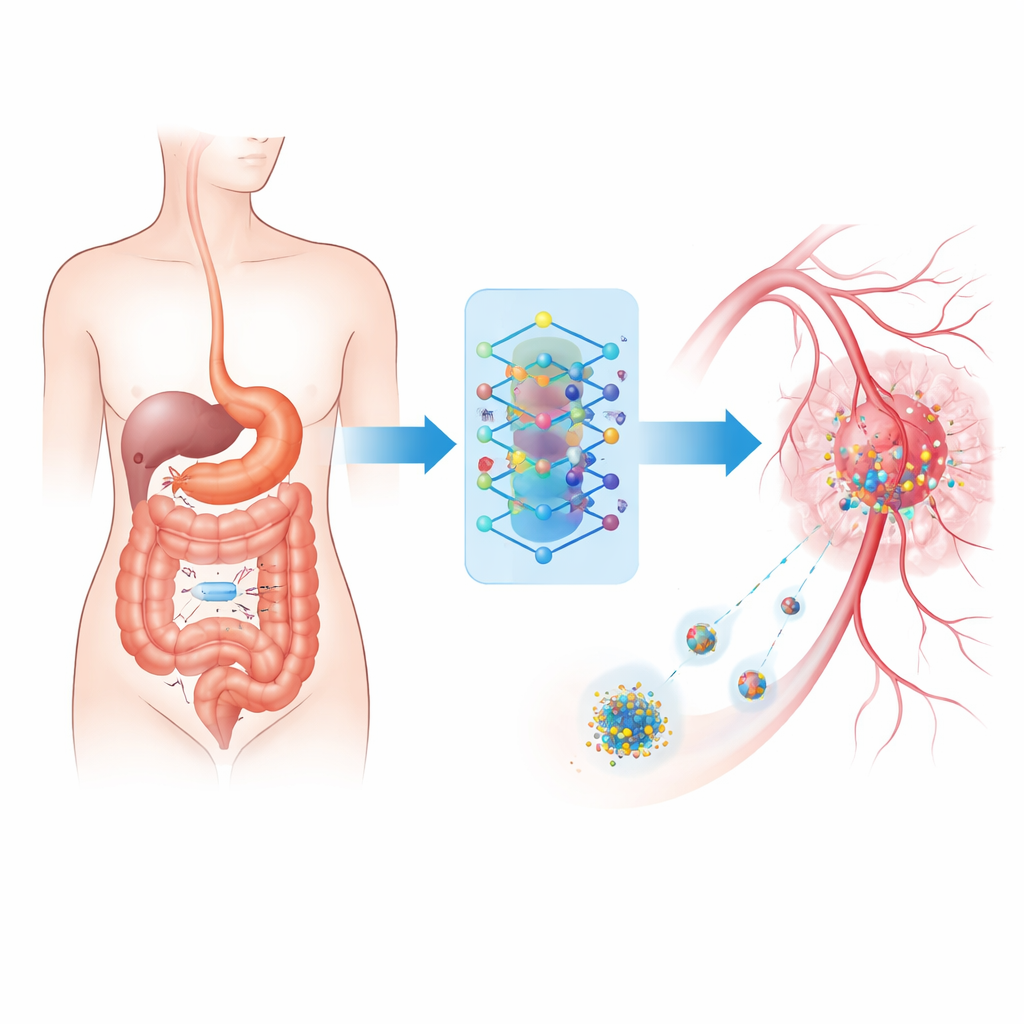
Una minuscola telecamera in viaggio
Al centro del sistema c’è un dispositivo di imaging wireless ingeribile — una capsula delle dimensioni di una vitamina che percorre naturalmente il tratto digestivo scattando decine di migliaia di fotografie. Invece di affidarsi unicamente al medico per rivedere questo flusso massiccio di immagini, la capsula le invia a un’unità indossabile all’esterno del corpo. Qui, un computer compatto utilizza software avanzati di riconoscimento dei pattern per distinguere il tessuto normale da lesioni sospette che potrebbero essere cancerose o gravemente infiammate. Questa configurazione ricalca l’endoscopia in capsula già in uso negli ospedali, ma è potenziata per funzionare in tempo reale e connettersi direttamente agli strumenti di trattamento.
L’intelligenza artificiale come decisore
L’unità indossabile esegue un modello di analisi delle immagini attentamente addestrato su tecniche moderne di visione artificiale. Il modello ha imparato a riconoscere 25 diverse condizioni gastrointestinali — da polipi e ulcere a infiammazioni gravi — usando una ampia raccolta pubblica di immagini endoscopiche e istologiche. Per far fronte al fatto che alcune malattie sono molto più rare di altre, gli autori hanno addestrato il sistema in due fasi: prima per apprendere le caratteristiche visive generali di ciascuna condizione e poi per affinare il modello in modo che reperti pericolosi ma poco comuni non vengano ignorati. Nei test, questo approccio ha classificato correttamente le immagini più di nove volte su dieci, con prestazioni particolarmente buone nelle categorie correlate al cancro.
Vedere dentro la “scatola nera”
Poiché il personale medico deve poter fidarsi di qualsiasi diagnosi automatizzata che possa influenzare una dose di farmaco, gli autori hanno impiegato tecniche di IA spiegabile per mostrare quali parti di ciascuna immagine guidano la decisione del modello. Sovrapposizioni in stile mappa di calore evidenziano le regioni esatte che il sistema ha ritenuto importanti. Queste mappe esplicative non sono state solo esaminate visivamente; sono state valutate con test quantitativi che misuravano quanto la fiducia del modello cambiasse quando le regioni evidenziate venivano rimosse o aggiunte, quanto fossero stabili le spiegazioni attraverso ripetute sessioni di addestramento e quanto si sovrapponessero ai contorni delle lesioni tracciati dagli esperti. Tra i vari metodi testati, uno chiamato LayerCAM ha prodotto le spiegazioni più fedeli e coerenti, aiutando i medici a verificare che il sistema stia “guardando” nel punto giusto.
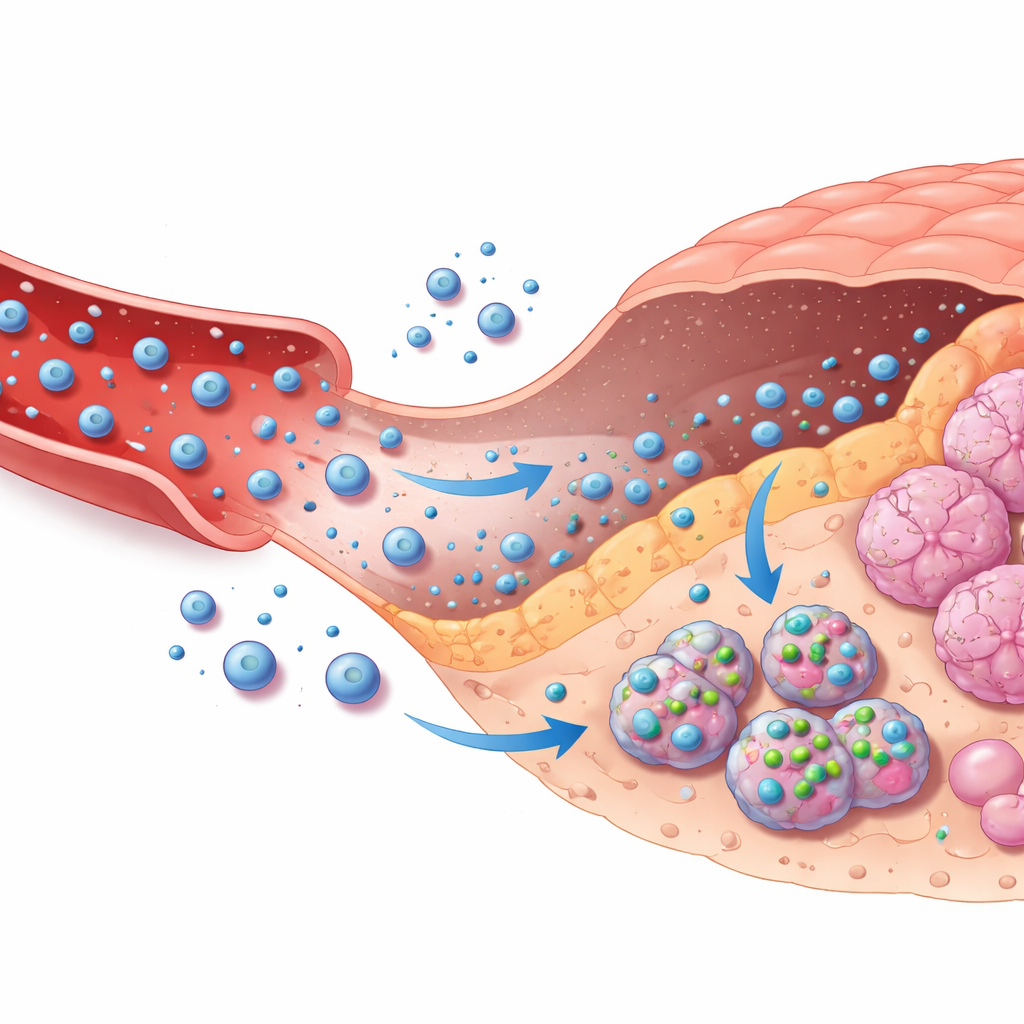
Guidare i vettori farmacologici nel corpo
La seconda metà del quadro collega queste decisioni basate sulle immagini alla somministrazione mirata della chemioterapia. Gli autori modellano come un comune farmaco antitumorale, la doxorubicina, viaggi da una pompa esterna attraverso il flusso sanguigno, fuoriesca nei tessuti tumorali, entri nelle cellule tumorali e venga infine eliminato. Questo è rappresentato in un modello matematico multi‑compartimentale che monitora i livelli di farmaco nel sangue, nel tessuto circostante e all’interno delle cellule. Sulla base della fiducia dell’IA che una lesione sia maligna e della gravità apparente, un semplice sistema di regole sceglie tra nessun trattamento, trattamento moderato o trattamento intensivo, regolando la velocità con cui le nanoparticelle cariche di farmaco rilasciano il loro contenuto e la durata dell’infusione. Uno strato di sicurezza controlla costantemente i livelli predetti di farmaco all’interno delle cellule e riduce automaticamente la dose se si avvicina un limite di sicurezza, anche se l’IA risultasse eccessivamente fiduciosa.
Proteggere la privacy e prevenire abusi
Siccome lo stesso canale che trasporta le immagini può anche trasmettere comandi di trattamento, la sicurezza è critica. Gli autori introducono uno schema di privacy leggero che offusca i segnali biomedici usando una mappa matematica caotica prima che viaggino attraverso la nano‑rete del corpo, rendendo i dati intercettati molto difficili da interpretare. Su questo livello, il gateway indossabile autentica i dispositivi e verifica che i segnali di controllo corrispondano a pattern fisici attesi, contribuendo a bloccare comandi falsi. Le simulazioni mostrano come diverse impostazioni di privacy scambino una piccola perdita di accuratezza nella rilevazione per una protezione più forte, e identificano punti di funzionamento che mantengono elevate le prestazioni cliniche limitando nettamente la perdita di dati. Insieme a limiti rigorosi di dose, regole di spegnimento d’emergenza e registri di sicurezza, queste misure mirano a rendere il sistema resiliente sia agli incidenti sia agli attacchi.
Cosa potrebbe significare per i pazienti
In parole semplici, questo lavoro delinea come potrebbe funzionare un ciclo “vedi‑e‑tratta” all’interno del corpo: una telecamera ingeribile individua punti sospetti, un assistente intelligente interpreta quanto vede con ragionamenti trasparenti e un sistema di somministrazione controllata risponde con dosi accuratamente limitate e focalizzate sul tessuto malato. Lo studio è ancora teorico e basato su simulazioni, ma mostra che un progetto a ciclo chiuso di questo tipo può centrare obiettivi terapeutici e rispettare limiti di sicurezza rigorosi, anche quando l’IA commette errori o quando le condizioni variano da persona a persona. Se realizzato nella pratica, questo tipo di sistema potrebbe contribuire a trasformare la chemioterapia da uno strumento grossolano a uno molto più preciso e personalizzato per le malattie gastrointestinali.
Citazione: Kamal, I.R., El-Zoghdy, S.F. & Soliman, R.F. Explainable AI for gastrointestinal lesion surveillance and precision targeted drug delivery. Sci Rep 16, 9807 (2026). https://doi.org/10.1038/s41598-026-40882-z
Parole chiave: imaging gastrointestinale, IA spiegabile, somministrazione mirata di farmaci, nanomedicina, endoscopia in capsula