Clear Sky Science · it
Separazione efficace delle vortici di Dean a portate ridotte per l’isolamento di cellule rare
Perché è importante separare le cellule rare
Le cellule tumorali che finiscono nel flusso sanguigno o in altri fluidi corporei sono come segnali d’allarme precoci per la malattia. Sono però enormemente superate in numero dalle normali cellule del sangue, il che le rende estremamente difficili da trovare e studiare. Questo articolo descrive un nuovo dispositivo su scala micro che utilizza flussi delicati a spirale all’interno di un canale microscopico per deviare le cellule più grandi, simili alle tumorali, dalle più piccole cellule del sistema immunitario a velocità dei liquidi molto inferiori rispetto al solito. Questo approccio a basso stress e facilmente integrabile potrebbe aiutare i laboratori ad arricchire le cellule rare per diagnosi e monitoraggio terapeutico senza danneggiarle.
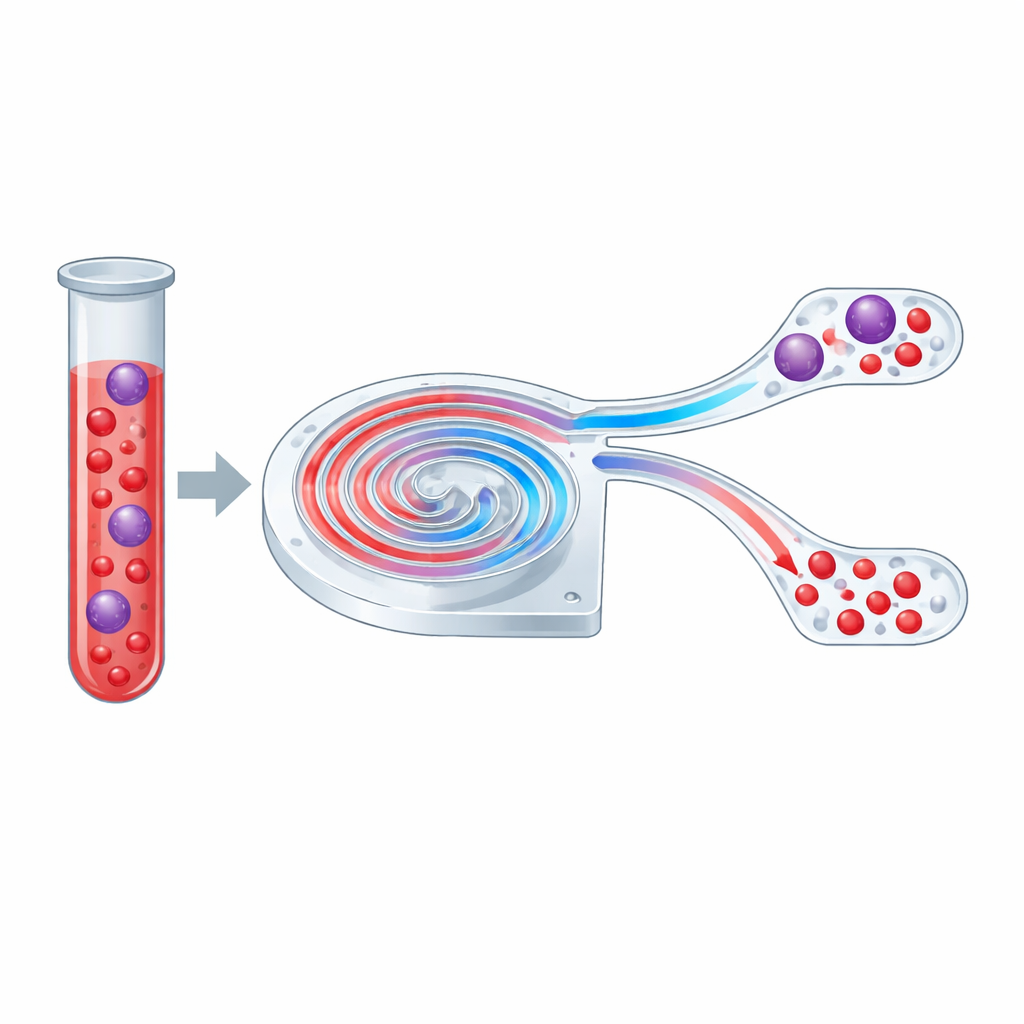
Una piccola strada a spirale per le cellule
Il fulcro dello studio è un microchip trasparente che contiene un canale a spirale più sottile di un capello umano. Quando il fluido scorre in un canale rettilineo, le cellule avvertono principalmente una spinta nella direzione del flusso e una lieve deviazione laterale che dipende dalla loro dimensione. In un percorso curvo e a spirale compare un secondo effetto: il liquido rotola formando coppie di vortici attraverso la sezione del canale, noti come vortici di Dean. Questi vortici trascinano gli oggetti più piccoli attraverso il flusso mentre quelli più grandi restano più vicini a un lato. Sintonizzando questo equilibrio, gli autori hanno progettato una spirale in grado di dividere una miscela di particelle o cellule in due correnti basandosi principalmente sulla dimensione.
Far funzionare le spirali a velocità delicate
La maggior parte dei dispositivi a spirale esistenti ordina in modo efficiente solo quando sono spinti con forza, a portate di centinaia o migliaia di millilitri all’ora. Tali condizioni riducono i tempi di processo ma aumentano lo stress di taglio sulle cellule e rendono difficile collegare la spirale ad altri passaggi microfluidici che preferiscono flussi più lenti e controllati. Il gruppo si è posto un obiettivo diverso: mantenere un forte separazione basata sulla dimensione intorno a 50 millilitri all’ora, un ordine di grandezza più delicato. Per ottenerlo hanno variato sistematicamente la geometria di nove progetti di spirale—cambiando larghezza e altezza del canale e la pendenza della parete esterna—e hanno poi combinato esperimenti con simulazioni al computer del flusso circolante.
Seguire le particelle attraverso i vortici
Per comprendere prima la fisica, i ricercatori hanno fatto scorrere per ogni spirale sfere di plastica fluorescenti di due dimensioni, 10 e 15 micrometri. A bassa velocità entrambi i tipi di sfere si raccoglievano vicino alla parete interna. All’aumentare del flusso, il fascio focalizzato migrava attraverso la sezione verso la parete esterna, ma a velocità di soglia diverse per ciascuna dimensione. Per un disegno rappresentativo, le sfere più piccole si spostavano verso l’esterno intorno a 30 millilitri all’ora, mentre quelle più grandi intorno a 60 millilitri all’ora. Questo ha creato un intervallo intermedio in cui grandi e piccole uscivano da lati opposti. Le simulazioni del moto del fluido hanno rivelato che, a velocità maggiori, le sfere si posizionano molto vicino ai centri dei vortici di Dean, confermando un’idea di lunga data ma in precedenza non dimostrata sul funzionamento di questi dispositivi.
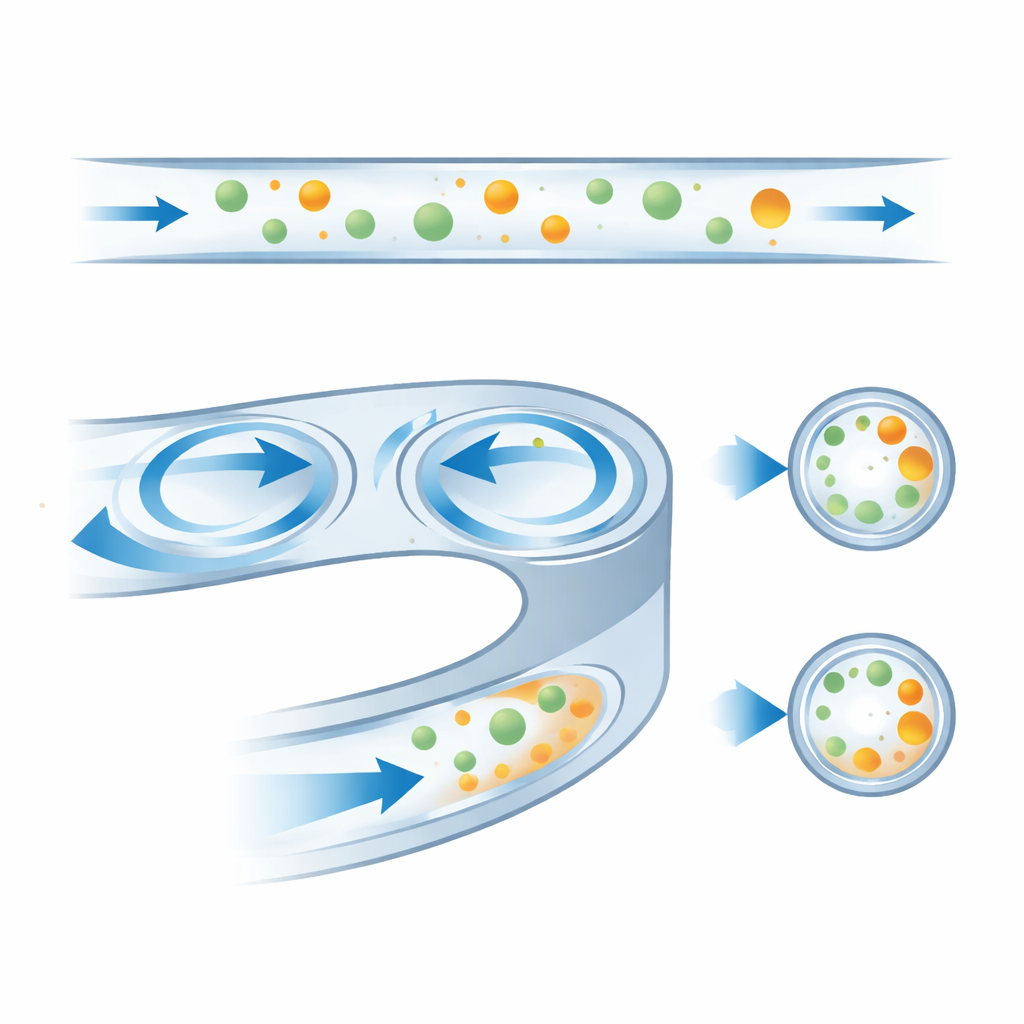
Plasmare il canale per la migliore separazione
Confrontando molti progetti, gli autori hanno identificato come scelte geometriche semplici controllino le prestazioni. Una pendenza maggiore sulla parete esterna spinge i vortici interni più verso l’esterno, spostando le posizioni stabili delle particelle e modificando la portata alla quale cambiano lato. Canali stretti portano i vortici troppo vicini alla parete interna, facendo sì che le particelle vengano attratte troppo presto, mentre canali molto piatti richiedono velocità più elevate prima che avvenga qualsiasi spostamento. Il miglior compromesso usava un canale largo 250 micrometri con una pendenza della parete e un rapporto d’aspetto moderati, che forniva un chiaro divario tra le due dimensioni delle sfere a 40–60 millilitri all’ora e rimaneva robusto a piccole variazioni di flusso.
Dalle sfere di plastica alle cellule tumorali vive
Con la spirale ottimale in mano, il gruppo è passato a campioni biologici. Hanno testato diverse linee cellulari tumorali che imitano le cellule tumorali circolanti e ne hanno confrontato il comportamento con quello dei globuli bianchi provenienti da sangue preparato. Nonostante fossero più morbide e più variabili nelle dimensioni rispetto alle sfere, tutti i tipi cellulari si sono focalizzati in stream stretti e sono passati dal lato interno a quello esterno all’aumentare del flusso, in modo fortemente dipendente dalla dimensione. Operando a 50 millilitri all’ora, il dispositivo ha convogliato circa l’89% dei globuli bianchi verso il lato di “scarto” mantenendo il 75–86% delle cellule più grandi, simili a tumorali, nel lato “arricchito”. È importante che la sopravvivenza cellulare sia rimasta intorno al 98%, anche dopo il passaggio attraverso la spirale a diverse portate.
Cosa significa per i futuri test sul cancro
In termini semplici, gli autori hanno costruito e decifrato un piccolo filtro a spirale in grado di raschiare delicatamente la maggior parte delle cellule di sfondo del sangue trattenendo le più rare e più grandi cellule simili a tumorali, il tutto a velocità relativamente lente e compatibili con le cellule. Chiarendo come si formano i flussi interno ed esterno e come la forma del canale li controlla, il lavoro trasforma una tecnologia in gran parte basata su tentativi ed errori in uno strumento più prevedibile. Da solo, il dispositivo non catturerà ogni singola cellula tumorale, ma fornisce un potente step di pre-arricchimento che può essere collegato direttamente a metodi biologici più selettivi. Questa combinazione potrebbe rendere più facile rilevare, analizzare e monitorare il cancro usando piccoli campioni di fluido dei pazienti.
Citazione: Dupont, E., Artinyan, L., Brunin, C. et al. Effective dean vortex separation at reduced flow rates towards rare cell sorting. Sci Rep 16, 10422 (2026). https://doi.org/10.1038/s41598-026-40845-4
Parole chiave: ordinamento cellulare microfluidico, microcanale a spirale, cellule tumorali circolanti, vortici di Dean, biopsia liquida