Clear Sky Science · it
ABE9 fuso con la nickasi SpRY Cas9 consente la generazione precisa di modelli murini privi di mutazioni collaterali
Strumenti più affilati per costruire modelli di malattia migliori
Molte malattie gravi sono causate da errori di una singola lettera nel nostro DNA. Per comprendere e infine trattare queste condizioni, gli scienziati spesso creano topi che portano le stesse mutazioni dei pazienti umani. Ma riscrivere il DNA in modo così preciso è sorprendentemente difficile: i metodi più vecchi possono danneggiare il genoma, introdurre mutazioni aggiuntive e offuscare i risultati sperimentali. Questo studio presenta uno strumento di editing genico raffinato, chiamato ABE9-SpRY, progettato per cambiare una specifica lettera del DNA lasciando intatte le lettere vicine — e il resto del genoma — nella maggior parte dei casi.
Da tagli pesanti a lievi ritocchi del DNA
L'editing CRISPR-Cas9 tradizionale funziona come una coppia di forbici molecolari, tagliando entrambi i filamenti del DNA. Le cellule riparano queste rotture in modo imperfetto, spesso lasciando piccole inserzioni o delezioni che interrompono i geni in modi imprevedibili. Questo è utile per disattivare i geni, ma non per riprodurre una mutazione precisa che causa una malattia. Gli editor di basi, al contrario, non tagliano il DNA. Piuttosto, spingono chimicamente una lettera del DNA a trasformarsi in un'altra — in questo caso, cambiando A in G — mantenendo intatta la doppia elica. Questo approccio riduce drasticamente grandi delezioni e riarrangiamenti, ma i precedenti editor di adenina soffrivano ancora di tre problemi principali: talvolta modificavano lettere vicine “spettatrici”, potevano raggiungere solo siti accanto a specifiche brevi etichette di sequenza e occasionalmente causavano modifiche in posizioni non intenzionali nel genoma.
Progettare una matita molecolare più selettiva
I ricercatori si sono posti l'obiettivo di affrontare tutte e tre le limitazioni contemporaneamente. Hanno iniziato con ABE9, una variante più recente di editor di basi che concentra la sua attività su una porzione molto stretta di DNA, riducendo così la “finestra di editing” in modo che molte meno lettere vicine vengano modificate per errore. Hanno quindi fuso ABE9 con una Cas9 nickasi ingegnerizzata chiamata SpRY. Diversamente dalla Cas9 standard, che richiede un preciso segnale “NGG” accanto al sito bersaglio, SpRY può riconoscere una gamma molto più ampia di sequenze di DNA. Questo permette di raggiungere posizioni legate a malattie nel genoma che in precedenza erano fuori portata. Lo strumento risultante, ABE9-SpRY, è pensato per essere sia altamente preciso sia molto più flessibile nei siti in cui può operare.
Mettere alla prova il nuovo editor in cellule ed embrioni
Per verificare se ABE9-SpRY rispettasse il progetto, il team lo ha confrontato con un editor ampiamente usato e più aggressivo chiamato ABE8e-SpRY. Hanno preso di mira quattro posizioni rilevanti per malattie in geni che codificano canali ionici (TPC1, TPC2 e TRPM4), che svolgono ruoli importanti nel cuore e nel fegato. In cellule nervose murine coltivate in laboratorio, ABE8e-SpRY ha modificato la lettera bersaglio in modo più efficiente ma ha anche alterato molte basi vicine. ABE9-SpRY, al contrario, ha prodotto meno modifiche complessive ma una frazione molto più alta di risultati “puliti” — letture in cui è stata cambiata solo la lettera prevista, senza mutazioni aggiuntive nella regione locale. Lo stesso schema si è verificato negli embrioni murini. Quando i ricercatori hanno iniettato i componenti di editing nelle uova fecondate, ABE8e-SpRY spesso convertiva quasi tutte le copie del gene bersaglio ma con molti cambiamenti spettatori. ABE9-SpRY ha modificato un numero inferiore di copie complessive, e dove ha agito la sequenza del DNA è stata tipicamente corretta esattamente come previsto.
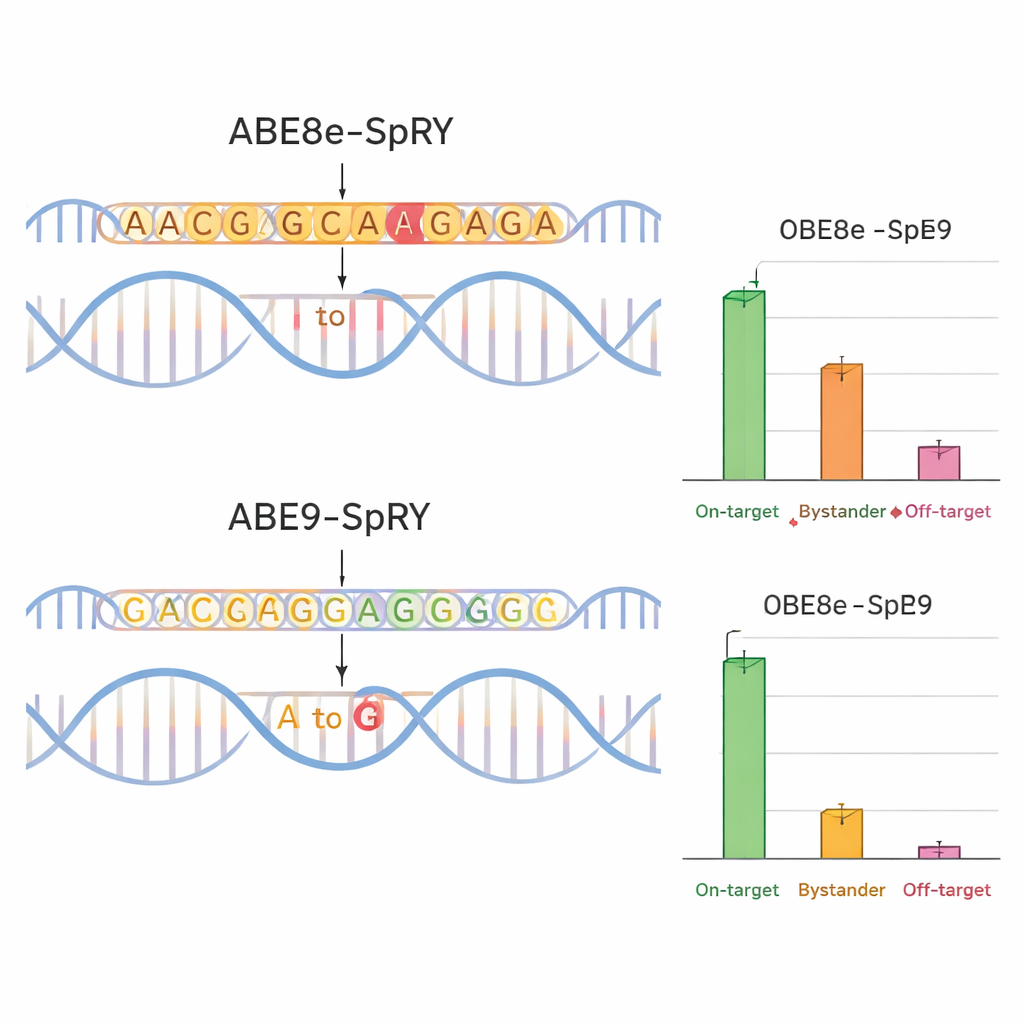
Modifiche più pulite, meno effetti collaterali
La precisione non riguarda solo il vicinato locale del DNA. Il team ha anche esaminato se il loro editor altersse regioni distanti del genoma. Usando previsioni computazionali e sequenziamento mirato, hanno misurato cambiamenti off-target in siti potenzialmente simili negli embrioni murini. ABE8e-SpRY ha frequentemente introdotto cambiamenti non intenzionali A-to-G in queste posizioni, talvolta a livelli sorprendentemente elevati. ABE9-SpRY ha mostrato molti meno eventi di questo tipo, con solo rare modifiche off-target e nessuna attività rilevabile in un test specializzato per danni al DNA indipendenti da Cas9. Importante, quando ABE9-SpRY è stato usato da solo — non in test di gruppo — per introdurre due mutazioni specifiche nei topi, ha generato numerosi animali fondatori in cui la modifica desiderata era presente ad alti livelli e trasmessa in modo affidabile alla progenie, ancora con minime modifiche spettatrici o piccole inserzioni e delezioni.
Estendere l'editing preciso alle cellule staminali umane
Poiché le cellule staminali specifiche del paziente sono sempre più usate per studiare le malattie e testare farmaci, i ricercatori hanno provato ABE9-SpRY anche in cellule staminali pluripotenti indotte umane. Hanno preso di mira la versione umana del gene TPC1 in una posizione equivalente a una delle sedi murine. Utilizzando un reporter fluorescente per arricchire le cellule modificate, hanno osservato che ABE8e-SpRY produceva tassi grezzi di editing più alti ma ancora modificava più basi vicine. ABE9-SpRY ha editato meno alleli nel complesso, ma la proporzione di sequenze perfettamente modificate — una singola modifica intenzionale e nient’altro — era nettamente più alta, con meno inserzioni o delezioni distruttive. Nel lavoro con cellule staminali, in cui singoli cloni vengono espansi per studi dettagliati, questo tipo di modifica “pulita” è generalmente più preziosa dell’efficienza brute-force.
Perché questo è importante per la ricerca sulle malattie futura
Per gli scienziati che cercano di capire come un singolo cambiamento di una lettera del DNA conduca a malattia, mutazioni involontarie aggiuntive possono essere fuorvianti. Questo studio mostra che ABE9-SpRY, pur essendo un po’ meno potente in termini di velocità grezza di editing, può inserire cambiamenti di una singola lettera nei genomi di topi e cellule staminali umane con notevole accuratezza e ampia flessibilità di targeting. Ciò lo rende un promettente cavallo da soma per costruire modelli animali e cellulari fedeli di disturbi genetici umani, specialmente in situazioni in cui anche una sola mutazione estranea potrebbe confondere la biologia o compromettere una potenziale terapia.
Citazione: Ong, J.K., Bhunia, S., Hilbert, B. et al. ABE9 fused to SpRY Cas9 nickase enables precise generation of bystander free mouse models. Sci Rep 16, 7463 (2026). https://doi.org/10.1038/s41598-026-40642-z
Parole chiave: editing delle basi adenina, modelli di malattia CRISPR, genetica murina, effetti off-target, editing genico in hiPSC