Clear Sky Science · it
Legame a bassa affinità dell'anticorpo anti-B7-H3 clone MJ18 con B7-H3 murino non induce regressione tumorale
Perché è importante per la ricerca sul cancro
L'immunoterapia oncologica spesso si basa su anticorpi—proteine prodotte in laboratorio progettate per legarsi alle cellule tumorali e aiutare il sistema immunitario a eliminarle. Un bersaglio promettente è una molecola chiamata B7-H3, abbondante in molti tumori umani ma scarsa nei tessuti sani. Questo articolo esamina a fondo un anticorpo di uso comune nella ricerca, MJ18, che dovrebbe bloccare B7-H3 negli studi su topo. Gli autori rilevano che MJ18 si lega solo marginalmente al bersaglio previsto e non rallenta la crescita tumorale, sollevando dubbi su come interpretare esperimenti preclinici passati che hanno usato questo strumento.
La promessa di una bandiera tumorale
B7-H3 ha suscitato grande interesse perché agisce come uno scudo molecolare: i tumori ricchi di questa proteina tendono ad avere meno cellule immunitarie aggressive al loro interno e sono associati a esiti peggiori per i pazienti. In diversi modelli murini, la cancellazione del gene B7-H3 nelle cellule tumorali scatena un attacco immunitario più potente e può portare alla riduzione o alla scomparsa dei tumori. Queste osservazioni hanno stimolato lo sviluppo di farmaci, cellule immunitarie ingegnerizzate e coniugati anticorpo-farmaco che prendono di mira B7-H3 nei tumori umani. Tuttavia, il modo preciso in cui B7-H3 attenua l’immunità—e persino quale recettore con cui interagisce sulle cellule immunitarie—rimane incerto, soprattutto perché le versioni murina e umana di B7-H3 differiscono strutturalmente.
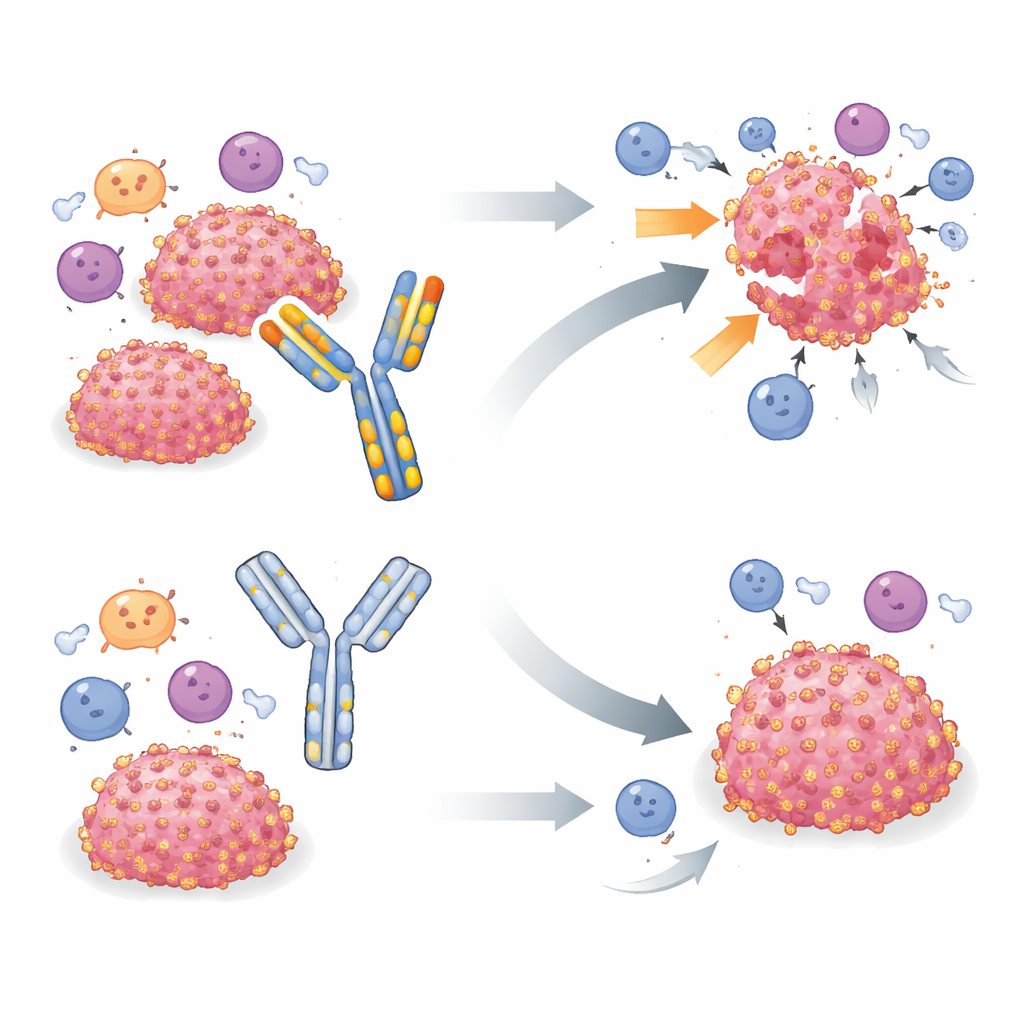
Uno strumento d'uso comune sotto la lente
Per studiare B7-H3 nei topi viventi, molti gruppi hanno fatto affidamento su un unico anticorpo derivato da ratto chiamato MJ18, descritto come capace di riconoscere B7-H3 murino e bloccarne l’attività immunosoppressiva. Studi precedenti che hanno impiegato MJ18 in vari modelli di malattia, compresi tumori, spesso riportavano una crescita tumorale più lenta e una sopravvivenza migliore. Il team attuale ha inizialmente testato MJ18 in un modello murino di rabdomiosarcoma, un tumore dei tessuti molli dell’infanzia in cui B7-H3 era già stato segnalato come importante meccanismo di evasione. Quando MJ18 non ha migliorato il controllo del tumore, i ricercatori hanno esteso i test ad altri due tipi tumorali positivi per B7-H3—pancreatico e mammario—that sono chiaramente sensibili alla cancellazione genica di B7-H3. In tutti e tre i modelli, l’eliminazione di B7-H3 nelle cellule tumorali ha ritardato o eliminato robustamente i tumori, ma il trattamento dei topi con MJ18 a dosi e regimi simili a quelli riportati in letteratura non ha avuto alcun impatto rilevabile sulla crescita tumorale o sulla sopravvivenza.
Verificare se MJ18 colpisce davvero il bersaglio
Gli autori si sono quindi posti una domanda di base sorprendentemente mai affrontata in modo rigoroso: MJ18 si lega veramente a B7-H3 murino, e con quale forza? Mediante citometria a flusso hanno confrontato MJ18 con un altro anticorpo, EPNCIR122, noto per rilevare B7-H3. Su diverse linee cellulari tumorali murine, EPNCIR122 ha prodotto un segnale chiaro che scompariva quando il gene B7-H3 veniva eliminato, confermandone la specificità. MJ18, al contrario, non ha mostrato un legame convincente nemmeno ad alte concentrazioni. Nell’analisi delle cellule immunitarie spleniche, MJ18 si è legato, ma il pattern non corrispondeva a B7-H3, e EPNCIR122 non ha rilevato B7-H3 su queste cellule, suggerendo che MJ18 si stesse attaccando a qualcos’altro.
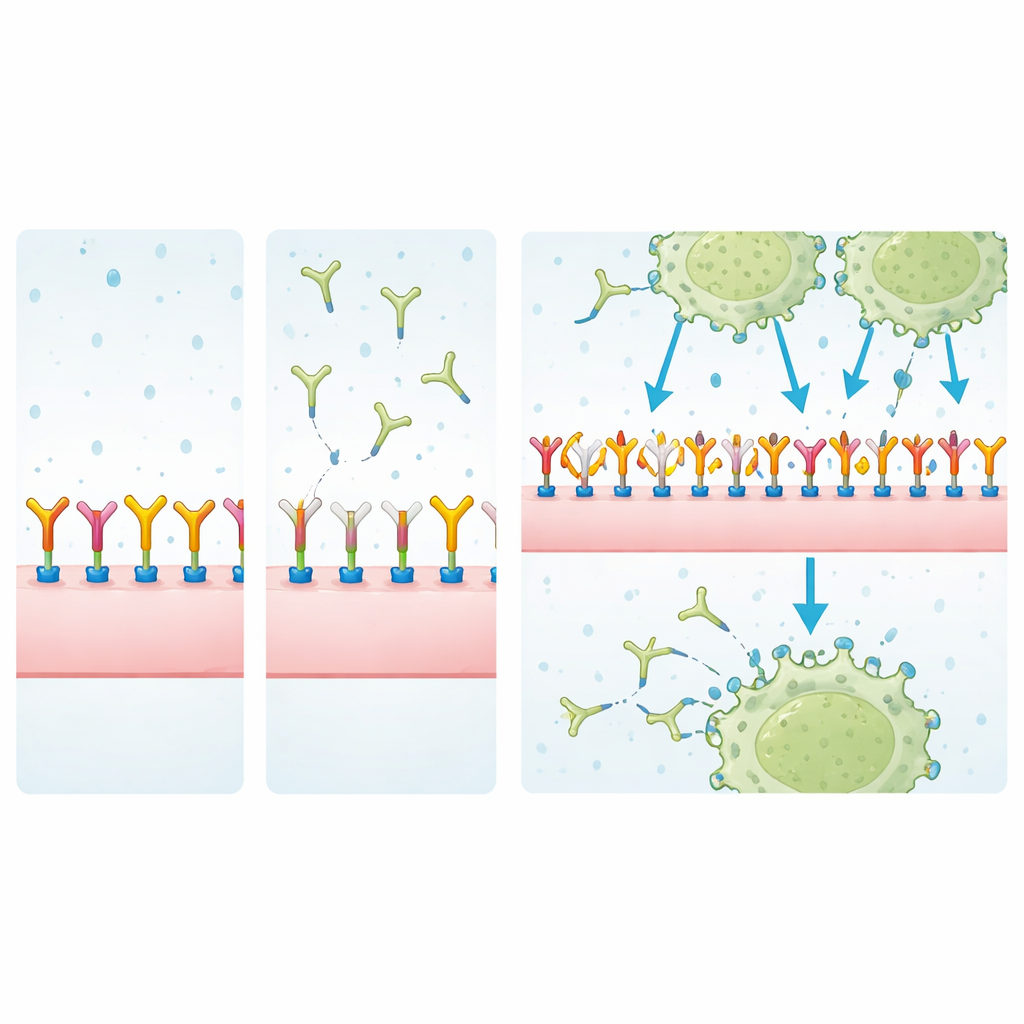
Approfondire i partner di legame
Per identificare cosa MJ18 potrebbe effettivamente riconoscere, i ricercatori hanno isolato le proteine di superficie cellulare usando MJ18 o EPNCIR122 e le hanno analizzate mediante spettrometria di massa, escludendo i contaminanti di fondo comuni. Nelle cellule tumorali, EPNCIR122 ha arricchito fortemente B7-H3 rispetto ad altre proteine, confermandone l’elevata specificità. MJ18, invece, ha pescato un miscuglio di proteine in cui B7-H3 compariva solo debolmente e a livelli simili a leganti non specifici. Misurazioni con risonanza plasmonica di superficie, una tecnica sensibile per quantificare le interazioni molecolari, hanno chiarito il quadro: l’affinità di MJ18 per B7-H3 murino era circa 7.000 volte più debole rispetto a quella di EPNCIR122—ben al di sotto di quanto tipico per anticorpi terapeutici.
Quando gli anticorpi vengono catturati dalle cellule sbagliate
La storia non si è fermata al legame debole. Nelle cellule della milza, test aggiuntivi hanno mostrato che MJ18 e anticorpi simili di ratto venivano riconosciuti dai recettori Fc murini—molecole sulle cellule immunitarie che legano naturalmente la porzione Fc degli anticorpi. Il blocco di questi recettori ha ridotto nettamente il segnale di MJ18, implicando che gran parte del legame apparente derivava dall’interazione delle cellule immunitarie con l’anticorpo stesso, piuttosto che dal riconoscimento da parte di MJ18 di una proteina specifica di superficie. I tentativi di identificare un partner proteico unico per MJ18 sulle cellule immunitarie hanno prodotto solo candidati a livelli indistinguibili dal rumore di fondo. Nel complesso, i dati suggeriscono che MJ18 si comporta in larga parte come un anticorpo non specifico e a bassa affinità le cui interazioni sono dominate dall’ingaggio dei recettori Fc piuttosto che dal riconoscimento preciso di B7-H3.
Quali implicazioni per il futuro
Per i non specialisti, il messaggio principale è semplice: mentre B7-H3 rimane un bersaglio interessante in molti tumori, l’anticorpo MJ18 non è un dardo affidabile. Si lega a B7-H3 nei topi solo debolmente e non riproduce il potente controllo tumorale osservato quando il gene B7-H3 viene rimosso. Studi murini precedenti che riportavano benefici significativi con MJ18 potrebbero quindi riflettere altri effetti—ad esempio l’interazione della porzione Fc dell’anticorpo con recettori delle cellule immunitarie—invece di un vero blocco di B7-H3. Gli autori sostengono che il campo necessita urgentemente di anticorpi murini contro B7-H3 ben validati e ad alta affinità, e che i ricercatori dovrebbero confermare routinariamente specificità e forza di tali strumenti. Solo con reagenti affidabili le intuizioni dai modelli animali potranno guidare con fiducia lo sviluppo di terapie mirate a B7-H3 per i pazienti.
Citazione: Gulyás, D., Nammor, T., Frizzell, J. et al. Low-affinity binding of anti-B7-H3 clone MJ18 to murine B7-H3 fails to induce tumor regression. Sci Rep 16, 9519 (2026). https://doi.org/10.1038/s41598-026-40628-x
Parole chiave: B7-H3, immunoterapia del cancro, validazione degli anticorpi, checkpoint immunitari, modelli tumorali