Clear Sky Science · it
Analisi teorica della soppressione a bassa potenza tramite optogenetica dei potenziali d’azione nei cardiomiociti ventricolari umani espressi con canalarodopsine selettive per il potassio
Un modo più delicato, basato sulla luce, per calmare un cuore in corsa
I ritmi cardiaci rapidi e caotici possono provocare svenimenti, ictus o morte improvvisa. I trattamenti attuali—farmaci potenti, defibrillatori impiantati o scosse ad alta energia—possono salvare la vita ma sono anche dolorosi e imprecisi. Questo studio esplora un’idea molto diversa: usare deboli lampi di luce e proteine appositamente progettate per spingere con delicatezza le cellule cardiache verso un ritmo sicuro e stabile, impiegando molta meno energia rispetto agli approcci attuali.
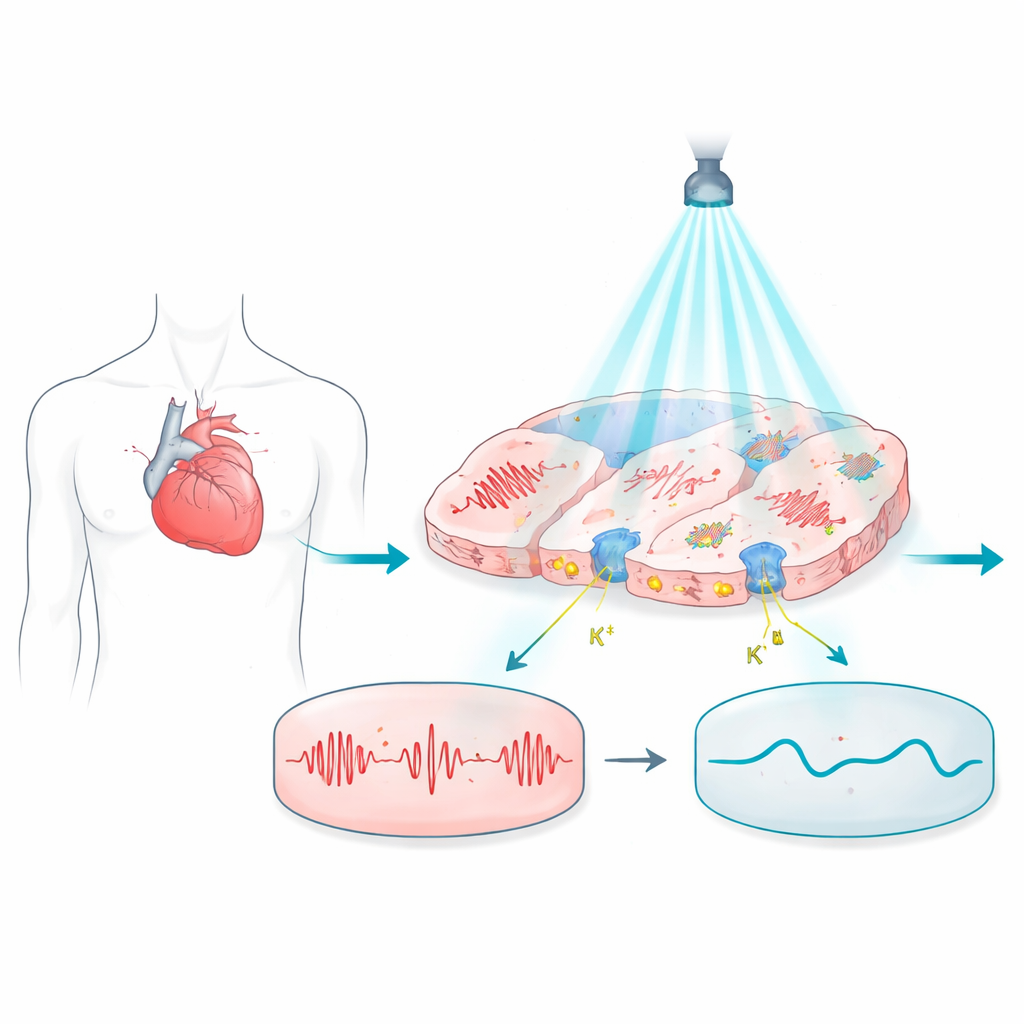
Fare luce sui battiti problematici
Il lavoro si basa sull’optogenetica, una tecnica in cui le cellule vengono dotate di proteine sensibili alla luce in modo che la loro attività elettrica possa essere controllata con lampi luminosi. Nel cuore, queste proteine potrebbero in principio sostituire gli elettrodi metallici, offrendo controllo senza contatto e indolore. Tuttavia, la maggior parte delle proteine sensibili alla luce utilizzate finora tende a spingere il potenziale di membrana verso valori più positivi, verso uno stato eccitato, il che rende difficile mantenere le cellule quiete a riposo o regolare con precisione la durata di ogni battito. Questo ne limita l’utilità per spegnere in sicurezza ritmi pericolosi o correggere disturbi elettrici che dipendono da tempistiche sottili.
Nuovi interruttori luminosi tarati sul “riposo” del cuore
Proteine scoperte di recente, chiamate canalarodopsine selettive per il potassio, tra cui WiChR e HcKCR1, promettono di correggere questo disallineamento. A differenza delle proteine più vecchie che lasciano passare una miscela di ioni carichi, questi canali preferiscono fortemente il potassio e tendono naturalmente a riportare il potenziale di membrana verso lo stesso livello negativo che la cellula assume a riposo. Gli autori hanno costruito modelli computazionali dettagliati di cellule cardiache ventricolari umane che esprimono questi nuovi canali e le hanno confrontate con due opsine ben note e più eccitatorie, ChR2(H134R) e ChRmine. Simulando come queste cellule rispondono a diverse lunghezze d’onda e intensità di luce, hanno potuto esplorare in sicurezza condizioni difficili o dispendiose da testare in cuori reali.
Luce soffusa, controllo deciso
Le simulazioni mostrano che i canali selettivi per il potassio forniscono un controllo molto più economico e stabile. WiChR, in particolare, potrebbe arrestare completamente i potenziali d’azione—i brevi picchi elettrici che innescano ogni battito cardiaco—usando intensità luminose centinaia o migliaia di volte inferiori rispetto a quanto necessario per molti strumenti precedenti. Sotto illuminazione continua, WiChR e HcKCR1 mantengono il potenziale di membrana vicino al normale livello di riposo, tenendo efficacemente la cellula in uno stato quieto e sicuro. Per contro, ChR2 e ChRmine tendevano a spingere il potenziale verso valori più positivi, talvolta bloccando l’attività ma solo dopo aver portato la cellula in uno stato stressato e ipereccitato. WiChR ha funzionato bene anche con brevi impulsi luminosi, prevenendo in modo affidabile gli spike delle cellule cardiache battito dopo battito, suggerendo che potrebbe far fronte a ritmi cardiaci rapidi senza surriscaldare i tessuti o sprecare energia.
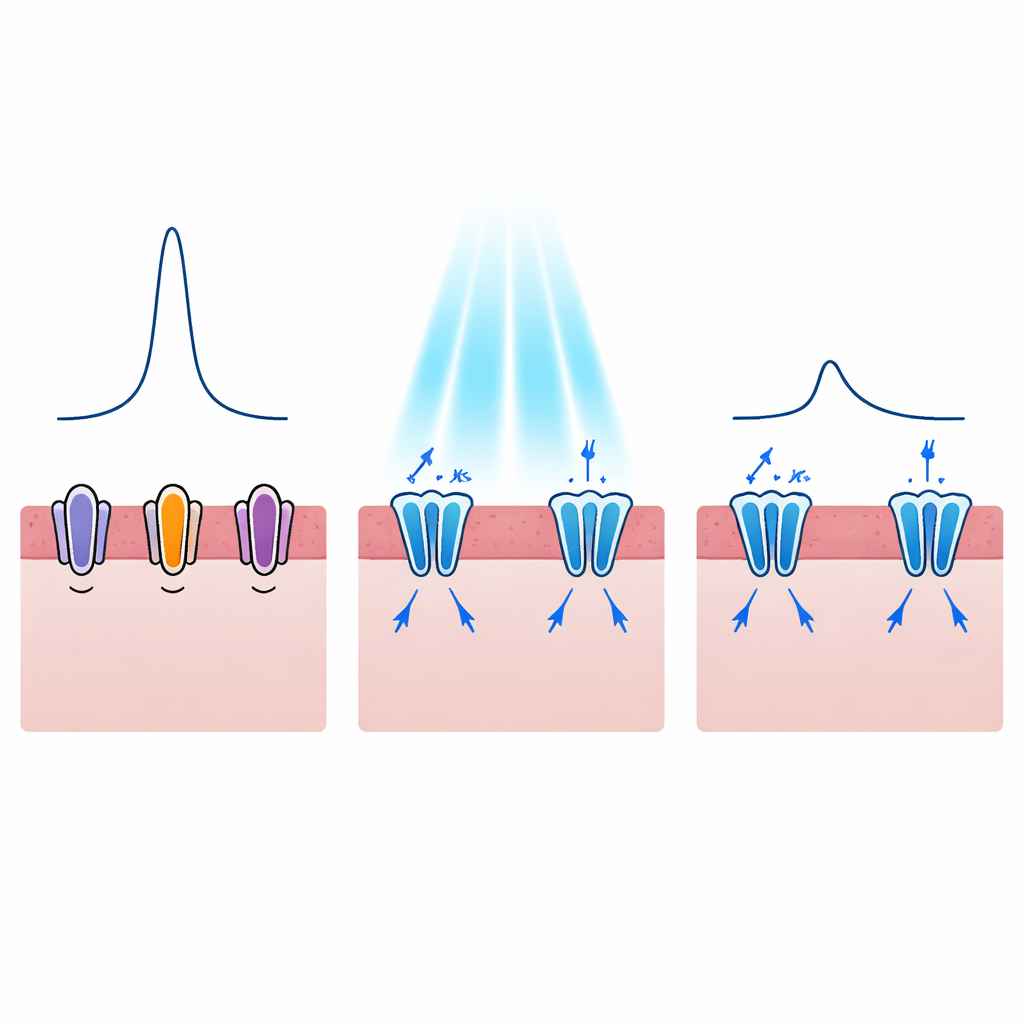
Rimodellare ogni battito, non solo fermarlo
Le aritmie pericolose sono spesso collegate non solo al fatto che una cellula cardiaca spara, ma anche a quanto a lungo rimane eccitata. In disturbi come la sindrome del QT lungo, l’impulso elettrico di ciascun battito si allunga, aumentando la probabilità di evolvere in ritmi fatali. Gli autori si sono quindi chiesti se i canali potassio attivabili dalla luce possano accorciare questo impulso in modo controllato. I loro modelli hanno mostrato che attivare WiChR o HcKCR1 durante la fase di plateau del potenziale d’azione genera forti correnti di potassio verso l’esterno che riportano il potenziale verso il basso più precocemente. All’aumentare dell’intensità luminosa, la durata dell’impulso elettrico scende da circa 300 millisecondi a circa la metà di quel valore, e questo effetto può essere ottenuto anche con flash luminosi molto brevi. WiChR tende a produrre periodi di quiete più duraturi, mentre HcKCR1 offre un recupero più rapido una volta spenta la luce, suggerendo potenziali usi clinici differenti.
Dai modelli al computer alle terapie future
Nel complesso, lo studio conclude che i canali luminosi selettivi per il potassio, in particolare WiChR, sono strumenti promettenti per un controllo delicato e a bassa potenza del cuore. Possono sia silenziare attività elettrica fuori controllo sia accorciare battiti troppo lunghi, mantenendo al contempo il potenziale di membrana vicino al suo stato naturale di riposo. Sebbene i risultati derivino da simulazioni dettagliate su singole cellule piuttosto che da esperimenti sull’intero cuore, forniscono indicazioni quantitative su quanta luce potrebbe essere necessaria, quando applicarla e quali varianti proteiche siano più adatte a obiettivi diversi. A lungo termine, questa linea di ricerca apre alla possibilità che i cardiologi possano usare fasci di luce finemente tarati, anziché scosse dolorose, per prevenire o fermare aritmie potenzialmente letali.
Citazione: Dixit, N., Pyari, G. & Roy, S. Theoretical analysis of low-power optogenetic suppression of action potentials in human ventricular cardiomyocytes expressed with potassium-selective channelrhodopsins. Sci Rep 16, 9765 (2026). https://doi.org/10.1038/s41598-026-40578-4
Parole chiave: optogenetica cardiaca, soppressione delle aritmie, canalarodopsine per il potassio, durata del potenziale d’azione, sindrome del QT lungo