Clear Sky Science · it
Sexaggio in ovo e genotipizzazione mediante tecniche PCR: un contributo ai principi 3R nell’allevamento di polli
Perché ciò che avviene dentro un uovo conta
Ogni anno milioni di pulcini maschi vengono soppressi poco dopo la schiusa perché non utili per la produzione di uova. Allo stesso tempo, laboratori di ricerca in tutto il mondo schiudono più animali di quanti ne servano realmente, semplicemente perché non riescono a determinare il sesso o il profilo genetico di un embrione in tempo utile. Questo studio presenta un modo pratico per “leggere” il sesso e i geni di un pulcino mentre è ancora in sviluppo dentro l’uovo, usando test del DNA di routine. Effettuando la procedura precocemente e in modo delicato, il metodo mira a evitare la schiusa di animali in eccesso e a ridurre la sofferenza, senza richiedere costose apparecchiature industriali.
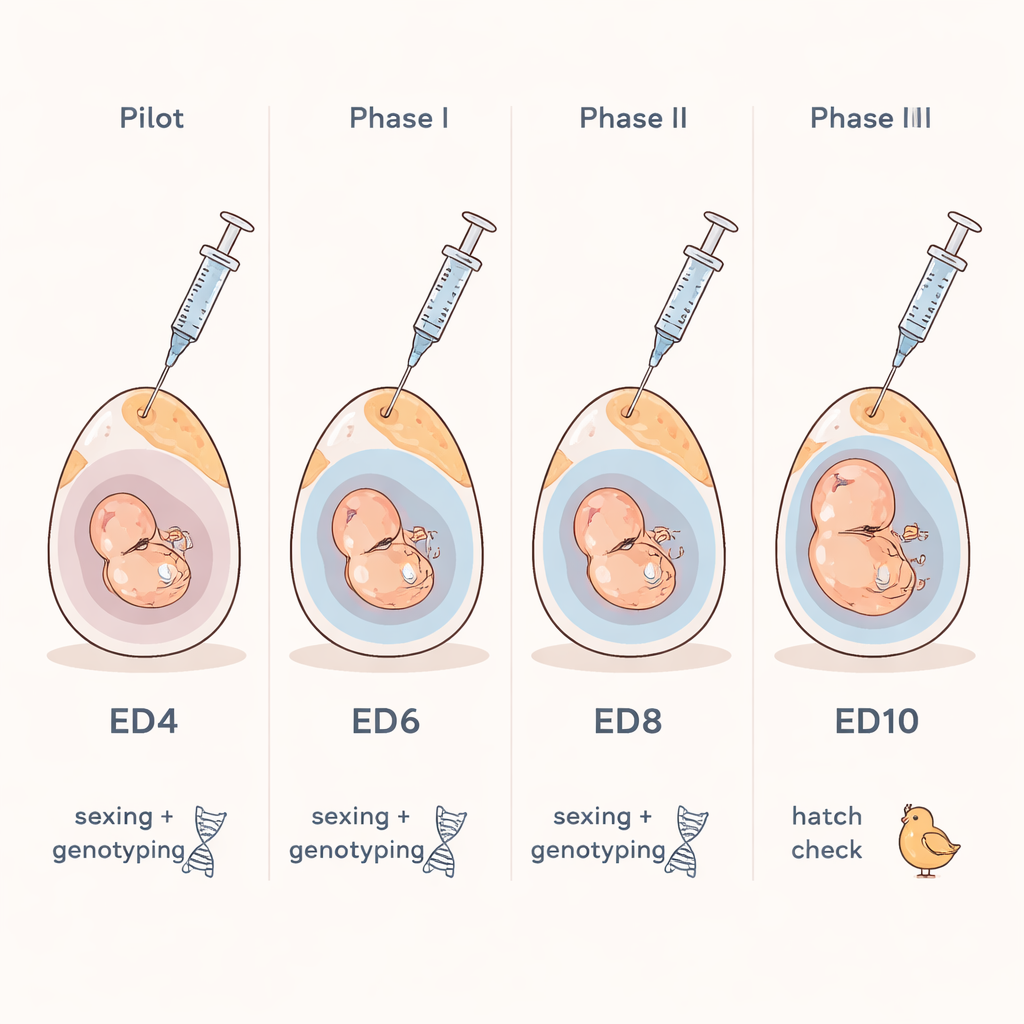
Osservare l’interno dell’uovo senza aprirlo
I ricercatori si sono concentrati su una domanda semplice: è possibile prelevare in sicurezza una minuscola quantità di fluido da un uovo fecondato e usarla per identificare il sesso dell’embrione e i tratti genetici chiave? Si sono ispirati a un concetto noto in medicina umana, dove i medici analizzano i fluidi attorno a un feto per verificare condizioni genetiche. Nei polli, una sottile sacca piena di liquido chiamata allantoide si forma attorno all’embrione man mano che cresce. Al giorno sette di incubazione questa sacca contiene abbastanza fluido perché un ago sottile possa raggiungerla senza toccare l’embrione. Il team ha usato una luce intensa per localizzare la camera d’aria all’estremità arrotondata dell’uovo, ha praticato un foro delle dimensioni di uno spillo nel guscio e ha aspirato poche gocce di fluido con una siringa minuscola.
Da poche gocce a un’impronta genetica
Il fluido prelevato da uova allo stadio iniziale contiene solo tracce di DNA. Per ovviare a ciò, gli scienziati hanno prima amplificato tutto il materiale genetico presente in ogni campione, creando molte copie senza alterarne il contenuto. Hanno quindi applicato due test di laboratorio di routine: una reazione a catena della polimerasi (PCR) standard e una variante chiamata Kompetitive Allele Specific PCR (KASP). Entrambi i test possono distinguere i cromosomi sessuali dei pulcini maschi e femmine e possono anche rilevare marcatori genetici specifici, come la mutazione responsabile del guscio azzurro o la presenza di un gene inserito in laboratorio in linee di ricerca speciali. Su oltre 800 uova di diverse razze — incluse ovaiole commerciali, incroci Araucana dai colori vivaci e una linea di ricerca geneticamente modificata — questi metodi hanno fornito identificazioni corrette in circa il 92–100% dei casi.
Trovare il momento più sicuro per il prelievo
Campionare troppo presto rischia di danneggiare strutture fragili vitali per l’embrione, mentre campionare troppo tardi lascia poco tempo per agire sui risultati. Per individuare la finestra ideale, il team ha prima coltivato embrioni senza guscio per osservare come membrane e spazi fluidi si espandono nel tempo. Hanno poi eseguito una serie di prove a stadi in uova integre. Il fluido poteva essere raccolto a partire dal giorno quattro, ma i tassi di successo per i test del DNA erano inferiori in questi primi giorni e la procedura risultava tecnicamente più difficile. Confrontando i tassi di schiusa tra uova perforate e controlli intatti, hanno riscontrato che il giorno sette rappresenta il miglior compromesso: era disponibile una quantità sufficiente di fluido allantoideo chiaro, i test del DNA funzionavano in modo affidabile e la maggior parte degli embrioni sopravviveva fino alla schiusa. A questo punto restano ancora diversi giorni prima dell’eventuale insorgenza della percezione del dolore nell’embrione di pulcino, offrendo un margine etico per le decisioni.
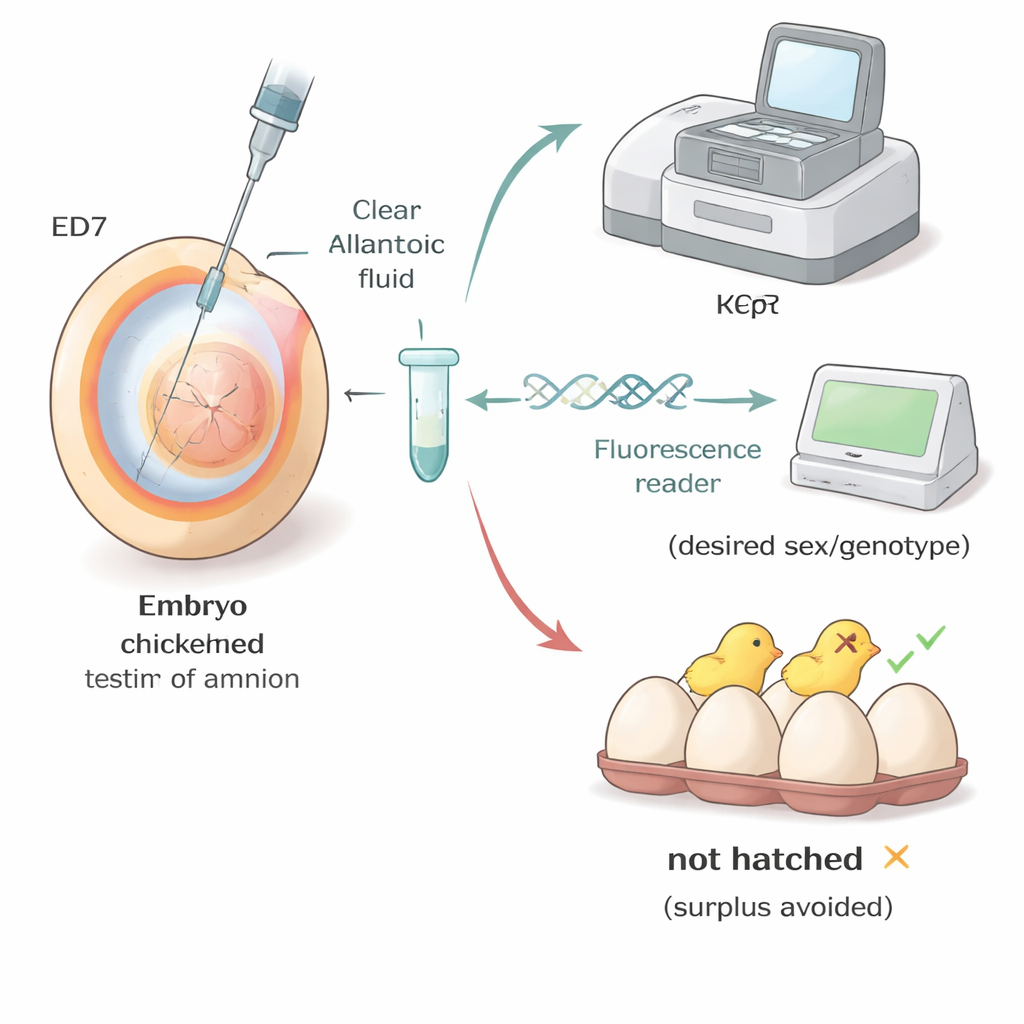
Applicare il metodo in allevamenti reali
I ricercatori hanno testato il loro flusso di lavoro in condizioni simili a quelle di impianti di allevamento e laboratori universitari. In linee di ovaiole commerciali marroni e bianche, uova campionate tra il giorno quattro e il giorno sette hanno mostrato che la schiudibilità generalmente migliorava quando il prelievo veniva effettuato più tardi, con i risultati migliori ancora al giorno sette. In una linea specializzata «surrogate host» utilizzata per la genetica avanzata, il team è andato oltre: ha determinato sesso e genotipo degli embrioni al giorno sette, quindi ha scelto solo quelli con la combinazione di sesso e genetica desiderata per proseguire fino alla schiusa. Quasi tutti gli embrioni selezionati sono schiusi in pulcini sani che hanno sviluppato come previsto, dimostrando che la selezione precoce può ridurre drasticamente il numero di animali indesiderati senza compromettere la qualità dei pulcini.
Cosa significa questo per il benessere animale e la ricerca
Per un non specialista, il messaggio centrale è semplice: con una puntura e strumenti di laboratorio di routine, è ora possibile sapere, mentre il pulcino è ancora in sicurezza dentro l’uovo, se è maschio o femmina e se porta particolari tratti genetici. Lo studio dimostra che eseguire questo intervento intorno al giorno sette di incubazione è sia tecnicamente affidabile sia sufficientemente delicato da permettere la sopravvivenza della maggior parte degli embrioni. Consentendo di rimuovere gli embrioni indesiderati prima che siano presumibilmente in grado di provare dolore, l’approccio supporta i largamente accettati principi 3R: sostituire, ridurre e perfezionare l’uso degli animali nella scienza. Per incubatoi e laboratori di ricerca, questa tecnica offre un percorso realistico verso meno animali in eccesso, un uso migliore delle risorse e standard di benessere più elevati — senza la necessità di complesse macchine industriali.
Citazione: Dierks, C., Förster, A., Meunier, D. et al. In ovo sexing and genotyping using PCR techniques: a contribution to the 3R principles in chicken breeding. Sci Rep 16, 7464 (2026). https://doi.org/10.1038/s41598-026-40562-y
Parole chiave: embrione di pollo, sexaggio in ovo, genotipizzazione PCR, benessere animale, principi 3R