Clear Sky Science · it
Scoperta dell’idrossitriazolo come potenziale inibitore della glyoxalase‑I mediante tecniche di progettazione di farmaci assistita da computer
Perché bloccare un piccolo spazzino cellulare potrebbe combattere il cancro
Le cellule tumorali spesso crescono così in fretta da annegare nei loro stessi scarti. Uno dei loro trucchi di sopravvivenza è una squadra di pulizia incorporata che detossifica i prodotti di scarto reattivi derivati dalla combustione degli zuccheri. Questo studio esplora come disattivare un membro chiave di quella squadra, un enzima chiamato glyoxalase‑I, usando il computer per setacciare decine di migliaia di molecole e poi esperimenti per testare i migliori candidati. L’obiettivo è scoprire nuovi punti di partenza per farmaci che un giorno potrebbero aiutare i medici a avvelenare selettivamente le cellule tumorali dall’interno.
Un sistema di smaltimento nascosto dentro le nostre cellule
Ogni cellula scompone costantemente gli zuccheri per produrre energia, e questo processo genera un rifiuto reattivo chiamato metilgliossale. In quantità normali, il nostro organismo converte il metilgliossale in acido lattico innocuo tramite il sistema glyoxalase, una via in due fasi che si basa sulla molecola helper glutatione. La glyoxalase‑I è il primo e più cruciale passo di questa catena. Le cellule tumorali, che bruciano zuccheri a ritmo frenetico, dipendono fortemente dalla glyoxalase‑I per impedire che il metilgliossale raggiunga livelli tossici. Se questo enzima viene bloccato, il metilgliossale si accumula e può spingere le cellule danneggiate verso la morte programmata. Ciò rende la glyoxalase‑I un bersaglio interessante per farmaci anticancro che colpiscono una debolezza fondamentale del metabolismo tumorale.
Esplorare lo spazio chimico con silicio e statistiche
Piuttosto che testare sostanze a caso in laboratorio, i ricercatori hanno utilizzato la progettazione di farmaci assistita da computer per cercare in una ampia collezione commerciale di oltre 50.000 piccole molecole. Software specializzati hanno prima pulito e standardizzato ogni molecola, quindi hanno previsto la sua forma tridimensionale e il comportamento a pH simile a quello fisiologico. Un rapido screening virtuale ha valutato quanto bene ciascun candidato potesse adattarsi al sito attivo della glyoxalase‑I. Il team ha poi applicato regole semplici su dimensione, solubilità e altre proprietà di drug‑likeness per scartare le molecole improbabili di funzionare nell’organismo. Un programma di docking più dettagliato ha esaminato come le molecole più promettenti potevano orientarsi all’interno dell’enzima, in particolare come potessero raggiungere e agganciare l’atomo di zinco che si trova al centro della chimica della glyoxalase‑I.
Un nuovo modo di afferrare il nucleo metallico dell’enzima
Tentativi precedenti di bloccare la glyoxalase‑I si sono concentrati su gruppi chimici ben noti, come gli acidi carbossilici e gli acidi idrossamici, efficaci nel legare i metalli ma spesso caratterizzati da scarsa stabilità o effetti collaterali indesiderati. Il presente studio ha invece individuato un diverso tipo di unità «afferrametallo»: un anello idrossitriazolo. Tra sedici molecole classificate ai vertici e scelte per l’acquisto e i test in laboratorio, una contenente questo anello — codificata SPB07393SC — è emersa come la più interessante. Nel docking virtuale, il suo gruppo idrossitriazolo raggiungeva l’atomo di zinco, mentre i due anelli aromatici si infilavano in tasche apolari vicine dell’enzima. Simulazioni al computer del complesso su decine di nanosecondi suggerivano che la molecola restasse saldamente legata, con distanze stabili, una forma proteica compatta e una rete persistente di legami a idrogeno.
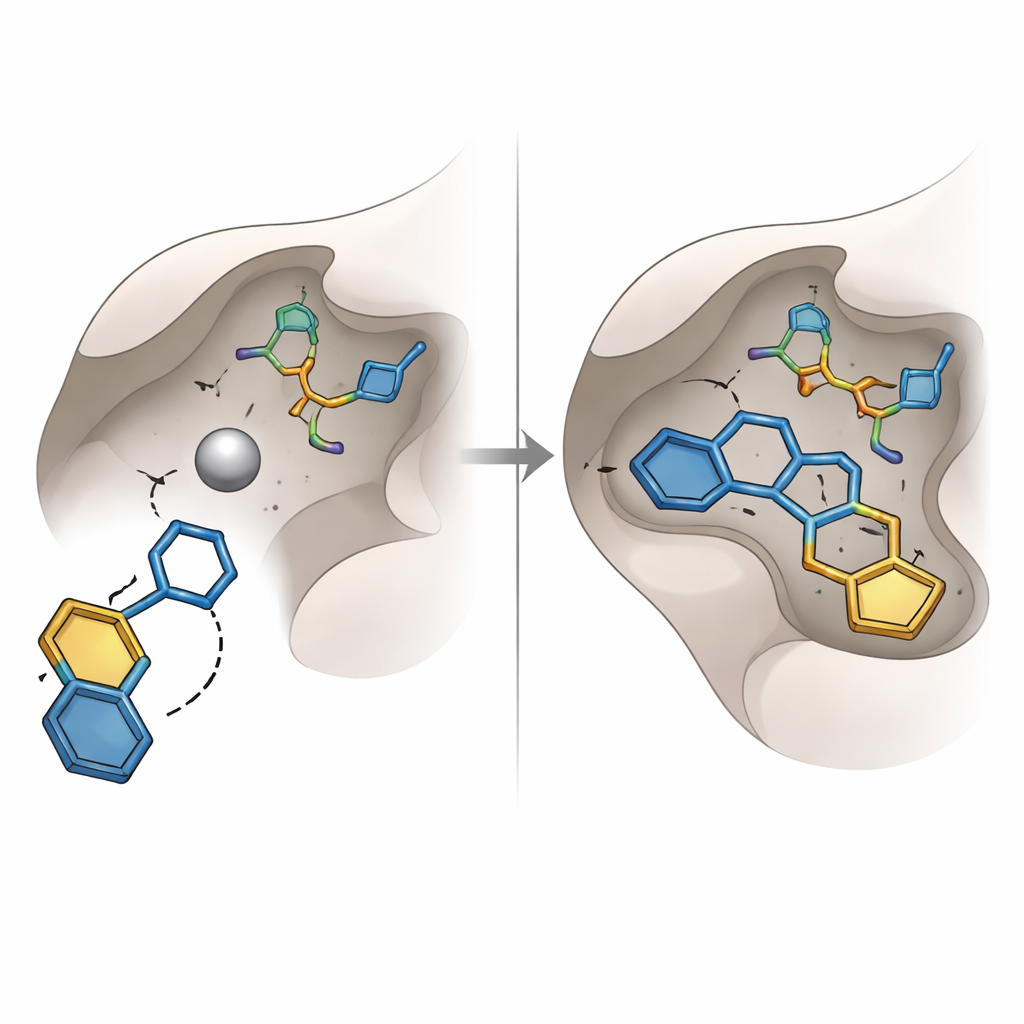
Mettere alla prova le previsioni
Per verificare se i modelli computazionali si traducessero in effetti reali, il team ha misurato quanto bene le molecole selezionate rallentassero l’attività della glyoxalase‑I umana purificata in un saggio su piastra. Quindici delle sedici candidate hanno mostrato solo inibizione debole o trascurabile nelle condizioni testate, evidenziando i rischi di fare affidamento esclusivamente su punteggi di docking statico. Al contrario, SPB07393SC ha inibito fortemente l’enzima, con una potenza a metà nel range dei micromolari che la rende un solido «hit» iniziale piuttosto che un farmaco finito. Strumenti software aggiuntivi hanno previsto che questa molecola dovrebbe avere una solubilità accettabile, buona assorbibilità, la capacità di raggiungere il cervello se necessario e una bassa probabilità di provocare certe tossicità genetiche o epatiche, sebbene queste previsioni di sicurezza richiedano ancora conferma sperimentale.
Cosa significa per i futuri farmaci contro il cancro
Il lavoro introduce l’idrossitriazolo come un nuovo modo per ancorare i candidati farmaceutici all’atomo di zinco al centro della glyoxalase‑I, ampliando il repertorio di strategie chimiche a disposizione dei progettisti di farmaci. Pur essendo la SPB07393SC soltanto un punto di partenza, la sua combinazione di potenza nell’inibire l’enzima, comportamento previsto simile a quello di un farmaco e legame stabile nelle simulazioni dinamiche la segnala come uno scaffold promettente per ulteriori ottimizzazioni. Più in generale, lo studio mostra sia i punti di forza sia i limiti dello screening guidato dal computer: può rapidamente ridurre vaste librerie chimiche a pochi contendenti realistici, ma esperimenti di laboratorio accurati restano essenziali per rivelare quali molecole disabilitano davvero l’enzima su cui le cellule tumorali fanno affidamento per gestire i loro rifiuti tossici.
Citazione: Al-Qazzan, M., Al-Balas, Q., Alnajjar, B. et al. Discovery of hydroxytriazole as a potential glyoxalase-I inhibitor utilizing computer-aided drug design techniques. Sci Rep 16, 9945 (2026). https://doi.org/10.1038/s41598-026-40497-4
Parole chiave: glyoxalase I, metabolismo del cancro, progettazione di farmaci assistita da computer, inibitori che legano lo zinco, docking molecolare