Clear Sky Science · it
Portatori nanometrici ferritici rivestiti di chitosano a risposta a stimoli per la somministrazione mirata di capsaicina e attività bioselettiva verso HepG2 dipendente dal nucleo
Spezia con un potere nascosto
I peperoncini non aggiungono solo piccante al cibo: la loro sensazione di bruciore deriva dalla capsaicina, un composto naturale che può anche uccidere le cellule tumorali. Tuttavia l’impiego della capsaicina come farmaco è risultato difficile perché si scioglie poco in acqua, viene eliminata rapidamente dall’organismo e irrita i tessuti sani a dosi elevate. Questo studio esplora un modo per domare quella molecola infuocata inserendola in particelle minuscole e intelligenti che possono trasportare la capsaicina in modo sicuro nel flusso sanguigno e rilasciarla principalmente all’interno dei tumori epatici.
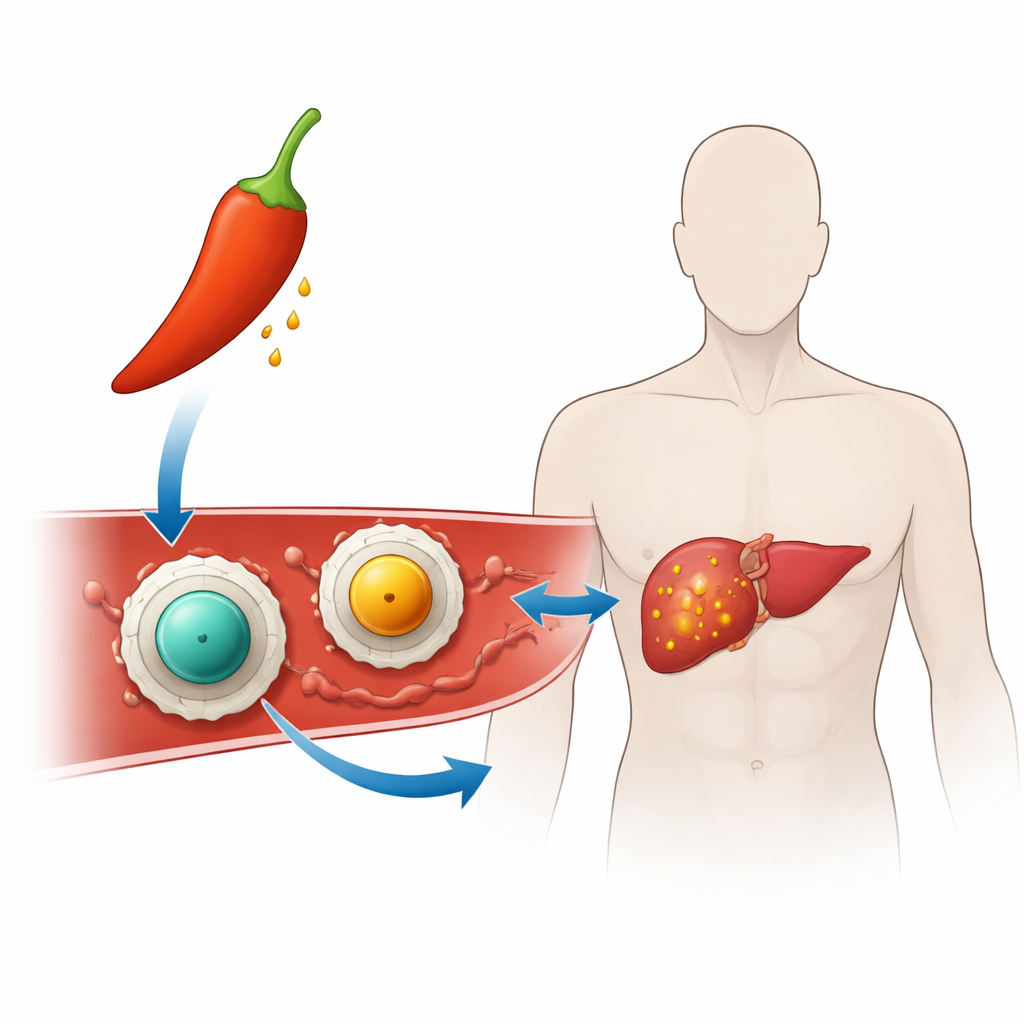
Trasformare il peperoncino in terapia mirata
I ricercatori hanno costruito “nanoveicoli” – particelle migliaia di volte più piccole di un granello di sabbia – per trasportare la capsaicina verso le cellule tumorali. Ciascun nanoveicolo ha un nucleo solido costituito da un minerale magnetico chiamato ferrite (o ferrite di zinco o ferrite di manganese) avvolto in un sottile rivestimento di chitosano, una sostanza simile a uno zucchero derivata da crostacei già impiegata in prodotti medici e alimentari. Questo rivestimento rende le particelle più facilmente sospendibili in acqua e le aiuta ad aderire alle superfici cellulari e al DNA, caratteristica importante per l’effetto antitumorale. Caricando la capsaicina nello strato di chitosano, il gruppo sperava di mantenere il farmaco stabile e nascosto fino al raggiungimento dell’ambiente ostile all’interno di un tumore.
Rilascio intelligente nelle condizioni tumorali
Una caratteristica chiave dei tumori è che tendono a essere più acidi e più ricchi di alcuni antiossidanti, come il glutatione, rispetto ai tessuti sani. Il gruppo ha progettato i propri nanoveicoli per riconoscere queste condizioni. Nei test di laboratorio a pH simile a quello del sangue normale, meno del 10 percento della capsaicina immagazzinata è fuoriuscito in due giorni, suggerendo che le particelle trasporterebbero il loro carico in sicurezza durante la circolazione. In condizioni simili a quelle tumorali – più acide e con abbondante glutatione – le particelle hanno rilasciato circa un terzo della capsaicina. Questo comportamento “on–off” significa che il farmaco ha maggiori probabilità di essere rilasciato all’interno delle cellule tumorali piuttosto che lungo il tragitto, aumentando potenzialmente il beneficio riducendo gli effetti collaterali.
Come gli ingredienti delle particelle influenzano sicurezza e efficacia
Pur apparendo simili a prima vista, i due nanoveicoli differivano per il nucleo interno. Le particelle a base di zinco tendevano a essere più piccole e trattenevano la capsaicina in modo più forte, mentre quelle a base di manganese erano più porose e rilasciavano il farmaco più facilmente. Entrambi i tipi avevano una forte carica superficiale positiva, che favorisce l’interazione con le superfici negative di cellule e DNA. I test sul sangue umano hanno mostrato danni molto bassi ai globuli rossi, e le particelle vuote si sono rivelate delicate sulle cellule polmonari normali, a sostegno della loro sicurezza di base. Quando caricate con capsaicina, entrambi i sistemi sono diventati più potenti contro le cellule tumorali del fegato, ma la versione a base di manganese ha raggiunto il miglior equilibrio: ha danneggiato più intensamente le cellule tumorali restando relativamente meno dannosa per le cellule normali.
Oltre il cancro: effetti protettivi aggiuntivi
I nanoveicoli hanno fatto più che consegnare capsaicina. Hanno anche rallentato la crescita di diversi batteri patogeni in modo efficace quanto un antibiotico standard in alcuni test, e hanno aiutato a neutralizzare radicali liberi dannosi, collegati a infiammazione e danno tissutale. Misure spettrometriche attente hanno mostrato che, una volta che la capsaicina è stata imballata nelle particelle ferrite–chitosano, si è legata al DNA in modo più forte e più stabile. Esperimenti cinetici rapidi hanno rivelato una dinamica in due fasi: il DNA si lega prima alla superficie carica positivamente della particella, poi il complesso si riorganizza in un’associazione più stretta e duratura. Queste interazioni rafforzate spiegano probabilmente perché le particelle caricate mostrano effetti anticancerogeni, antibatterici e antiossidanti più forti rispetto alla capsaicina o alle particelle di ferrite da sole.
Cosa potrebbe significare per i pazienti
Per ora, questi risultati provengono da piastre di laboratorio, non da pazienti. Tuttavia suggeriscono che nanoveicoli accuratamente progettati possono trasformare un ingrediente alimentare piccante in un’arma oncologica più precisa. Scegliendo il giusto materiale del nucleo e il rivestimento, i ricercatori hanno creato pacchetti minuscoli che mantengono la capsaicina stabile, la trasportano in sicurezza nel sangue e la rilasciano preferenzialmente in condizioni simili a quelle tumorali, in particolare nelle cellule del cancro al fegato. Tra i design testati, le particelle a base di manganese hanno offerto la combinazione più promettente di uccisione mirata delle cellule tumorali, basso danno alle cellule normali e benefici antibatterici e antiossidanti aggiuntivi. Con ulteriori studi su animali e valutazioni di sicurezza, tali particelle “intelligenti” ispirate al peperoncino potrebbero un giorno contribuire a terapie più focalizzate e meno invasive per il cancro al fegato e potenzialmente altre malattie.
Citazione: Bakr, E., Elshami, F.I., Okba, E.A. et al. Stimuli-responsive chitosan-coated ferrite nanocarriers for targeted capsaicin delivery and core-dependent HepG2-selective bioactivity. Sci Rep 16, 8957 (2026). https://doi.org/10.1038/s41598-026-40433-6
Parole chiave: capsaicina, tumore del fegato, nanoparticelle, somministrazione mirata di farmaci, veicoli a risposta a stimoli