Clear Sky Science · it
MOV10, una nuova immunoterapia e biomarcatore prognostico, contribuisce allo sviluppo del glioma regolando l'autofagia
Perché questo studio sul cancro cerebrale è importante
Il glioblastoma, una forma aggressiva di cancro cerebrale, è notoriamente difficile da trattare. La maggior parte dei pazienti sopravvive solo pochi mesi dopo la diagnosi, nonostante interventi chirurgici, radioterapia e chemioterapia. Questo studio si concentra su una singola molecola chiamata MOV10 che risulta particolarmente attiva in questi tumori. Mostrando come MOV10 favorisca la crescita delle cellule tumorali, la loro fuga al sistema immunitario e la resistenza alla morte cellulare, i ricercatori identificano un nuovo possibile bersaglio per terapie più efficaci — e un potenziale marcatore prognostico per prevedere l’andamento clinico dei pazienti.
Un aiutante nascosto dei tumori cerebrali letali
Il gruppo ha iniziato analizzando grandi banche dati pubbliche sul cancro contenenti informazioni genetiche e cliniche di centinaia di persone con glioma, un gruppo ampio di tumori cerebrali che include il glioblastoma. Hanno scoperto che MOV10, una proteina coinvolta nella gestione degli RNA all’interno delle cellule, è espressa a livelli più elevati nei tessuti di glioma rispetto al cervello normale. I pazienti i cui tumori esprimevano più MOV10 tendevano a sopravvivere meno a lungo, e questa associazione rimaneva significativa anche tenendo conto di età, grado tumorale e caratteristiche genetiche chiave. Sfruttando questi fattori, i ricercatori hanno costruito un modello matematico che mostra come i livelli di MOV10 possano contribuire a prevedere le probabilità di sopravvivenza di un paziente, suggerendo che MOV10 potrebbe fungere da biomarcatore prognostico.
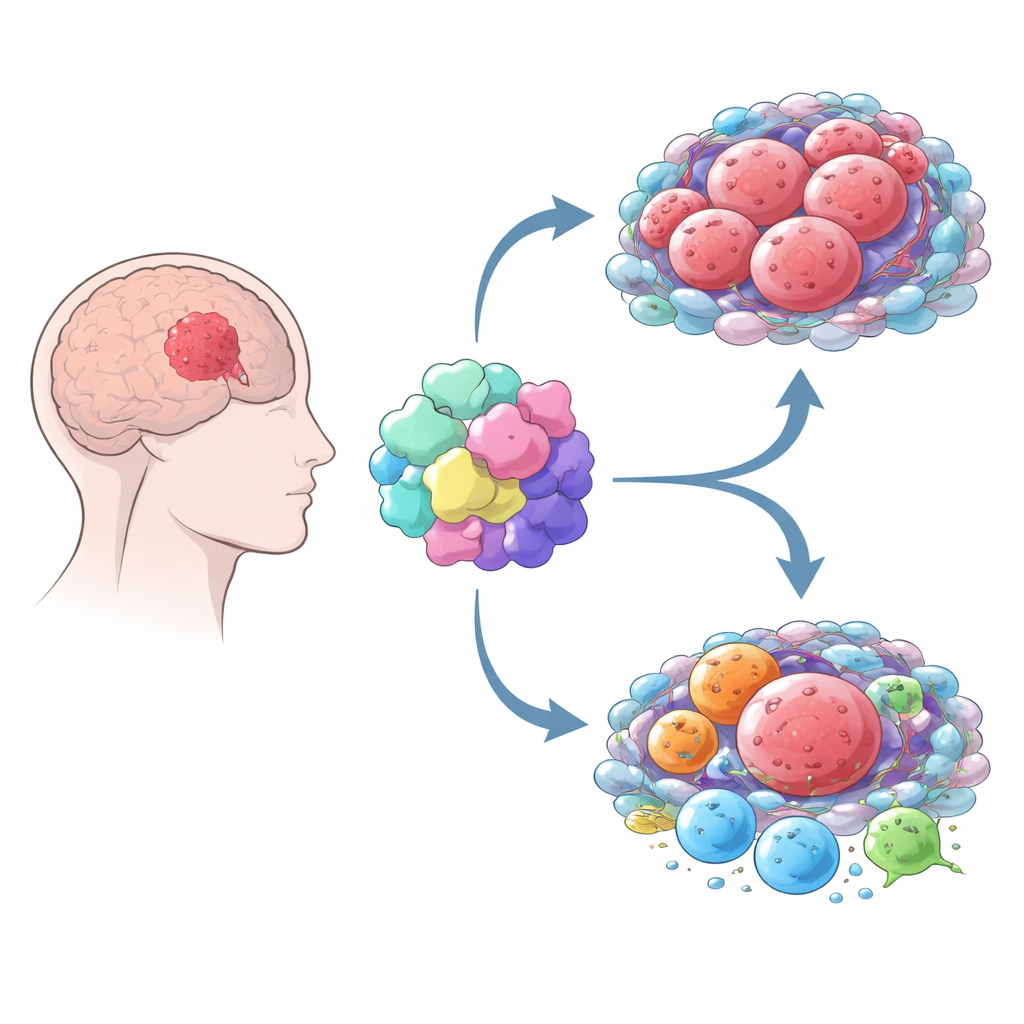
Come MOV10 rimodella il quartiere tumorale
Il cancro non cresce isolato: sfrutta il “quartiere” circostante fatto di cellule immunitarie e di supporto. Combinando diversi strumenti computazionali, gli autori hanno mostrato che i gliomi con alti livelli di MOV10 sono circondati da una miscela più ricca di cellule immunitarie e stromali rispetto ai tumori con bassi livelli di MOV10. Ma non si tratta di un attacco immunitario efficace. Al contrario, i tumori con MOV10 elevato contengono più macrofagi, in particolare un sottotipo spesso definito M2, che tipicamente sostiene la crescita tumorale e attenua le risposte immunitarie. Questi tumori mostrano inoltre firme più marcate di cellule T esaurite e maggiore attività di “freni” immunitari che sono bersagli di farmaci immunoterapici popolari, come PD-1 e CTLA-4. Nel complesso, il quadro suggerisce che MOV10 sia associato a un ambiente immunosoppressivo in cui le difese dell’organismo risultano indebolite.
Dai big data alle cellule in laboratorio
Per andare oltre le correlazioni, i ricercatori hanno analizzato MOV10 direttamente in campioni di pazienti e in cellule coltivate. Hanno confermato che MOV10 è più abbondante nei tessuti di glioma rispetto al cervello normale e che diverse linee cellulari di glioma ampiamente usate mostrano anch’esse livelli elevati. Quando hanno usato piccoli RNA interferenti per ridurre MOV10 nelle cellule di glioma coltivate in piastre, le cellule si dividevano più lentamente, formavano meno colonie e perdevano parte della loro capacità di muoversi e invadere membrane artificiali. Proteine che guidano la progressione del ciclo cellulare e l’invasione sono diminuite in abbondanza, a sostegno dell’idea che MOV10 promuova attivamente comportamenti aggressivi piuttosto che essere un semplice spettatore.
Collegare MOV10 alle cellule immunitarie e ai percorsi di “autopulizia”
Lo studio ha inoltre indagato come MOV10 interagisca con due processi chiave: il comportamento dei macrofagi associati al tumore e il sistema di “autopulizia” cellulare noto come autofagia. Nei campioni tumorali umani, MOV10 è stato trovato nelle stesse aree dei macrofagi di tipo M2. In un sistema di co-coltura, quando le cellule di glioma sono state ingegnerizzate per produrre meno MOV10, meno macrofagi di tipo M2 migravano attraverso una barriera verso di esse, implicando che MOV10 nelle cellule tumorali aiuta ad attirare o sostenere queste cellule immunitarie pro-tumorali. Allo stesso tempo, analisi genetiche hanno collegato MOV10 a diversi geni coinvolti nell’autofagia. Utilizzando marcatori fluorescenti che evidenziano le strutture di riciclo cellulare, il gruppo ha mostrato che ridurre MOV10 aumentava l’attività autofagica nelle cellule di glioma e innescava una maggiore morte cellulare programmata. Variazioni nelle proteine caratteristiche dell’autofagia e dell’apoptosi confermavano queste osservazioni.
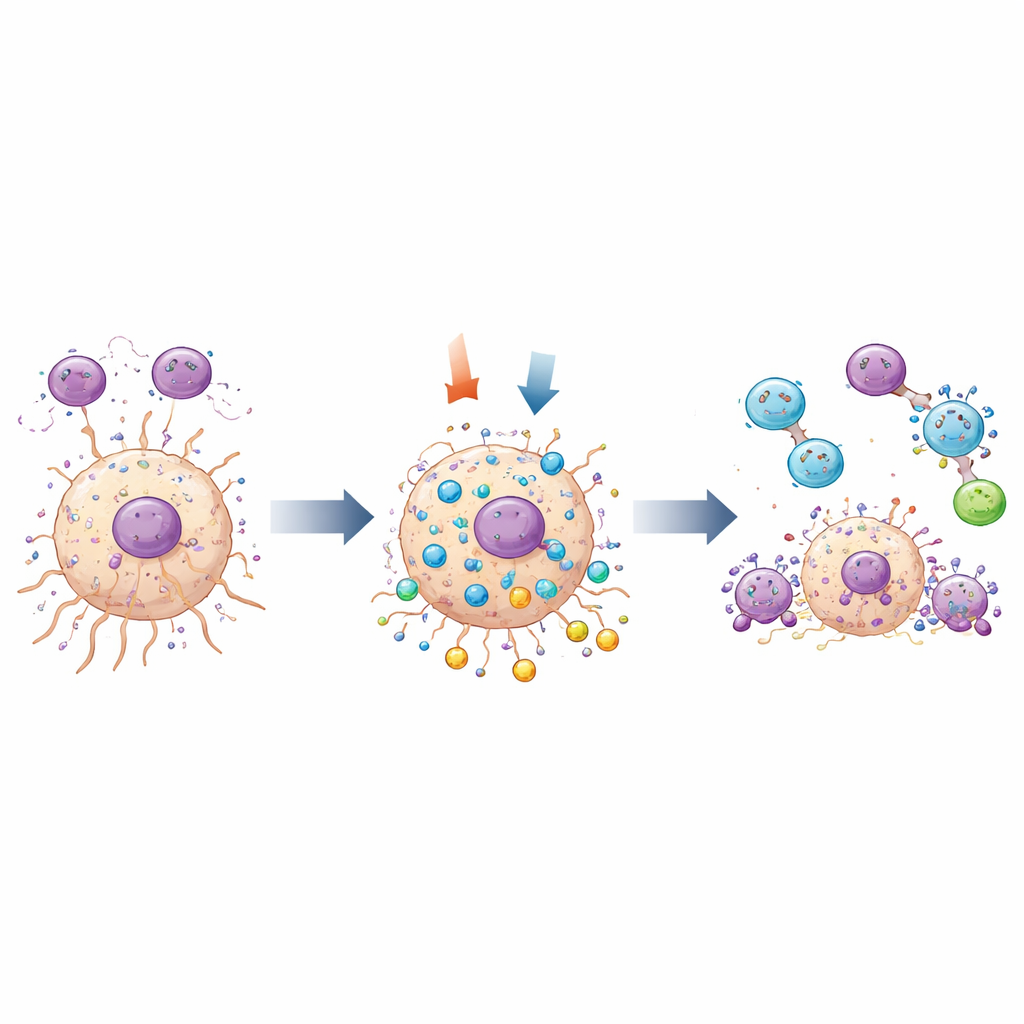
Cosa significa per i trattamenti futuri
Nel complesso, i risultati dipingono MOV10 come un alleato multifunzionale del glioma: favorisce la crescita e l’invasione delle cellule tumorali, contribuisce a creare un microambiente immunosoppressivo ricco di macrofagi che supportano il tumore e mantiene sotto controllo i sistemi di autocancellazione e riciclo della cellula. Quando MOV10 viene silenziato, le cellule di glioma crescono meno, muoiono più facilmente e sembrano meno capaci di reclutare tipi di cellule immunitarie dannose. Per i non specialisti, il messaggio chiave è che MOV10 è sia un “termometro” sia un “interruttore”: il suo livello nei tumori può aiutare a prevedere l’esito dei pazienti e ridurlo potrebbe, in linea di principio, rendere i tumori cerebrali più vulnerabili ai trattamenti. Sebbene siano necessari ulteriori studi su modelli animali e successivi trial clinici, MOV10 emerge ora come un promettente bersaglio nella ricerca di terapie migliori contro uno dei tumori cerebrali più letali.
Citazione: Wang, F., Ruan, L., Yang, W. et al. MOV10, a novel immunotherapy and prognostic biomarker, contributes to glioma development by regulating autophagy. Sci Rep 16, 9501 (2026). https://doi.org/10.1038/s41598-026-40396-8
Parole chiave: glioblastoma, immunoterapia per i tumori cerebrali, proteina MOV10, microambiente tumorale, autofagia e apoptosi