Clear Sky Science · it
Splicing alternativo ed espressione genica differenziale durante i cambiamenti della recettività endometriale in pazienti con fallimento ricorrente d’impianto
Perché alcuni embrioni non si impiantano
Molte coppie che ricorrono alla fecondazione in vitro si trovano davanti a un enigma frustrante: anche quando vengono trasferiti embrioni di alta qualità, la gravidanza può comunque non instaurarsi. Questo studio esamina da vicino il rivestimento dell’utero — l’endometrio — per comprendere perché alcune donne sperimentano ripetuti fallimenti d’impianto. Analizzando come i geni vengono attivati o disattivati, come i loro messaggi vengono tagliati e riorganizzati e come si comportano le cellule immunitarie durante la breve finestra in cui l’utero è pronto ad accogliere un embrione, la ricerca mette in luce nuovi indizi molecolari che un giorno potrebbero guidare test e trattamenti più mirati.
La breve finestra di accoglienza dell’utero
L’impianto può avvenire solo durante un periodo limitato di ogni ciclo, quando il rivestimento uterino diventa «recettivo». I ricercatori hanno confrontato campioni di tessuto provenienti da 90 donne fertili e 73 donne con fallimento ricorrente d’impianto, tutti raccolti in tre momenti chiave: poco prima che il rivestimento diventasse recettivo, durante la finestra recettiva e poco dopo la sua chiusura. Utilizzando il sequenziamento dell’RNA ad alta resa, hanno misurato quali geni erano attivi e come i loro messaggi di RNA venivano elaborati. Questo disegno sperimentale ha permesso di seguire come un endometrio sano si prepara per un embrione e come questa preparazione deragli in donne che ripetutamente non riescono a impiantare nonostante la presenza di embrioni di buona qualità. 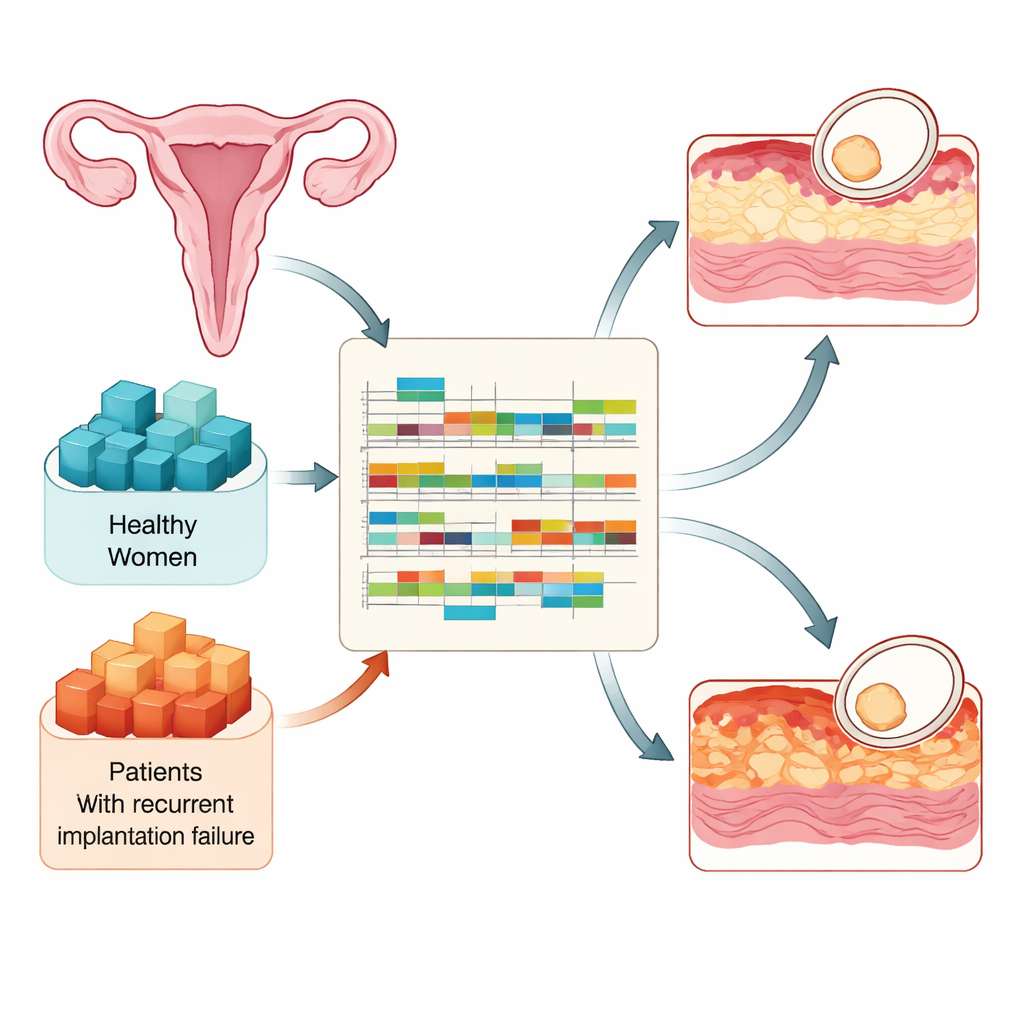
I messaggi genici tagliati e riorganizzati
Oltre a contare quanto è attivo ciascun gene, il gruppo si è concentrato sullo splicing alternativo — il processo mediante il quale un singolo gene può essere tagliato in varianti di messaggi differenti, portando a forme proteiche distinte. Hanno rilevato oltre un milione di eventi di splicing nei confronti effettuati, con due tipi — l’esclusione di interi segmenti e la scelta tra segmenti mutuamente esclusivi — particolarmente comuni. Limitandosi ai cambiamenti sia frequenti sia statisticamente robusti, hanno osservato da centinaia a migliaia di spostamenti nello splicing mentre il rivestimento passava dalla fase non recettiva a quella recettiva, in particolare dalla fase precoce (pre‑recettiva) fino alla finestra di impianto. Molti di questi cambiamenti si sono verificati anche quando la quantità complessiva del gene restava invariata, il che significa che la forma della proteina variava senza un cambiamento nell’attività genica totale.
Cellule che aderiscono, si rimodellano e comunicano con il sistema immunitario
I geni interessati dallo splicing alterato e dai cambiamenti di attività erano fortemente coinvolti nei meccanismi con cui le cellule aderiscono tra loro, come viene riorganizzato lo scheletro cellulare e come inviano e ricevono segnali immunitari. Queste funzioni sono cruciali mentre l’endometrio si trasforma da una barriera semplice a una superficie in grado di accogliere e ancorare un embrione, rimodellando anche i vasi sanguigni. Sia nelle donne fertili sia in quelle con fallimento d’impianto, la fase recettiva è stata caratterizzata da un intenso rimodellamento di queste vie, ma le donne con fallimenti ricorrenti tendono a mostrare cambiamenti nello splicing più frequenti o con schemi diversi. Alcuni dei geni coinvolti sono già stati proposti come marcatori della finestra di impianto ideale, rafforzando l’idea che non sia solo l’attività genica, ma la forma esatta dei loro prodotti, a definire quando il rivestimento è davvero pronto.
Cellule immunitarie e un regolatore chiave dello splicing
Il gruppo ha anche stimato i tipi di cellule immunitarie presenti nel tessuto usando gli stessi dati di RNA. Nelle donne con fallimento d’impianto, la fase recettiva mostrava meno linfociti T citotossici e meno cellule natural killer in stato di riposo, ma più monociti e alcuni sottotipi di macrofagi rispetto alle fasi precedenti. Successivamente, dopo la chiusura della finestra, i profili mutavano nuovamente, con variazioni nelle natural killer attivate e nei sottotipi di macrofagi. Diversi di questi cambiamenti nelle cellule immunitarie seguivano da vicino specifici eventi di splicing, suggerendo che il rimodellamento dei messaggi genici e l’equilibrio immunitario siano collegati. Tra le proteine che controllano lo splicing, una chiamata KHDRBS3 è emersa come un nodo centrale connesso a molti degli eventi alterati e si è costantemente ridotta di livello quando il rivestimento diventava recettivo, sia nelle donne fertili sia in quelle affette. Ciò suggerisce che possa contribuire a guidare il cambiamento nei modelli di splicing che accompagna l’apertura della finestra di impianto. 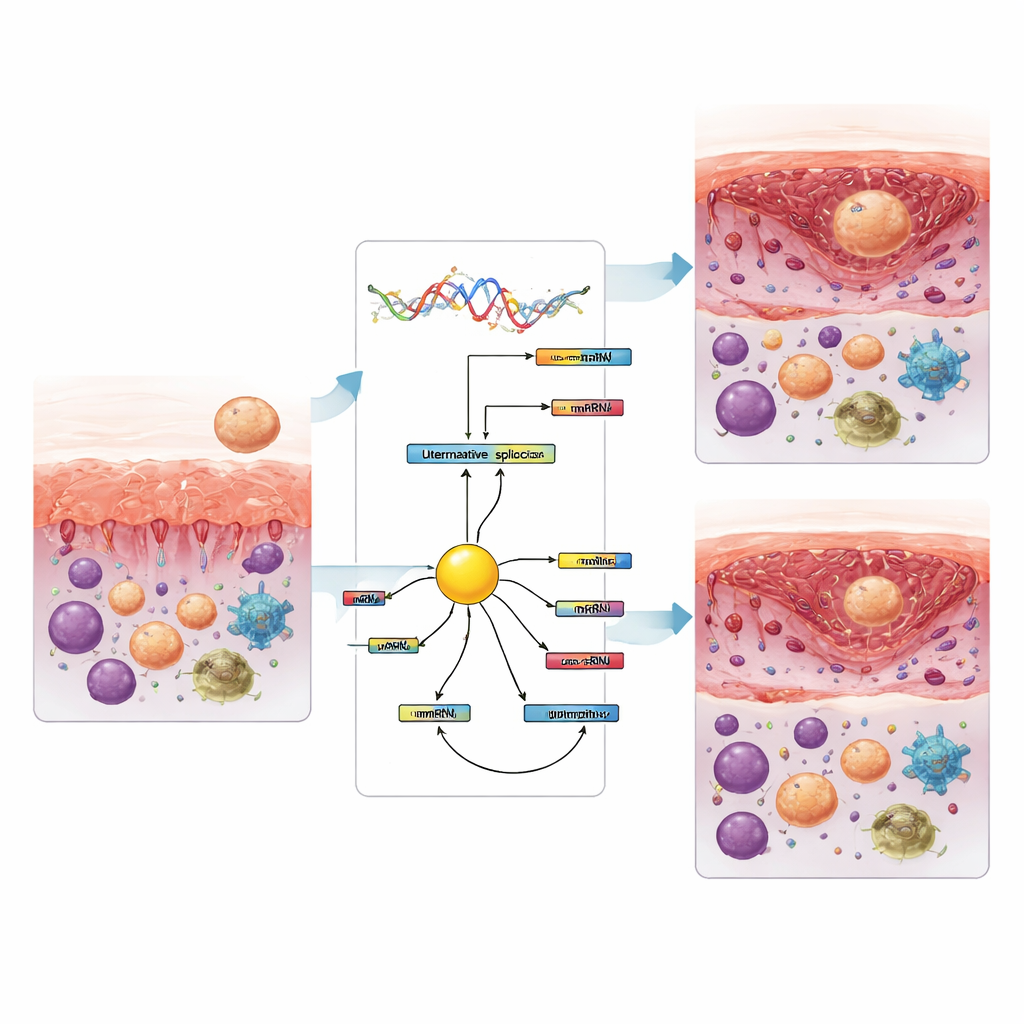
Indicazioni per futuri test e trattamenti
Per tradurre questi schemi molecolari in possibili terapie, i ricercatori hanno chiesto se farmaci a piccola molecola già esistenti potessero controbilanciare le firme di splicing anomale osservate. Incrociando le loro liste di geni con ampi database di risposta ai farmaci, hanno identificato diversi composti approvati o sperimentali che prendono di mira geni collegati all’impianto, inclusi agenti che influenzano le risposte immunitarie o le vie ormonali. Pur essendo ancora lontani dall’essere pronti per l’uso clinico in questo contesto, offrono una mappa iniziale per i test di laboratorio.
Cosa significa per le pazienti
Nel complesso, lo studio mostra che il fallimento d’impianto non è semplicemente una questione di avere i «geni sbagliati», ma di come quei geni vengono editati in messaggi diversi e di come l’ambiente immunitario dell’utero si regoli nel tempo. Il lavoro mette in evidenza KHDRBS3 e fattori correlati come regolatori promettenti di questo processo e rivela spostamenti coordinati nelle cellule immunitarie che possono favorire o ostacolare il tentativo di un embrione di stabilirsi. A lungo termine, tali intuizioni potrebbero portare a test più raffinati per determinare il vero timing e la qualità della finestra recettiva di una donna, così come a trattamenti mirati che modulino delicatamente il messaggio genico o l’equilibrio immunitario per offrire agli embrioni maggiori possibilità di impianto.
Citazione: Wang, Ml., Lu, Bj., Lu, X. et al. Alternative splicing and differential gene expression during changes in endometrial receptivity in patients with recurrent implantation failure. Sci Rep 16, 9754 (2026). https://doi.org/10.1038/s41598-026-40386-w
Parole chiave: recettività endometriale, fallimento ricorrente d’impianto, splicing alternativo, cellule immunitarie uterine, fecondazione assistita