Clear Sky Science · it
Selezione adattativa di esempi per il rilevamento spiegabile di mitosi basato su prototipi in patologia digitale
Perché è importante per la cura del cancro
Quando i patologi esaminano campioni tumorali al microscopio, contare quante cellule tumorali sono in divisione attiva aiuta a stabilire quanto è aggressivo un tumore e quali trattamenti siano più appropriati. L’intelligenza artificiale può ora individuare rapidamente queste cellule in vetrini digitali, ma le sue decisioni spesso restano un mistero anche per gli esperti. Questo articolo introduce un metodo chiamato Selezione Adattativa di Esempi (AES) che permette a un sistema di IA di “mostrare il proprio ragionamento” indicando casi reali passati che supportano o contraddicono ogni decisione, rendendo il rilevamento automatico delle mitosi più trasparente e clinicamente affidabile.
La sfida di individuare le cellule in divisione
Le cellule tumorali in divisione, note come figure mitotiche, sono piccole, rare e visivamente molto variabili. Con la comune colorazione ematossilina-eosina possono assomigliare a strutture innocue come cellule in necrosi o certi tipi di cellule immunitarie. Gli esperti devono scorrere enormi vetrini digitali per trovarle, un processo lento, faticoso e soggetto a disaccordi. I moderni sistemi di deep learning possono eguagliare o superare le prestazioni degli esperti in questo compito, ma si comportano come scatole nere: forniscono un punteggio per ogni cellula sospetta senza spiegare chiaramente il perché. In medicina, dove le decisioni di trattamento possono cambiare la vita, questa mancanza di chiarezza è un serio ostacolo all’adozione clinica dell’IA.
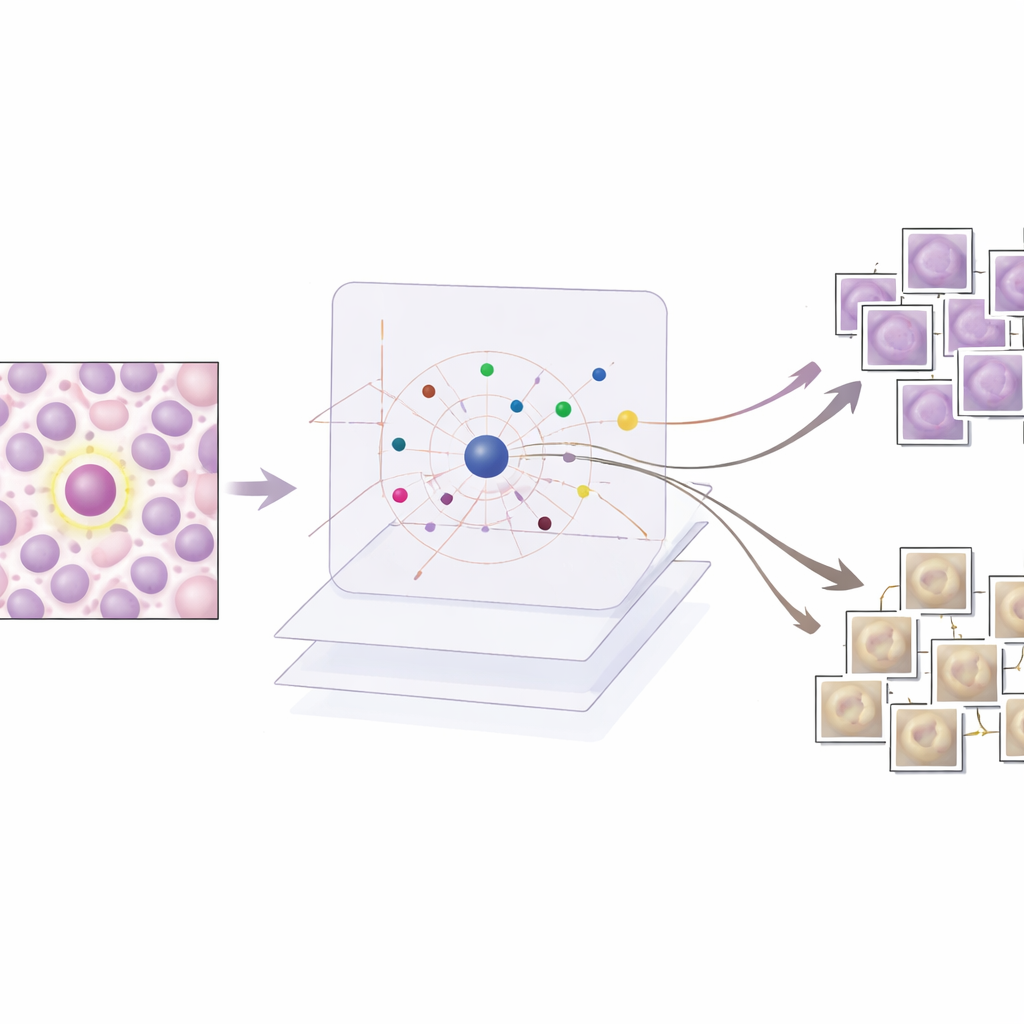
Costruire un rilevatore potente ma opaco
Gli autori addestrano innanzitutto una rete di rilevamento oggetti all’avanguardia, basata sull’architettura Faster R-CNN, per trovare le figure mitotiche in un ampio e vario dataset chiamato MIDOG++. Queste immagini provengono sia da tumori umani sia canini, coprendo diversi tipi di cancro e laboratori, e includono più di undicimila cellule in divisione accuratamente annotate. Per preservare i dettagli fini, le vetrine vengono suddivise in piccoli patch e fortemente aumentate per riprodurre le variazioni reali nella colorazione e nell’acquisizione. Il rilevatore risultante ottiene prestazioni solide attraverso i tipi di tumore, con punteggi F1 fino a 0,84, confermando che è accurato ma complesso—esattamente il tipo di sistema che richiede spiegazioni migliori prima che i clinici possano fidarsene in pratica.
Insegnare all’IA a spiegarsi con esempi
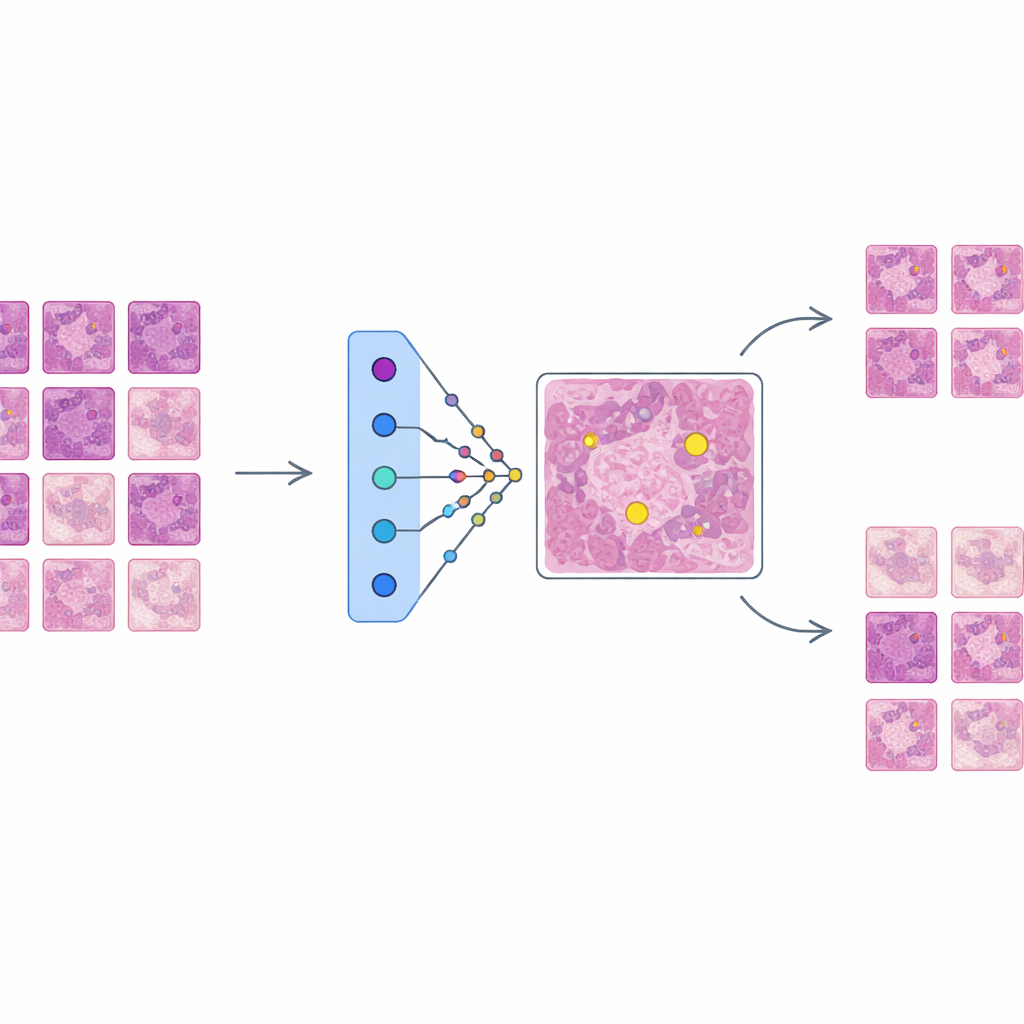
AES si pone sopra questo rilevatore addestrato come uno strato di interpretabilità, senza modificare il funzionamento interno del rilevatore. Per ogni regione candidata che il rilevatore indica come potenzialmente mitotica, AES esplora una libreria di patch tissutali reali tratte dai dati di addestramento. Da questa libreria seleziona un piccolo insieme di esempi “di supporto” che assomigliano a vere mitosi e un insieme di esempi “contraddittori” che richiamano più da vicino cellule non mitotiche. Dietro le quinte, AES tratta i punteggi di confidenza del rilevatore come un paesaggio continuo e usa uno strumento matematico chiamato funzione a base radiale per approssimare come quella confidenza cambia nelle vicinanze di ogni caso. Vengono mantenuti solo i prototipi che influenzano in modo significativo la confidenza locale, così la spiegazione di una singola decisione coinvolge tipicamente una decina circa di esempi accuratamente scelti invece di centinaia di elementi poco rilevanti.
Cosa rivelano gli esempi sulle decisioni dell’IA
I ricercatori valutano AES sia quantitativamente sia qualitativamente. Dal punto di vista numerico, mostrano che un dizionario compatto di circa 190 immagini prototipiche può imitare i punteggi di confidenza del rilevatore con altissima accuratezza, mantenendo il numero di esempi mostrati per caso sufficientemente basso da poter essere esaminato da un umano. Dal punto di vista qualitativo, esaminano tre scenari comuni. Quando il rilevatore è chiaramente corretto, AES restituisce solo prototipi mitotici che supportano fortemente la decisione, rassicurando i clinici. Per i falsi positivi, il metodo mette in luce prototipi mitotici somiglianti che spiegano perché il rilevatore è stato fuorviato da texture o pattern cromatinici simili, spesso insieme a prototipi non mitotici più deboli che suggeriscono incertezza. Per le mitosi non rilevate, AES tende a restituire principalmente prototipi non mitotici o esempi ambigui, evidenziando punti ciechi nei dati di addestramento e suggerendo dove sono necessari nuovi esempi o annotazioni migliori.
Dalla scatola nera a uno strumento collaborativo
Ancorando ogni previsione a una manciata di patch tissutali reali e annotate, AES fa sì che un rilevatore complesso si comporti più come un collega umano che giustifica le decisioni richiamando casi passati. Il sistema non si limita a indicare se una cellula è probabilmente in divisione, ma mostra anche il perché e quanto ne sia sicuro, attraverso la combinazione e l’influenza dei prototipi di supporto e di contraddizione. Questo design permette ai patologi di confermare rapidamente previsioni forti, concentrare l’attenzione su regioni borderline o confuse e identificare pattern di errore sistematici che possono guidare ulteriore addestramento. Pur essendo stato sviluppato per il rilevamento delle mitosi, lo stesso approccio potrebbe essere esteso ad altri compiti in patologia digitale, aiutando a trasformare l’IA da automazione opaca a un assistente interpretabile basato sui casi, che i clinici possono interrogare, fidarsi e perfezionare.
Citazione: Banik, M., Kreutz-Delgado, K., Mohanty, I. et al. Adaptive example selection for prototype based explainable mitosis detection in digital pathology. Sci Rep 16, 9481 (2026). https://doi.org/10.1038/s41598-026-40283-2
Parole chiave: IA spiegabile, patologia digitale, rilevamento delle mitosi, modelli basati su prototipi, diagnostica del cancro