Clear Sky Science · it
Fonte pulsata ultra-intensa di radiazione ionizzante basata sull’accelerazione diretta di elettroni da laser per studiare l’effetto FLASH
Perché i lampi di radiazione ultraveloci sono importanti
La radioterapia oncologica è un esercizio di equilibrio: erogare abbastanza radiazione per eliminare i tumori senza danneggiare in modo duraturo i tessuti sani. Un’idea recente e promettente, chiamata effetto FLASH, suggerisce che somministrare la dose in un singolo impulso ultracorto e ultraintenso possa risparmiare il tessuto normale pur colpendo il cancro. Questo studio presenta un nuovo tipo di sorgente sperimentale basata su un potente laser che genera impulsi estremamente brevi di elettroni ad alta energia, e la usa per osservare come l’ossigeno in acqua e in liquidi biologici venga rapidamente consumato durante l’irradiazione — un processo ritenuto centrale per l’effetto FLASH. 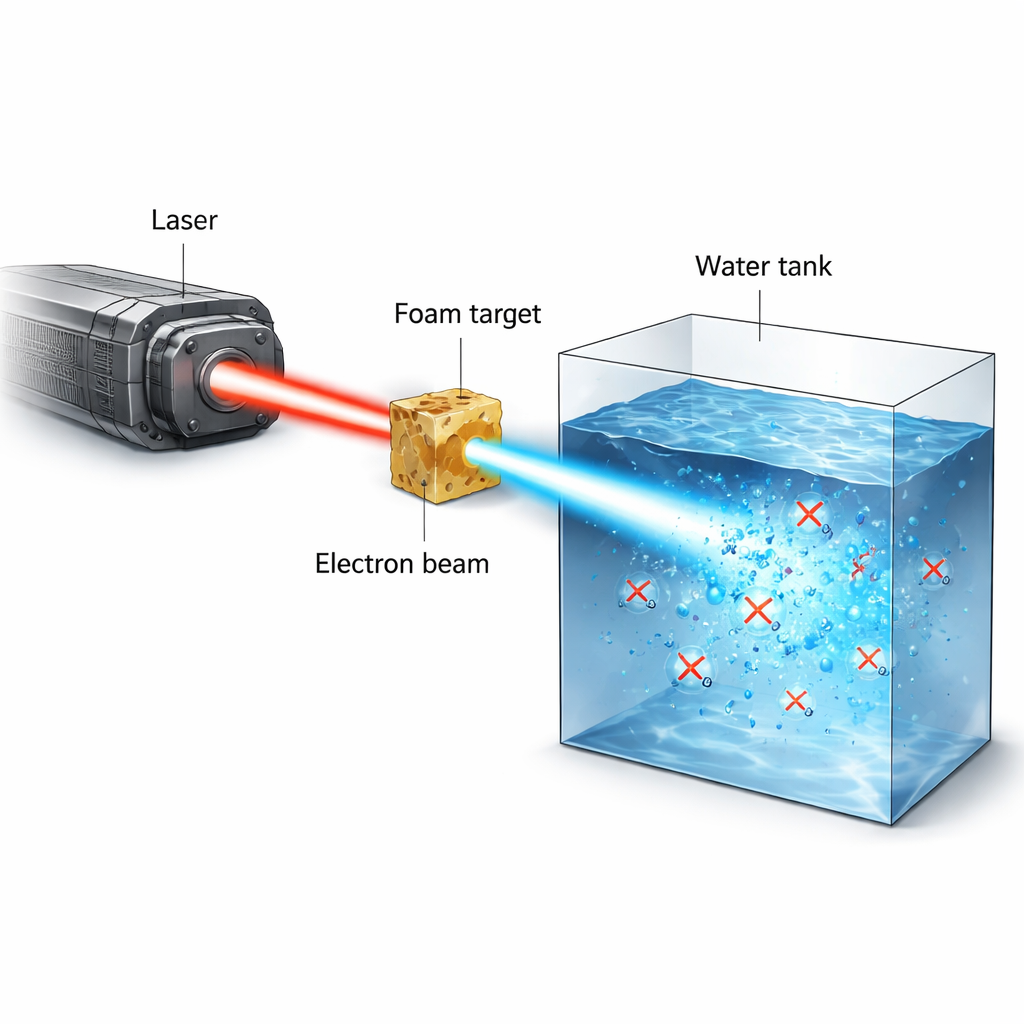
Dai macchinari ospedalieri ai fasci guidati dal laser
La radioterapia convenzionale impiega raggi X, elettroni o protoni prodotti da grandi acceleratori. Queste macchine tipicamente erogano la dose su tempi che vanno dai millisecondi ai secondi e, pur essendo molto precise, danneggiano comunque i tessuti sani perché la radiazione rompe indirettamente il DNA scindendo le molecole d’acqua e generando specie reattive dell’ossigeno. La presenza di ossigeno nei tessuti sani ben vascolarizzati peggiora questo danno — il cosiddetto effetto ossigeno. La radioterapia FLASH mira a invertire questo meccanismo erogando l’intera dose terapeutica in una frazione di secondo a tassi di dose ultra-alti, il che sembra proteggere temporaneamente i tessuti normali negli studi animali senza proteggere i tumori. Tuttavia, gli acceleratori medici standard faticano a raggiungere questi tassi di dose estremi, il che motiva la ricerca di sorgenti alternative come i laser ad alta potenza.
Trasformare schiuma e luce in un potente impulso di elettroni
I ricercatori hanno usato il laser ad alta potenza PHELIX per generare fasci stretti ad alta corrente di elettroni con energie di diversi milioni di elettronvolt (MeV). Il laser ionizza inizialmente una schiuma polimerica a bassa densità trasformandola in un plasma vicino alla densità critica. In un secondo impulso ultracorto, della durata inferiore a un trilionesimo di secondo, il laser spinge e intrappola gli elettroni all’interno di un canale di plasma, accelerandoli direttamente a energie elevate. Questo processo, chiamato accelerazione laser diretta, produce un fascio strettamente collimato che può trasportare decine di nanocoulomb di carica in un impulso della scala del picosecondo. Quando questo fascio colpisce acqua o materiale simile all’acqua, può depositare 20–50 gray di dose in un singolo colpo, a tassi di dose istantanei superiori a 10^13 gray al secondo — molto al di là di quanto possono ottenere le macchine convenzionali.
Osservare l’ossigeno scomparire in un lampo
Per sondare come impulsi così intensi influenzino la chimica in condizioni simili a tessuti biologici, il team ha costruito serbatoi d’acqua sigillati che potevano operare in vuoto e essere riempiti con acqua pura, terreno di coltura cellulare o cellule lisate, tutti completamente ossigenati in precedenza. Il fascio di elettroni è stato modellato e filtrato in modo che gli elettroni ad alta energia dominassero la dose all’interno del serbatoio, mentre protoni e raggi X sono stati in gran parte soppressi o contabilizzati con cura mediante strati di schermatura e film radiochromici. Un sensore ottico posto sulla parete interna del serbatoio monitorava l’ossigeno disciolto misurando come le molecole di ossigeno quenchassero la luminescenza di una macchia di colorante. Dopo ogni singola irradiazione a impulso, il sensore ha registrato un calo improvviso della concentrazione di ossigeno che poi si rilassava lentamente man mano che l’ossigeno diffondeva nella regione del sensore. Combinando i dati dei film, le simulazioni e la nota potenza di arresto degli elettroni, gli autori hanno ricostruito la dose erogata al volume irradiato e l’hanno collegata direttamente alla perdita di ossigeno misurata. 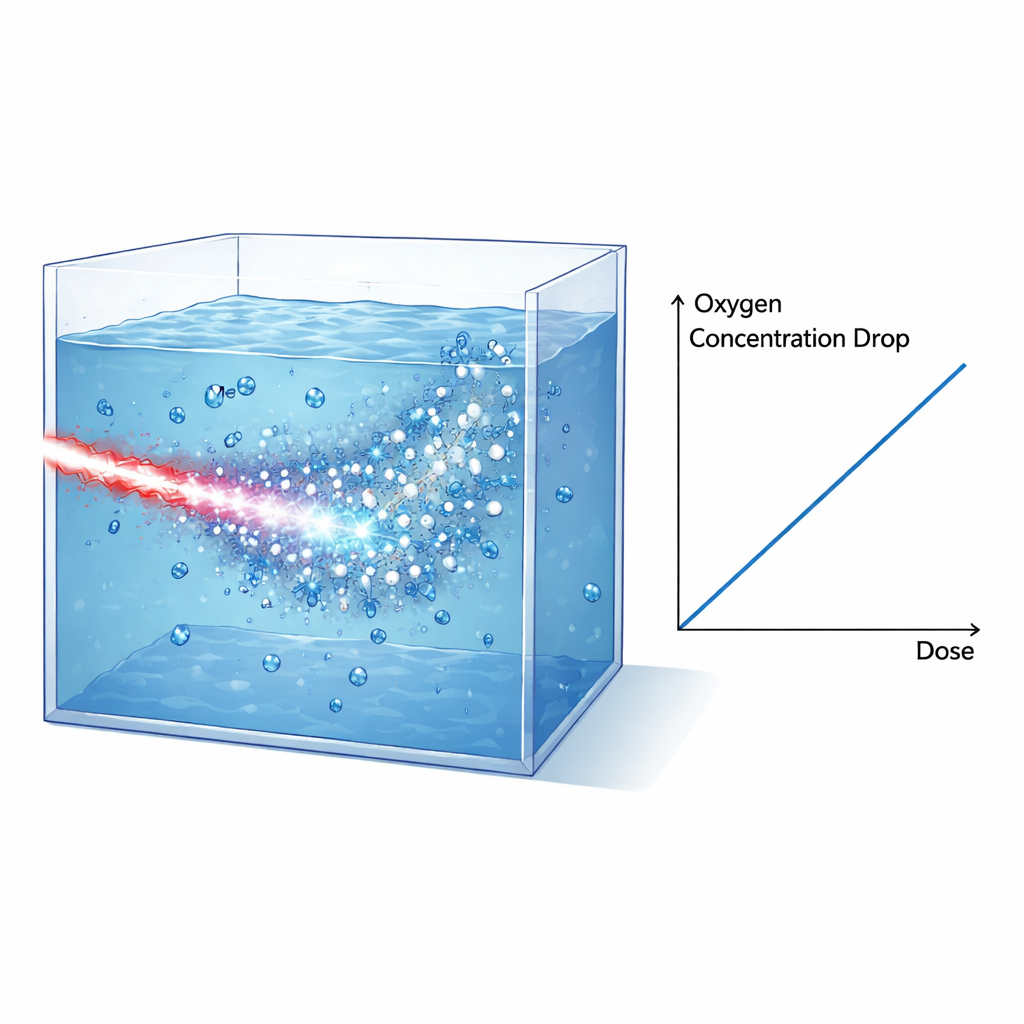
Collegare esperimento e teoria
La scoperta chiave è che la diminuzione dell’ossigeno disciolto è proporzionale alla dose erogata sia per l’acqua sia per il terreno di coltura, con pendenze molto simili. Dopo aver corretto per una piccola dose aggiuntiva dovuta ai raggi X, il consumo misurato di ossigeno in acqua è di circa 0,32 micromoli per litro per gray. Questo valore concorda sorprendentemente bene con le previsioni di dettagliate simulazioni Monte Carlo della struttura delle tracce (TRAX-CHEM), che seguono i percorsi degli elettroni nell’acqua e modellano la chimica rapida che si sviluppa nei microsecondi successivi all’irradiazione. Crucialmente, in questo schema guidato dal laser quasi l’intera dose viene erogata nell’ordine di un picosecondo — molto più breve dei tempi caratteristici delle reazioni chimiche successive. Ciò significa che l’esperimento riproduce da vicino le condizioni ideali assunte in queste simulazioni, fornendo un test rigoroso dei modelli sottostanti.
Costruire un banco di prova migliore per la scienza FLASH
Oltre a validare la teoria, gli autori usano i loro risultati per progettare una disposizione sperimentale migliorata. Semplificando la geometria, eliminando i magneti e posizionando simmetricamente acqua e film misuratori di dose attorno al fascio, i futuri allestimenti potrebbero misurare direttamente la dose all’interno del serbatoio senza ricostruzioni complesse, sopprimendo ulteriormente i contributi indesiderati di protoni e raggi X. Le simulazioni mostrano che modificando il bersaglio — ad esempio aggiungendo sottili strati di plastica o oro — si può regolare la dose per colpo tra circa 40 e 80 gray, offrendo una piattaforma flessibile per esplorare un’ampia gamma di condizioni rilevanti per FLASH.
Cosa significa per i futuri trattamenti oncologici
Per i non specialisti, il messaggio centrale è che questa sorgente basata su laser crea impulsi di elettroni estremamente intensi e ultrabrevi che imitano — e in alcuni aspetti superano — le condizioni immaginate per la radioterapia FLASH. Lo studio mostra che questi impulsi consumano rapidamente l’ossigeno disciolto in acqua e mezzi biologici in modo coerente con previsioni teoriche avanzate. Poiché la deplezione di ossigeno e la chimica radicalica correlata sono tra i principali candidati a spiegare perché FLASH potrebbe risparmiare i tessuti sani, disporre di una sorgente controllabile e ben caratterizzata come questa rappresenta un passo avanti significativo. Fornisce un potente banco di prova per affinare i modelli e, in ultima analisi, per guidare la progettazione di futuri macchinari clinici che potrebbero trattare il cancro in modo più efficace riducendo gli effetti collaterali.
Citazione: Gyrdymov, M., Bukharskii, N., Fabian, V. et al. Ultra-intense pulsed source of ionizing radiation based on direct laser acceleration of electrons for studying the FLASH effect. Sci Rep 16, 7164 (2026). https://doi.org/10.1038/s41598-026-40281-4
Parole chiave: Radioterapia FLASH, elettroni accelerati da laser, tasso di dose ultra-alto, deplezione di ossigeno, radiolisi dell’acqua