Clear Sky Science · it
Una pipeline automatizzata di analisi delle immagini per l’imaging redox ottico a campo largo di organoidi tumorali derivati da pazienti
Perché questo studio sull’imaging del cancro è importante
Trovare il farmaco giusto per il tumore di ciascuna persona è ancora un processo lento e spesso casuale. Questo studio affronta il problema combinando minitumori coltivati in laboratorio a partire da pazienti — chiamati organoidi — con un metodo rapido basato su telecamere per osservare come cambia il loro utilizzo energetico quando vengono somministrati i farmaci. Gli autori mostrano come una nuova pipeline informatica automatizzata possa setacciare grandi pile di immagini al microscopio, tracciare centinaia di organoidi per diversi giorni e rivelare quali trattamenti funzionano, il tutto molto più velocemente e in modo più affidabile di quanto un operatore umano potrebbe fare manualmente.
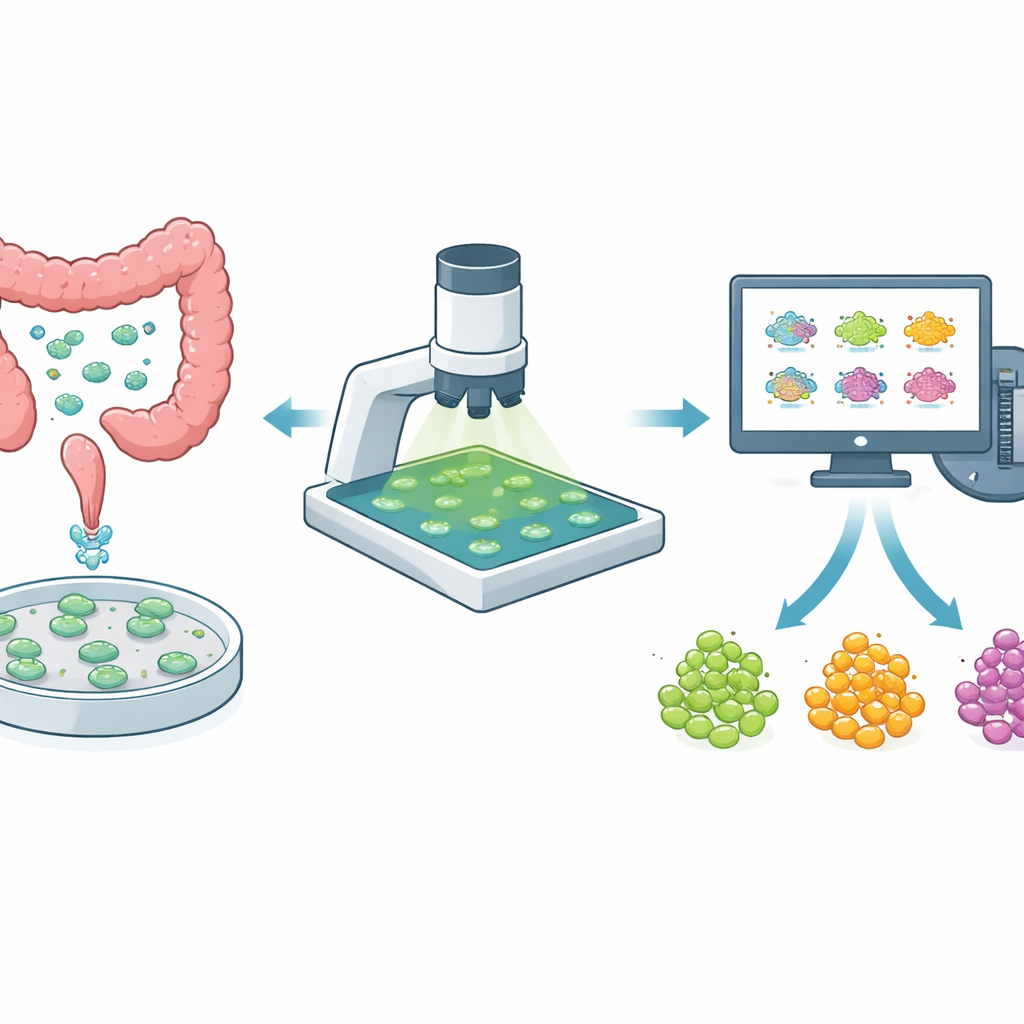
Mini-tumori in una piastra come banchi di prova
Invece di basarsi solo su cellule tumorali cresciute in strati piatti, i ricercatori usano sempre più spesso organoidi tridimensionali ottenuti direttamente dal tumore di un paziente. Questi minitumori conservano meglio la miscela di tipi cellulari e le nicchie di cellule resistenti ai farmaci che esistono nell’organismo. Nel cancro colorettale, dove i tumori variano molto tra persone diverse e perfino all’interno dello stesso paziente, gli organoidi sono un modo potente per testare l’efficacia di farmaci nuovi e già esistenti. Ma per essere utili nel guidare il trattamento, i test sugli organoidi devono essere delicati — in modo che lo stesso organoide possa essere osservato nel tempo — e abbastanza rapidi da permettere lo screening di molti farmaci e dosaggi.
Osservare l’“uso del combustibile” del tumore con la luce
Il gruppo utilizza una tecnica chiamata imaging redox ottico, che si basa sul debole bagliore naturale di molecole intracellulari coinvolte nella produzione di energia. Illuminando con colori specifici e raccogliendo la fluorescenza emessa, un semplice microscopio a campo largo può catturare una mappa di quanto ogni organoide sia “ossidato” o “ridotto” — un’istantanea del suo stato metabolico. Diversamente da microscopi più complessi e costosi, questa configurazione impiega componenti standard che molti laboratori possiedono già, rendendola relativamente semplice da adottare. Le variazioni in questo segnale redox spesso compaiono prima dei cambiamenti nelle dimensioni dell’organoide o della morte cellulare, diventando un segnale precoce utile per capire se un farmaco sta funzionando o no.
Trasformare immagini grezze in numeri affidabili
Finora, analizzare queste immagini significava che una persona doveva tracciare i contorni di ogni organoide, scegliere a occhio le regioni di sfondo e poi cercare di seguire quale organoide fosse quale nel corso di diversi giorni. Questo approccio lento e soggetto a errori non è adatto per ampi screening farmacologici. Gli autori hanno creato una pipeline automatizzata end-to-end che svolge tre compiti difficili: separare con precisione ogni organoide dall’ambiente circostante, assegnare a ciascuno un’identità coerente su più giorni e stimare il segnale di fondo in modo da evitare bias umani. Hanno perfezionato uno strumento di intelligenza artificiale esistente (Cellpose) per riconoscere gli organoidi anche quando variano nella forma, dimensione e fuoco, quindi hanno costruito un algoritmo di tracking che allinea immagini prese in giorni diversi e abbina gli organoidi in base alla sovrapposizione di forma e posizione.
Ingrandire il margine più attivo
Gli organoidi presentano zone distinte: un nucleo morto o in necrosi, una regione centrale più quieta e un bordo esterno vivo dove le cellule crescono attivamente e spesso sono più sensibili al trattamento. La pipeline ritaglia automaticamente questo sottile anello esterno — chiamato leading edge — per ogni organoide e ne calcola il valore redox. Seguendo il leading edge dello stesso organoide per tre giorni di trattamento con differenti dosi del farmaco romidepsina, il software rileva spostamenti sottili nel metabolismo. Gli autori dimostrano che questo tracciamento organoide-per-organoide riduce la variabilità rispetto all’analisi aggregata di tutti gli organoidi, aumentando la potenza statistica per evidenziare gli effetti del farmaco anche quando le risposte differiscono tra i singoli minitumori.
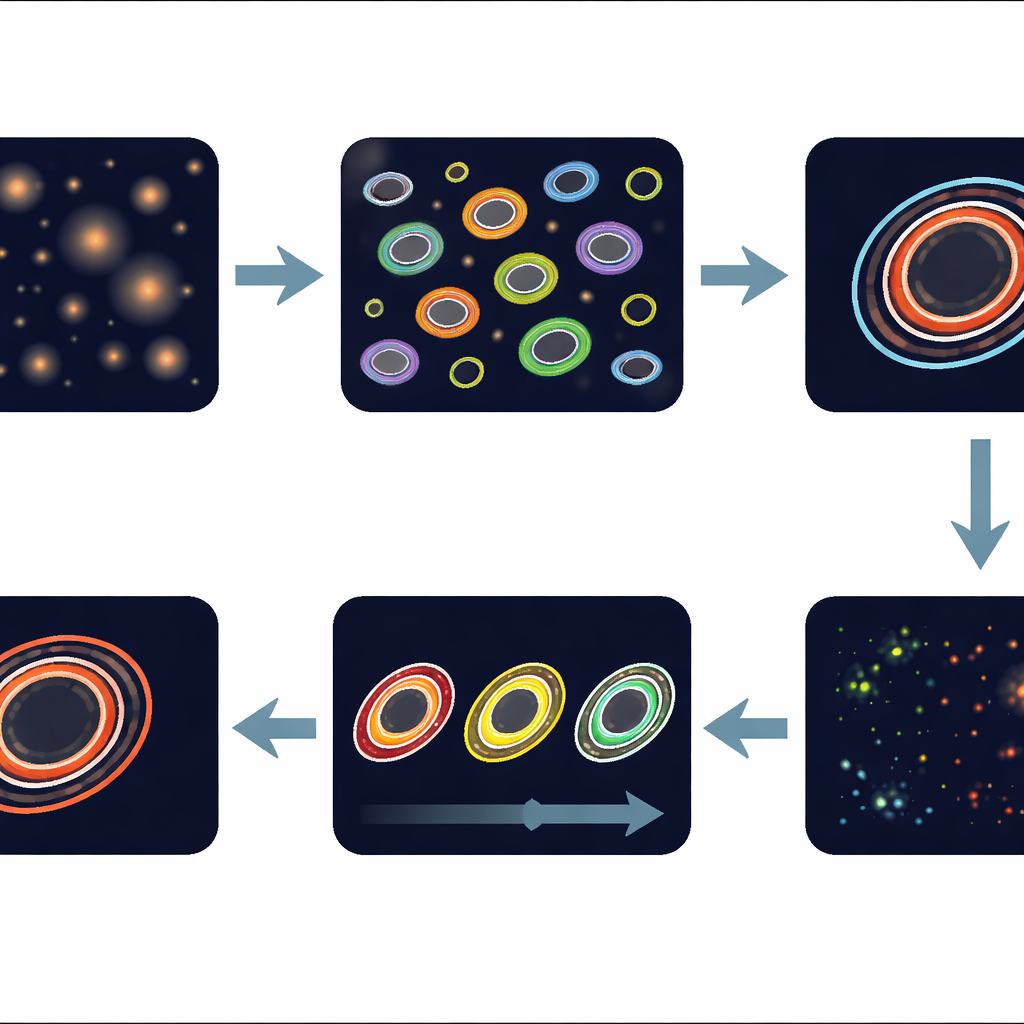
Risultati più rapidi e robusti per la risposta ai farmaci
I ricercatori hanno testato la loro pipeline su immagini provenienti da due diversi sistemi microscopici e hanno rilevato che i contorni automatizzati corrispondevano strettamente a quelli tracciati da esperti, e il tracciamento concordava con quello manuale per oltre il 94% dei casi. Quando hanno confrontato le misure complessive di risposta ai farmaci, il metodo automatizzato ha eguagliato la sensibilità dell’approccio manuale riducendo il tempo di analisi di oltre cento volte — da molte ore di lavoro umano a pochi minuti di elaborazione computazionale. Per i laboratori che lavorano con organoidi derivati da pazienti, questo significa che possono realisticamente analizzare grandi collezioni di immagini e scoprire come ogni minitumore reagisce al trattamento. A lungo termine, un’analisi automatizzata di questo tipo potrebbe avvicinare i test farmacologici basati su organoidi alla pratica clinica, supportando cure oncologiche più personalizzate ed efficaci.
Citazione: Hsu, A., Samimi, K., Gillette, A.A. et al. An automated image analysis pipeline for wide-field optical redox imaging of patient-derived cancer organoids. Sci Rep 16, 9757 (2026). https://doi.org/10.1038/s41598-026-40249-4
Parole chiave: cancro del colon-retto, organoidi derivati da pazienti, imaging redox ottico, analisi automatizzata delle immagini, risposta ai farmaci