Clear Sky Science · it
MyoFuse è un flusso di lavoro interamente basato su IA per la quantificazione automatizzata della fusione delle cellule muscolari scheletriche in vitro
Perché conta contare le cellule muscolari
Quando ci alleniamo, recuperiamo da una lesione o sviluppiamo malattie come il diabete, i nostri muscoli scheletrici si rimodellano continuamente. In laboratorio, gli scienziati riproducono questo processo coltivando cellule muscolari in una piastra e osservando come singole cellule si fondono in lunghi filamenti multinucleati. Un numero semplice, chiamato indice di fusione, indica quanto bene avviene questa fusione. Oggi però quel valore viene di solito ottenuto da persone che contano manualmente migliaia di minuscoli nuclei cellulari su uno schermo: un lavoro lento, soggetto a variabilità e errori. Questo studio presenta MyoFuse, un flusso di lavoro interamente basato su IA che automatizza questo compito di conteggio, con l’obiettivo di rendere la ricerca sul muscolo più rapida, affidabile e meno soggetta a bias.
La sfida di vedere ciò che è davvero presente
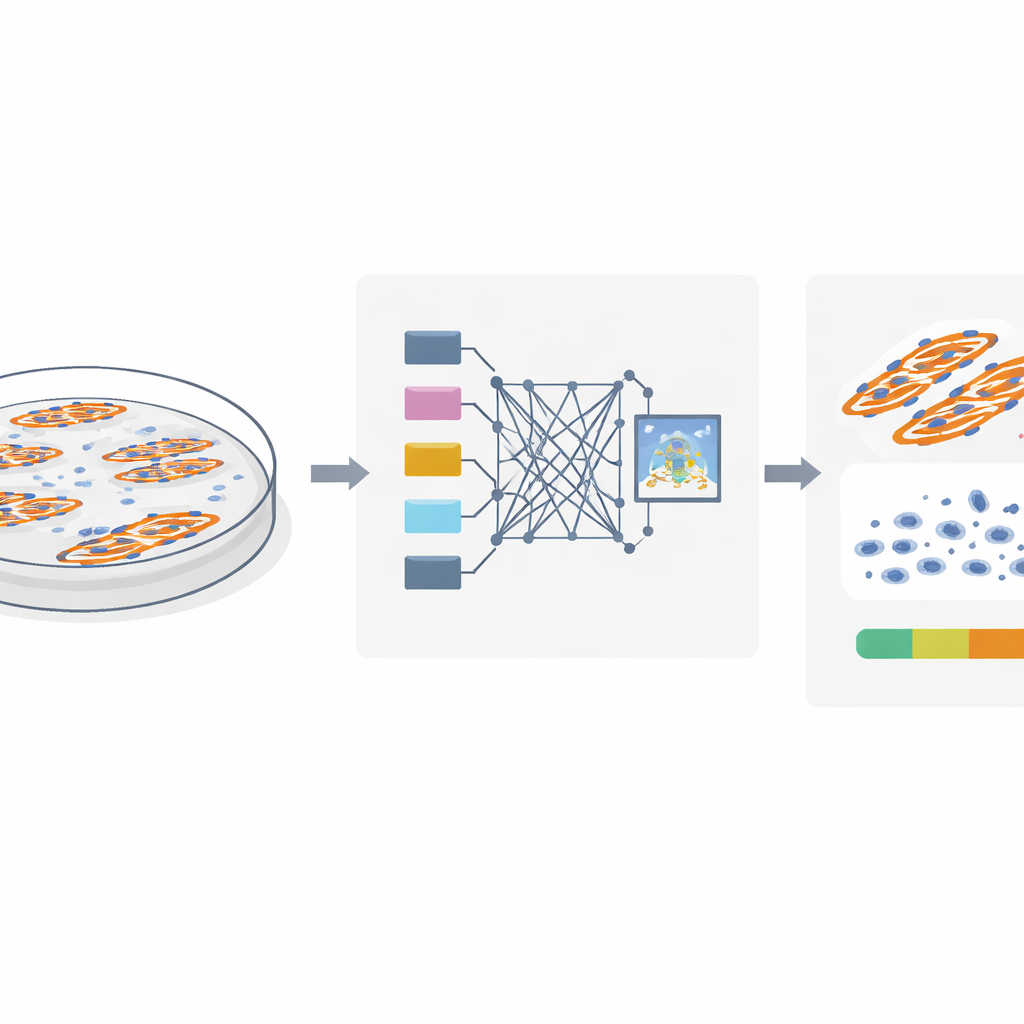
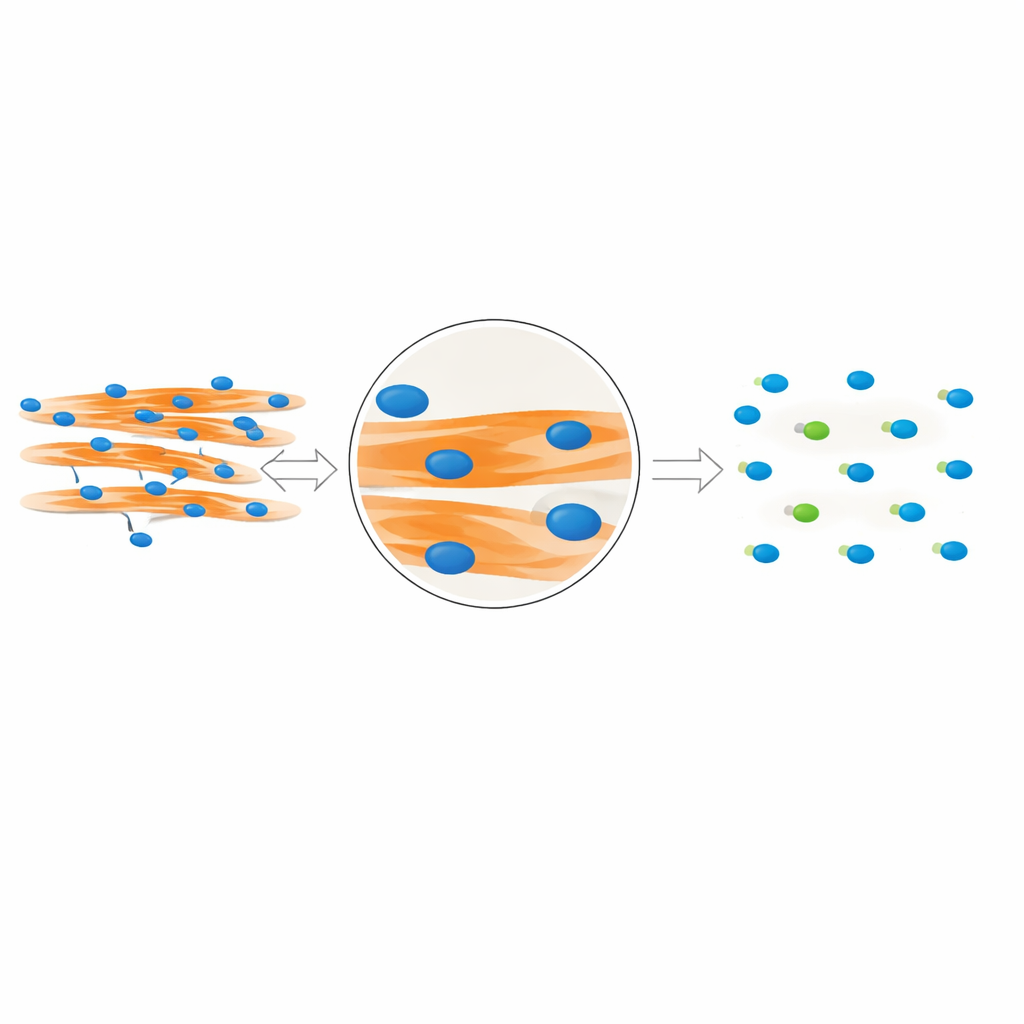
Per studiare la fusione delle cellule muscolari, i ricercatori colorano i nuclei e le fibre muscolari con coloranti fluorescenti e acquisiscono immagini al microscopio. La domanda chiave è quali nuclei si trovino effettivamente all’interno delle fibre fuse e quali appartengano a cellule non fuse che stanno nelle vicinanze. I metodi tradizionali presumono che se un nucleo si sovrappone a una fibra in un’immagine bidimensionale, allora debba essere all’interno di quella fibra. Tuttavia le cellule crescono in tre dimensioni: un nucleo può trovarsi sopra o sotto una fibra e apparire comunque sovrapposto nell’immagine. Gli autori utilizzano imaging confocale dettagliato sia su cellule muscolari di topo sia umane per mostrare che questo trucco della sovrapposizione può essere fuorviante, spingendo a includere molti nuclei vicini come se fossero parte delle fibre fuse e gonfiando così l’indice di fusione.
Un modo più intelligente di leggere le immagini fluorescenti
Il gruppo ha osservato che i veri nuclei “all’interno della fibra” lasciano un’impronta visiva distintiva. Poiché questi nuclei occupano fisicamente spazio all’interno della fibra, creano piccole interruzioni scure nel segnale fluorescente che marca la proteina muscolare MyHC. Al contrario, i nuclei che stanno sopra o sotto una fibra non disturbano questo segnale. Partendo da questa intuizione, gli autori hanno progettato MyoFuse, un flusso di lavoro IA in due fasi. Prima, un modello di segmentazione specializzato (adattato dallo strumento open source Cellpose) delimita con precisione i singoli nuclei, anche quando sono strettamente ammassati in gruppi. Secondo, una rete neurale leggera classifica il segnale MyHC circostante per ogni nucleo e decide se si trovi dentro o fuori dalla fibra, basandosi esclusivamente su questo pattern locale piuttosto che sulla semplice sovrapposizione.
Quanto bene l’IA corrisponde agli esperti umani
I ricercatori hanno testato in modo rigoroso MyoFuse su immagini di cellule muscolari C2C12 di topo e su cellule muscolari primarie umane provenienti da diversi muscoli. Per entrambe le specie, il conteggio totale dei nuclei fatto dall’IA e l’indice di fusione calcolato concordavano molto bene con le annotazioni manuali accurate degli esperti, mostrando correlazioni quasi perfette. A livello di singoli nuclei, il classificatore distingueva correttamente nuclei dentro e fuori dalle fibre in oltre il 90% dei casi nei vari dataset, con metriche di prestazione paragonabili alla discriminazione a livello umano. È importante che MyoFuse abbia funzionato bene anche su un set separato di cellule umane mai usato per l’addestramento, suggerendo che l’approccio può generalizzare a nuovi campioni invece di limitarsi a memorizzare le immagini di training.
Rivelare bias nascosti nei metodi comuni
Oltre alla sua accuratezza, MyoFuse ha messo in luce problemi sistematici nei metodi basati su maschere ampiamente usati che si affidano alla semplice sovrapposizione tra segnali nucleari e di fibra. Quando gli autori hanno confrontato gli indici di fusione ottenuti con MyoFuse e quelli derivanti da un approccio a maschera raffinato applicato alle stesse immagini, il metodo a maschera sovrastimava costantemente la fusione, specialmente nelle aree dove le fibre muscolari ricoprivano una frazione maggiore della piastra. Modificare le soglie di rilevamento cambiava i numeri ma non eliminava questo bias di fondo; i miglioramenti apparenti spesso derivavano da errori che si annullavano a vicenda piuttosto che da una migliore rappresentazione biologica. Il gruppo ha anche mostrato che le stime di fusione possono variare notevolmente tra diverse regioni di una stessa pozza, sottolineando che analizzare solo pochi campi scelti a mano può dare una visione distorta di quanto le cellule si stiano effettivamente fondendo.
Cosa significa per la ricerca sul muscolo futura
MyoFuse offre ai biologi del muscolo un modo per misurare la fusione cellulare che è sia più rapido sia più fedele a ciò che accade realmente in piastra. Combinando microscopia automatizzata con un’IA in grado di segmentare e classificare centinaia di migliaia di nuclei in pochi minuti, il flusso di lavoro riduce il carico di lavoro umano, minimizza le scelte soggettive su dove guardare e come impostare le soglie delle immagini, ed evita di contare cellule vicine come muscolo fuso. Gli autori riconoscono che condizioni di imaging estreme o protocolli di colorazione molto diversi potrebbero richiedere un riaddestramento, ma il metodo è reso disponibile pubblicamente ed è progettato per essere adattabile. Per i laboratori che studiano sviluppo muscolare, invecchiamento, rigenerazione o malattie metaboliche, MyoFuse promette misure di fusione più robuste e, con esse, conclusioni più affidabili su come i muscoli crescono e cambiano.
Citazione: Lair, B., Cazorla, C., Lobeto, A. et al. MyoFuse is a fully AI-based workflow for automated quantification of skeletal muscle cell fusion in vitro. Sci Rep 16, 9387 (2026). https://doi.org/10.1038/s41598-026-40047-y
Parole chiave: muscolo scheletrico, fusione cellulare, intelligenza artificiale, analisi delle immagini, miotogenesi