Clear Sky Science · it
La dinamica dell’actina mediata da caldesmon-1 è essenziale per la differenziazione osteogenica delle cellule interstiziali della valvola aortica
Perché l’irrigidimento delle valvole cardiache è importante
Con l’invecchiamento, una delle porte principali del cuore — la valvola aortica — può progressivamente irrigidirsi e diventare dura come una roccia. Questa condizione, chiamata stenosi aortica, costringe il cuore a pompare con maggiore sforzo e può portare a insufficienza cardiaca. Oggi gli unici trattamenti affidabili sono la sostituzione valvolare chirurgica o per via catheteristica. Lo studio riassunto qui si pone una domanda fondamentale: che cosa trasforma gradualmente il tessuto morbido e flessibile della valvola in materiale simile all’osso? Identificando un attore molecolare chiave in questo processo, la ricerca indica possibili farmaci futuri che potrebbero rallentare o prevenire la calcificazione valvolare invece di limitarsi a sostituire la valvola danneggiata.
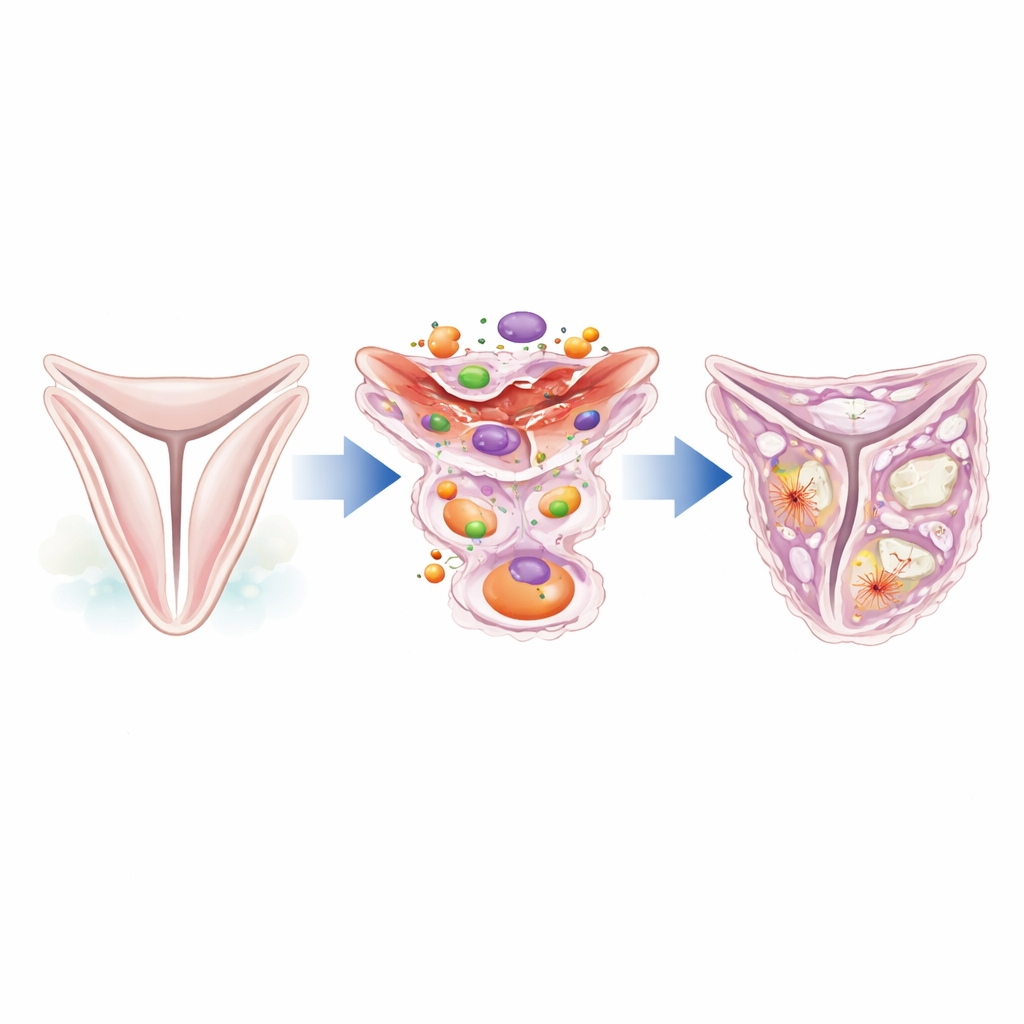
Uno sguardo più ravvicinato ai lavoratori nascosti della valvola
Le cuspidi della valvola aortica sono sostenute da uno strato sottile di cellule di supporto specializzate note come cellule interstiziali valvolari. In una valvola sana queste cellule restano quiescenti e contribuiscono a mantenere la struttura del tessuto. Sotto stress o dopo un danno, però, possono cambiare identità e comportarsi come cellule che formano tessuto cicatriziale o addirittura tessuto osseo. Gli autori si sono concentrati su una proteina chiamata caldesmon-1, che aiuta a controllare l’impalcatura interna delle cellule costituita da filamenti di actina. Analizzando dati di single-cell RNA sequencing già disponibili da valvole umane, hanno scoperto che caldesmon-1 è fortemente aumentata nelle valvole di pazienti con stenosi aortica rispetto a valvole normali, in particolare nelle cellule interstiziali presenti nelle regioni ispessite e fibrotiche.
Dal tessuto flessibile a macchie fibrotiche e simili all’osso
Studi microscopici su campioni di valvola umana hanno rivelato che la proteina caldesmon-1 è abbondante nelle cuspidi malate e si associa a marcatori di cellule attivate, contrattili e di tipo fibroblastico che producono collagene. Queste cellule ricche di caldesmon-1 si raggruppano attorno ad aree di fibrosi e calcificazione precoce, suggerendo che contribuiscono a costruire la matrice extra che ispessisce la valvola. Ulteriori analisi hanno mostrato che queste cellule esprimono geni tipici di tipi cellulari simili alla muscolatura liscia e predisposti all’osteogenesi, e sono produttori principali di proteine strutturali come il collagene di tipo I. In altre parole, ovunque la valvola si stia irrigidendo e cicatrizzando, le cellule interstiziali positive per caldesmon-1 sono presenti sulla scena.
Come una proteina che governa la forma spinge le cellule verso l’osso
Per comprendere causa ed effetto, il gruppo ha isolato cellule interstiziali valvolari umane e ha usato piccoli RNA interferenti per ridurre l’espressione di caldesmon-1. In assenza di questa proteina, le cellule persero la forma allungata e a fuso e divennero più tondeggianti. I loro filamenti di actina interni si assottigliarono e diminuirono la capacità di dividere e muoversi in modo direzionale. Quando i ricercatori esposero queste cellule a un mezzo di coltura osteogenico, ovvero che stimola la formazione ossea, le cellule normali formarono facilmente depositi di calcio, mentre le cellule private di caldesmon-1 mostrarono una minore mineralizzazione. Sequenziamenti RNA su larga scala confermarono che molti geni coinvolti nella formazione ossea e nel rimodellamento tissutale, inclusi noti driver osteogenici come RUNX2 e la fosfatasi alcalina, venivano fortemente attivati dalle condizioni osteogeniche ma non aumentavano quando caldesmon-1 era silenziata.
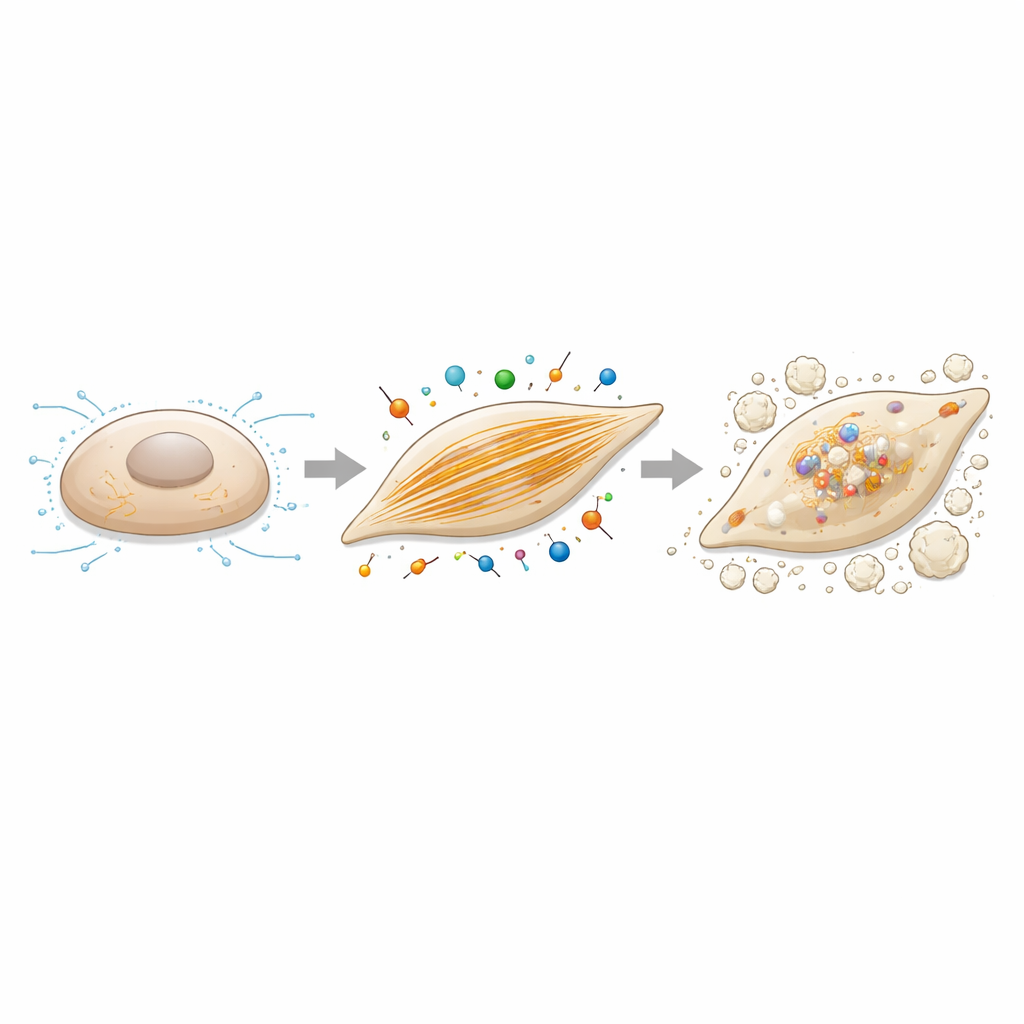
I filamenti di actina come leva di controllo per la calcificazione
Poiché caldesmon-1 regola l’actina, gli autori si sono chiesti se modificare direttamente l’assemblaggio dell’actina avrebbe cambiato la tendenza delle cellule a calcificare. Hanno trattato le cellule interstiziali valvolari con citochalasin B, un composto che interrompe in modo controllato la crescita dei filamenti di actina, applicando al contempo le stesse condizioni culturali promotrici di osteogenesi. A dosi che non compromettevano seriamente la sopravvivenza cellulare, questo trattamento ridusse nettamente la deposizione di calcio e abbassò l’espressione di geni correlati all’ossificazione, inclusi caldesmon-1 e RUNX2. Insieme agli esperimenti di silenziamento, questi risultati dipingono un quadro coerente: reti robuste di filamenti di actina e le forze contrattili che esse sostengono non sono semplici spettatori, ma guidano attivamente il passaggio da cellule di supporto quiescenti a cellule formanti osso nella valvola.
Cosa significa questo per i trattamenti futuri
Per il pubblico generale, il messaggio principale è che l’irrigidimento della valvola aortica è un processo attivo e regolato, non un semplice “logoramento”. Questo studio identifica caldesmon-1 come un coordinatore centrale che collega lo scheletro interno della cellula al programma genetico per la produzione di tessuto simile all’osso. Favorendo nelle cellule interstiziali valvolari un’identità contrattilе, fibrotica e infine osteogenica, caldesmon-1 contribuisce direttamente all’accumulo di depositi duri che restringono la valvola. Sebbene qualsiasi terapia diretta contro questa proteina o contro la dinamica dell’actina richiederà test approfonditi per evitare effetti indesiderati in altri tessuti, le vie mediate da caldesmon-1 emergono ora come candidati promettenti per farmaci destinati a rallentare o arrestare la calcificazione valvolare prima che sia necessario l’intervento chirurgico.
Citazione: Komoda, M., Sakaue, T., Nakao, Y. et al. Caldesmon-1–mediated actin dynamics is essential for osteogenic differentiation of aortic valve interstitial cells. Sci Rep 16, 9385 (2026). https://doi.org/10.1038/s41598-026-39938-x
Parole chiave: calcificazione della valvola aortica, caldesmon-1, cellule interstiziali valvolari, citoscheletro di actina, differenziazione osteogenica